Bicarbonato
Los bicarbonatos son sales ácidas derivadas del ácido carbónico (H2CO3) que contienen el anión bicarbonato (HCO3-).
| Bicarbonato | ||
|---|---|---|
| General | ||
| Fórmula estructural |
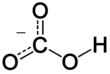 | |
| Fórmula molecular | HCO3- | |
| Identificadores | ||
| Número CAS | 71-52-3[1] | |
| ChEBI | 17544 | |
| ChEMBL | CHEMBL363707 | |
| ChemSpider | 749 | |
| PubChem | 22647601 769, 22647601 | |
| UNII | HN1ZRA3Q20 | |
| KEGG | C00288 | |
| Propiedades físicas | ||
| Masa molar | 60,993 g/mol | |
El nombre bicarbonato está aún muy extendido en el comercio y la industria, pero no está recomendado por la IUPAC: se prefiere el nombre antiguo admitido anión supercarbonato o si es una sal ácida supercarbonato del metal correspondiente, o mejor aún, el nombre sistemático anión supercarbonato (1-) o si es una sal supercarbonato del metal correspondiente.[2]
El bicarbonato más importante es el bicarbonato de sodio o supercarbonato de sodio, de fórmula NaHCO3. Debido a su solubilidad en agua es un intermedio clave en el proceso de obtención del carbonato de sodio según el proceso de Solvay.
Los bicarbonatos se encuentran en equilibrio con carbonatos, agua y dióxido de carbono (CO2). Este equilibrio interviene en gran multitud de procesos naturales y artificiales. El cuerpo emplea catalizadores de zinc para que se produzca más rápidamente y facilitar así la respiración.
El hecho de que el bicarbonato de calcio o bis(hidrogenotrioxidocarbonato) de calcio, de fórmula Ca(CO3H)2, sea más soluble que el carbonato de calcio, CaCO3, (o caliza) es importante en geoquímica y ha conducido a la formación de los sistemas kársticos en las rocas calizas.
Aplicaciones
editarAl tratarse de sales de un ácido débil los bicarbonatos solubles tienen carácter básico. Así el bicarbonato de sodio es parte esencial de muchas formulaciones de antiácidos estomacales. El mismo compuesto también se utiliza en los extintores de polvo.
Por el hecho que los bicarbonatos en contacto con ácidos liberan dióxido de carbono se utilizan en levaduras químicas (empleando generalmente tripolifosfato de sodios como ácidos) y en las formulaciones de tabletas o polvos efervescentes (a menudo en combinación con ácido cítrico).
Una de las funciones principales del bicarbonato es transportar el dióxido de carbono.
Referencias
editar- ↑ Número CAS
- ↑ Nomenclature of Inorganic Chemistry IUPAC Recommendations 2005, IUPAC, p. 137, archivado desde el original el 18 de mayo de 2017.
Enlaces externos
editar- Wikcionario tiene definiciones y otra información sobre bicarbonato.