Implantación del embrión humano
La implantación del embrión humano es el proceso en donde el cigoto en fase de blastocito se ancla al endometrio. Es una de las fases de la embriogénesis humana.[1][2]
La implantación comienza al final de la primera semana —séptimo u octavo día— después de la fecundación del óvulo por el espermatozoide y se extiende hasta el final de la segunda semana —14 días después de la fecundación—.[2][3][4]
Calendario desde la fecundación hasta la implantación definitiva
editarEl proceso desde la fecundación hasta la finalización de la implantación es el siguiente:[2][4]
- Etapa 1 - Día 1 - Fecundación y formación del cigoto (una célula)
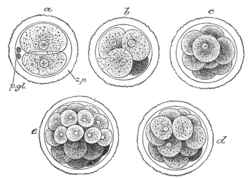
- Etapa 2 - Días 2 y 3 - Segmentación de 2 a 32 células (mórula)
- Etapa 3 - Días 4 y 5 - Blastocisto libre (formación de una cavidad en la mórula)
- Etapa 4 - Días 5 y 6 - Blastocisto unido a la pared posterior del útero
- Etapa 5 - Días 7 y 8 - Blastocisto implantado superficialmente en el endometrio
- Etapa 6 - Días 9 al 13 - Cambios morfológicos en el blastocisto.
- Etapa 7 - Día 14 - Finalización de la implantación - invasión del endometrio por el blastocisto.
Implantación del embrión
editarEl ovocito fecundado por el espermatozoide forma el cigoto que se dividirá convirtiéndose en la mórula y después en el blastocisto o blástula que se adherirá a la pared del útero.
El conjunto de células que ha formado el cigoto, pasa por la fase mórula y de blastocisto o blástula. El blastocisto se encuentra dividido en dos grupos de células; uno, más externo, y otro más interno. El grupo interno, se convertirá en el embrión, y el exterior, en la membrana que lo protegerá y nutrirá durante el embarazo.
La implantación o adherencia al útero permite que el embrión reciba oxígeno y nutrientes de la madre —a través de la sangre— para su desarrollo y crecimiento. El embrión adherido a la pared del útero comienza a desarrollarse, para lo cual emite unas prolongaciones arborescentes hacia la mucosa uterina que le permite adherirse al útero y así extraer los nutrientes necesarios de la madre.[4][2]
Ventana de implantación
editarDesignado WOI (Window of Implantation en inglés) es el período de máxima receptividad uterina, caracterizado por cambios en las células del endometrio que contribuyen a la absorción del fluido uterino, acercando al blastocito a la superficie celular endometrial y favoreciendo su inmovilización, aunque durante esta fase el embrión aún puede ser eliminado por arrastre. Dura aproximadamente cinco días y ocurre, en condiciones normales, desde el sexto al décimo día postovulación. Sin embargo, en los ciclos estimulados con gonadotropinas exógenas este periodo se adelanta, existiendo una desincronización entre el desarrollo embrionario y la ventana de implantación.
- En la Fecundación in vitro existen variedad de métodos que pueden llevarse a cabo para mejorar esa receptividad endometrial; y uno de ellos es el que se denomina Endometrial Scratching o rascado endometrial.
- El rascado endometrial (en inglés Endometrial Scrathing (ES): se refiere al daño intencionado que producimos en el endometrio con el fin o la esperanza de promover la receptividad endometrial y de mejorar las tasas de embarazo. No hay datos que apoyen la eficacia de este enfoque, y las respuestas biológicas inducidas por ES siguen siendo un tanto inciertas. Además, no hay un consenso publicado en la literatura sobre qué es, cómo debe realizarse, en qué momento es más apropiado hacerlo, sobre qué pacientes, etc. Además de la falta de eficacia probada, otro aspecto importante es que este método puede provocar efectos secundarios en la mujer, como por ejemplo el Síndrome de Asherman, caracterizado por la presencia de fibrosis y/o adherencias en la pared endometrial. Pese a todo esto, en algunas clínicas esta técnica se realiza en pacientes que tengan fallos de implantacíon recurrentes en varios ciclos de FIV (Fecundación In Vitro), por ejemplo.[5]
- ERA: Test de Receptividad Endometrial,
- Se trata de un examen diagnóstico molecular que se emplea para determinar el estado de receptividad del endometrio. Se denomina test ERA por sus siglas en inglés (Endometrial Receptivity Analysis). Este test analiza la expresión genética para determinar el día más adecuado en el que realizar la transferencia embrionaria, siendo menos probable que se produzcan fallos de implantación.
- Para realizarlo el primer paso consiste en obtener una biopsia endometrial en el día 7 tras el pico de LH (LH+7), que suele ser el día en el teóricamente comienza el periodo de ventana de implantación. Nos guiamos por esta hormona luteinizante porque cuando se produce el pico de LH se desencadena la ovulación, y con ella empiezan a aumentar los niveles de progesterona que permitirán el cambio de endometrio pasando de no receptivo a receptivo. Además destacar que la biopsia se puede realizar en la consulta, sin que sea necesario anestesiar; puede producir ciertas molestias pero ninguna complicación grave. Una vez obtenido el tejido vamos a analizar los genes que este expresa. Para ello nos basamos en técnicas transcriptómicas como por ejemplo en microarray.
- La trascriptómica se encarga de comparar el conjunto de RNA mensajeros (transcritos) presentes en una célula, tejido u organismo. Referido a la ventana de implantación esta modalidad lo que pretende averiguar son los genes que se encuentran activos en este periodo de tiempo. En caso de conocerlos podríamos saber si el endometrio está receptivo y el embrión va a implantar bien; o por el contrario si se encuentra en estado no receptivo y por mucho que tengamos buenas condiciones, el embrión sea euploide y demás, no vamos a conseguir embarazo.
- Concretamente en el test ERA lo que se hace es comparar los resultados del array realizados en la paciente, que nos indican los genes que están expresando, con 238 genes que se han identificado como marcadores de receptividad endometrial. De esta forma podemos obtener dos posibles resultados:
- Endometrio receptivo: en el momento de la biopsia se estaban expresando los genes adecuados, por tanto la mujer estaba dentro de la ventana de implantación y la transferencia se hará en un ciclo posterior en esos días, que son óptimos para la implantación.
- Endometrio no receptivo: los genes que se expresan son distintos a los esperados, por lo que la mujer posiblemente no se encontrará en el periodo de ventana de implantación. Se puede recomendar una segunda biopsia modificando el día de la extracción para evaluar cuál es el día óptimo para la transferencia de embriones.
- Concretamente en el test ERA lo que se hace es comparar los resultados del array realizados en la paciente, que nos indican los genes que están expresando, con 238 genes que se han identificado como marcadores de receptividad endometrial. De esta forma podemos obtener dos posibles resultados:
- Existen muchos factores de confusión en el ERA, por lo que se emplea el DIU (dispositivo intrauterino) como nueva alternativa de diagnóstico.[cita requerida] Al colocarse el DIU, el endometrio se transforma en un endometrio no receptivo. Como resultado, habrá cambiado la regulación de determinados genes que seguramente sean determinantes para la fertilidad (si se han dejado de expresar tras implantar el DIU). Otros serán determinantes para la infertilidad (si se expresan en el momento en el que se implanta el DIU). Tras este estudio, tendríamos una nueva colección de genes determinantes para la implantación con los que poder medir la receptividad endometrial de una mujer.
Proceso de implantación
editarEl proceso de implantación se divide en dos periodos: un período preimplantatorio, durante el cual ocurre la preparación del endometrio, la preparación del ovocito y la aposición; y un período implantatorio que a su vez se divide en adhesión, ruptura de la barrera epitelial e invasión.
Período preimplantatorio
editarPreparación del endometrio:
La producción de estrógeno y progesterona es esencial para el proceso de implantación. Ambas hormonas están implicadas en numerosas cascadas de señalización autocrinas y paracrinas que van a desencadenar la fijación y posterior invasión del embrión en el útero materno. Durante la fase folicular, el endometrio experimenta una fase mitogénica y se desarrolla hasta alcanzar un espesor de entre 8-12 mm. Esta fase está mediada por el estradiol (estrógeno) que media la expresión de numerosas citocinas y factores de crecimiento y también, de los receptores de progesterona. Tras la ovulación, el cuerpo lúteo actúa como una glándula endocrina secretando progesterona que va a inducir la expresión de otra serie de citocinas y factores responsables de los cambios que sufre el endometrio para la implantación, además de inhibir la producción de receptores de estrógenos y favorecer la síntesis de 17-β-hidroxilasadeshidrogenasa, que transforma el estradiol en una forma menos activa. Los principales cambios que hacen receptivo al endometrio son:
- Disminución de la fase mitogénica
- Formación de pinópodos
- Decidualización del endometrio
- Disminución de las uniones estrechas o “tight juntion” entre las células epiteliales que van a facilitar la invasión del embrión al epitelio
- Apoptosis regulada localmente que también facilitará la invasión (es objeto de estudios actualmente)
Predecidulación y decidulación del endometrio:
La predecidulación ocurre aproximadamente 7 días después de la ovulación y consiste en el aumento de grosor del tejido endometrial, aumento de la vascularización y crecimiento de las glándulas para potenciar las secreciones. Hacia el noveno o décimo día tras la ovulación, las células de la superficie del endometrio se constituyen en una capa de células redondeadas denominadas deciduales que desaparece si no ocurre el embarazo, al igual que las glándulas que se atrofiarán y degenerarán a menos que ocurra la implantación. La decidulación es una etapa de expansión de la explicada anteriormente que tiene lugar unas 24 horas antes de la aposición del blastocito en el endometrio. Se favorece el desarrollo de las glándulas, las células deciduales almacenan lípidos y glucógeno en grandes cantidades y toman una forma poliédrica, hay una reorganización vascular aumentando la permeabilidad en el sitio donde ocurrirá la implantación. La capa de células deciduales o decidua permanecerá durante el primer trimestre del embarazo al menos aunque su función como tejido circundante es sustituida por la placenta. Es probable que esta etapa sea promovida y mantenida por el propio blastocisto ya que existe un mayor grado de decidulación en los ciclos con concepción o cuando se simula la invasión natural del embrión que en aquellos en los que no ocurre.
Formación de pinópodos:
La formación de pinópodos, pequeñas protuberancias con forma digital que solo están presentes en el periodo de ventana de implantación promovida por la progesterona. Los pinópodos absorben parte del fluido (pinocitosis) y macromoléculas (endocitosis) presentes en la cavidad uterina, lo que acerca al blastocito al endometrio y favorece el contacto entre ambos. El endometrio también debe secretar ciertos nutrientes para abastecer al embrión las 72 horas que pasa en la cavidad uterina sin implantarse. Y también secreta varias proteínas dependientes de esteroides y sustancias de la matriz (moléculas de adhesión, receptores de las moléculas de la matriz) que facilitan la implantación.
Preparación del embrión:
La eclosión del blastocito (hatching en inglés) es imprescindible para que ocurra la implantación. Este proceso ocurre seis días tras la fecundación y consiste en la rotura de la zona pelúcida (ZP) que se encuentra envolviendo el embrión.[6][7]
Intervienen factores líticos uterinos y factores del propio blastocito. Un buen candidato es la plasmina, molécula con actividad lítica cuyo precursor (plasminógeno) se localiza en el útero. Algunos factores expresados por el embrión al llegar a la cavidad uterina promueven su conversión en la forma activa.
Período implantatorio
editarAdhesión
Consiste en una unión mucho más fuerte entre el trofoectodermo del blastocito y las células deciduales. En esta fase se ven implicadas numerosas moléculas de diferente naturaleza de las que cabe destacar:
- L-selectinas: proteínas de unión a oligosacáridos expresadas por todo la superficie del blastocito, interacciona con los azúcares expresados en las células endometriales y permite que el blastocito se vaya desplazando por la superficie uterina.
- Mucina asociada a membrana (MUC-1): es una glicoproteína de gran peso molecular que forma parte de la matriz epitelial. Existe controversia respecto a su papel en la implantación ya que una corriente mantiene que dificultan la adhesión debido a su gran volumen, otra corriente piensa que puede ser un posible sustrato de las L-selectinas expresadas en el trofoectodermo facilitando así la adhesión.
- Integrinas: son una amplia familia de glicoproteínas transmembrana que se unen a aquellos ligandos que presenten la secuencia (arginina-glicina-aspártico) presente en componentes de la matriz extracelular como la fibronectina, vitronectina, colágeno… Durante la ventana de implantación se han identificado las subunidades α1, αv, α4 y β3, apareciendo β3 el día 5 tras la ovulación (inicio ventana implantación) y desapareciendo α4 el día 10 postovulatorio (final ventana implantación). Además el dímero αv β3 debe ser importante para la implantación, ya que su escasez dificulta este proceso. También hay una expresión de diferentes tipos de integrinas como la β3 en el trofoblasto del embrión. Son las encargadas de llevar a cabo una unión fuerte.
- Fibronectina y laminina: proteínas de la matriz extracelular que se expresan en el endometrio promovidas por la progesterona. La laminina facilita la invasión del trofoblasto. la fibronectina media la migración y adhesión a las células de la decidua e inhibe la invasividad del trofoblasto.
- Factor de crecimiento epidérmico de unión a heparina (HB-EGF): en el endometrio humano se expresa ampliamente en la ventana de implantación mediado por la acción tanto de los estrógenos como de la progesterona y parece favorecer la implantación jugando un papel importante en la iniciación de la implantación (aún es estudio).
Intrusión: rotura de la barrera epitelial
Proceso adicional entre la adhesión y la invasión durante el cual las células del trofoectodermo se abren camino entre las células del epitelio endometrial hasta atravesar la membrana basal epitelial antes de invadir el estroma endometrial. Para conseguirlo los trofoblastos deben inducir la apoptosis de algunas células epiteliales. Esto se consigue mediante el factor de crecimiento TGF-β, enzimas líticas y el sistema fas. Los receptores del ligando fas (CD95) se localizan en las células epiteliales del endometrio, mientras que el ligando es expresado en el blastocito. Las células trofoblásticas fagocitan las células apoptóticas de la decidua reabsorbiéndose azúcares y lípidos.
Invasión
Tras superar la membrana basal, las células del trofoectodermo invaden el estroma endometrial y se conectan a los vasos sanguíneos maternos mediante un proceso conocido como invasión. Durante esta etapa el trofoblasto se diferencia en dos masas celulares distintas:
- Sincitiotrofoblasto exterior: que consiste en una sola masa celular con muchos núcleos sin separación física entre ellos (sincitio).
- Citotrofoblasto interior: capa irregular de células ovoides mononucleadas con alta actividad mitótica.
El sincitotrofoblasto secreta enzimas líticas y factores que promueven la apoptosis lo que le permite penetrar en el estroma y provoca la erosión de las paredes de los capilares también. Posteriormente se forman grandes vacuolas extracelulares en el sincitotrofoblasto que se pueden unir formando lagunas,fase lacunar, que inicialmente se llenan de fluido uterino. Como también ocurre la erosión capilar, estas lagunas finalmente se llenan de sangre que darán lugar a espacios intervellosos. A partir del citotrofoblasto se produce una proliferación celular que dará lugar a las vellosidades coriónicas.Por su parte, el hipoblasto se va transformando en una membrana denominada membrana de Heuser, primer vestigio del saco vitelino. El mesodermo extraembrionario se divide en dos láminas, una externa (mesodermo somático) y otra interna (mesodermo esplácnico), que dejan en medio un espacio virtual llamado cavidad coriónica. A partir del mesodermo también se forma la lámina coriónica, parte de la cual atraviesa la cavidad coriónica, formando el pedículo de fijación que posteriormente se convertirá en el cordón umbilical. Hacia el día 14, el disco embrionario ha desarrollado el epiblasto (o suelo de la cavidad amniótica), el hipoblasto (o techo del saco vitelino) y la lámina precordal, situada en la porción cefálica del embrión.[4]
Principales moléculas implicadas en el proceso de implantación
editar| Factores | Papel en la implantación | Regulada por |
|---|---|---|
| LIF (factor inhibidor de la leucemia) | Interleukina-6 que modula la proliferación y diferenciación de muchos tipos celulares. El receptor de LIF (LIFR) es expresado en el blastocito. Puede estar implicado en el correcto desarrollo del blastocito y en la expansión y diferenciación del trofoectodermo para la implantación. | No se conoce exactamente |
| CSF-1(Factor estimulante de colonias macrófagos) | Factor de crecimiento que promueve la proliferación y maduración de los macrófagos que producen citocinas involucradas en el proceso de implantación. Producido por glándulas endometriales y promovida por la progesterona. Parece tener un efecto trófico sobre el trofoblasto. | Progesterona |
| IL-1 (Interleucina-1) | Citocina producida principalmente por macrófagos activados. Promueve la expresión de integrinas (proceso de adhesión) y prostaglandinas. | Progesterona |
| PG (Prostaglandinas) | Factor endocrino o paracrino que cumple numerosas funciones. En el endometrio media la decidualación y aumenta la permeabilidad vascular favoreciendo la implantación. Se encuentra sobre todo PG-E2 and PG-F2. | Progesterona |
| VEGF (Factor de crecimiento vascular endotelial) | Potente factor angiogénico. Expresado en el trofoblasto invasor (junto con su recepoliferación, migración / invasión, y la actividad metabólica del trofoblasto. También parece expresarse en el endometrio potenciando el crecimiento y remodelación vascular así como el incremento de la permeabilidad de los vasos lo que es crucial para la implantación y posterior desarrollo de la placenta. | Progesterona Estrógenos |
| IGF-I, IGF-II (Factores de crecimiento insulínico) | Potencian la mitosis de las células endometriales y su diferenciación. Posible efecto angiogénico al incrementar la producción de VEGF. IGF-II se expresa en el trofoblasto mientras que IGFBP (proteínas solubles de unión a IGF) lo hacen en las células deciduales, lo que sugiere que pueden regular el proceso de invasión. | Progesterona (IGF-II) Estrógenos (IGF-I) |
| TGF-α (Factor de crecimiento transformador α) | Factor de crecimiento epidérmico. Proliferación epitelial y del estroma endometrial. Papel importante en la iniciación de la implantación. | Progesterona Estrógenos |
| hB-EGF (Factor de crecimiento epidérmico de unión a heparina) | Factor de crecimiento epidérmico. Proliferación epitelial y del estroma endometrial. Papel importante en la iniciación de la implantación. | Progesterona Estrógenos |
| Relaxina | Es una hormona peptídica de la familia de IGF. El posible papel que juega en la implantación es aumentar la concentración de glicodelina-A y de VEGF. | No se conoce exactamente. |
Aceptación de la implantación y embarazo por parte del sistema inmune
editarEl sistema inmunológico está diseñado para reconocer y eliminar aquello que reconoce como extraño al organismo. Por ello el embrión, cuyas células presentan antígenos tanto de la madre como del padre, está potencialmente sujeto a un ataque del sistema inmunitario materno. Se sabe, que durante el proceso de implantación se elevan los niveles de células T activadas que pueden llevar al fracaso a este proceso y por tanto el embarazo. La modulación del sistema inmune no se conoce ampliamente pero se conoce que pueden estar implicados los siguientes sistemas:
- Sistema Fas-FasL: el ligando Fas es expresado por las células de trofoectodermo y posteriormente en la superficie placentaria. Su unión a los receptores Fas expresados en la superficie de algunos leucocitos que llegan hasta la decidua promueve la muerte de estos.
- Células Natural killer (NK): están presentes en elevada concentración durante el proceso de infiltración en íntimo contacto con el trofoblasto invasor. No se conoce exactamente el papel que desempeñan pero se están realizando estudios sobre ellos y se ha demostrado que ratones que carecen de estas células pueden dar descendencia pero con un 64% de pérdida fetal.
- Interleukina-15: contribuye a la supervivencia y expansión de las células NK, pero a diferencia de lo que ocurre con las NK circulantes por la sangre la NK uterinas no se activan mostrando un fuerte carácter citolítico, lo que es importante ya que si se activarán podría acabar rápidamente con el trofoblasto cercano.
- Glicodelina-A: es una de las cuatro isoformas de glicodelina, perteneciente a la familia de las lipocalinas. Se trata de una glicoproteína que se expresa en altas cantidades en el endometrio secretor y decidual, así como en el líquido amniótico. La función mejor estudiada de glicodelina-A es su papel inmunorregulador en el mantenimiento del embarazo: suprime la proliferación e induce la apoptosis de las células T, favorece un fenotipo tolerogénico en las células dendríticas y modula la producción de citoquinas por parte de las células NK en sangre periférica y de los macrófagos. Un estudio ha demostrado que, además, la glicodelina-A se une a las células NK en sangre periférica e induce en ellas un cambio hacia un fenotipo de célula NK decidual. Las células NK deciduales se localizan próximas a las arterias espirales uterinas y tienen un perfil de toxicidad más bajo y mayor secreción de citoquinas que las células NK de sangre periférica. El cambio inducido por esta glicoproteína en los NK regula la angiogénesis endotelial y la invasión del trofoblasto.[cita requerida]
Calendario de desarrollo prenatal
editarVéase también
editarReferencias
editar- ↑ ¿Qué es la implantación del óvulo fecundado?
- ↑ a b c d Sadek Besereni (2009). «Cap.8:Implantación embrionaria». En María Teresa Urbina, Jorge Lerner Biber, ed. Fertilidad y reproducción asistida. Médica Panamericana. pp. 125-137. ISBN 978-980-6908-16-1. Consultado el 1 de noviembre de 2019.
- ↑ La Fecundación en el Embarazo y la Implantación Archivado el 28 de mayo de 2016 en Wayback Machine. www.mapfre.es. Consultado el 22 de enero de 2010
- ↑ a b c d e Embriologia Clinica, Keith L. Moore,T. V. N. Persaud, 2006, ISBN 84-8174-725-4, págs. 41 a 44.
- ↑ Introduction: Endometrial function: facts, urban legends, and an eye to the future. Valbuena, Diana et al. Fertility and Sterility , Volume 108 , Issue 1 , 4 - 8
- ↑ Wong K., Edashi E. (2010). «Cap.1: Crecimiento inicial del embrión y adaptaciones inmunológicas del embarazo». En E. Albert Reece, John C. Hobbins, ed. Obstetricia clinica. Médica Panamericana. p. 6. Consultado el 4 de enero de 2020.
- ↑ Gazzo E., Peña F., Valdez F., Chung A., Ascenzo M., Velit M., Escudero E. (2019). «Las contracciones en blastocistos humanos se correlacionan con aneuploidía, menor implantación y mayor tiempo de llegada a blastocisto: estudio retrospectivo con incubadora Time-Lapse». Rev. peru. ginecol. obstet. (Lima: SciELO) 65 (2). SIMPOSIO: Avances en Biología en Reproducción Asistida. Consultado el 4 de enero de 2020.
Bibliografía
editar- María Teresa Urbina, Jorge Lerner Biber, Fertilidad y reproducción asistida, Médica Panamericana, 2009, 125-137, ISBN 978-980-6908-16-1
- Hoozemans, Diederik; Roel Schats, Cornelis B Lambalk, Roy Homburg, Peter GA Hompes (octubre de 2004). «Human embryo implantation: current knowledge and clinical implications in assisted reproductive technology». Reproductive BioMedicine Online 9 (6): 692-715. PMID 15670421.
- Guzeloglu-Kayisli, Ozlem; Murat Basar, Aydin Arici (octubre de 2007). «Basic aspects of implantation». Reproductive BioMedicine Online 15 (6): 728-739. PMID 18062873.
- Sharma, Alok; Pratap Kumar (junio-Abril de 2012). «Understanding implantation window, a crucial phenomenon». J Hum Reprod Sci 5 (1): 2-6. PMC 409914. doi:10.4103/0974-1208.97777.
- Amy M Tetrault, B.S, M.S., Susan M Richman, M.D., Xiaolan Fei, M.D., and Hugh S Taylor, M.D. Decreased endometrial HOXA10 expression associated with use of the copper intrauterine-device. Fertil Steril. 2009 Dec;92(6):1820-4.