Benzamida
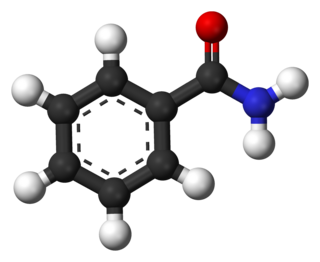
La benzamida es un compuesto orgánico sólido, de color blanco y ligeramente soluble en agua. Su fórmula molecular es C7H7NO.
| Benzamida | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Benzamida | ||
| General | ||
| Otros nombres | Fenil carboxamida, Benzoilamida | |
| Fórmula estructural | C6H5-CONH2 | |
| Fórmula molecular | C7H7NO | |
| Identificadores | ||
| Número CAS | 55-21-0[1] | |
| ChEBI | 28179 | |
| ChEMBL | CHEMBL267373 | |
| ChemSpider | 2241 | |
| PubChem | 2331 | |
| UNII | 6X80438640 | |
| KEGG | C09815 | |
| Propiedades físicas | ||
| Densidad | 1341 kg/m³; 1,341 g/cm³ | |
| Masa molar | 121,14 g/mol | |
| Propiedades químicas | ||
| Acidez | 23.35 (en DMSO) pKa | |
| Solubilidad en agua | 13 g/l | |
| Peligrosidad | ||
| NFPA 704 |
1
1
0
| |
| Frases R | R22 R40 | |
| Frases S | S36 S37 S39 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Síntesis
editarA partir de cloruro de benzoílo
editarLa benzamida usualmente es sintetizada por la reacción del cloruro de benzoílo con el amoníaco.[2]
Reacciones
editar1) Hidrólisis en medio ácido
editarLa benzamida en medio acuoso ácido hidroliza a ácido benzoico.[2]
2) Hidrólisis en medio básico
editarEn medio acuoso básico, alcalinizado con una base fuerte como el NaOH, hidroliza a benzoato de sodio.[2]
3) Deshidratación
editarEn presencia de pentóxido de difosforo a altas temperaturas la benzamida se deshidrata a benzonitrilo.
4) Reducción
editarLa reducción de benzamida con hidruro de litio e hidruro de aluminio produce bencilamina.[2]
5) Transposición de Hofmann
editarLa benzamida en presencia de bromo en medio alcalino produce anilina y dióxido de carbono.
Fármacos derivados
editarVarios fármacos son compuestos derivados de la benzamida, algunos de ellos son:
- Analgésicos
- Antieméticos/Prokinéticos
- Alizaprida
- Bromoprida
- Cinitaprida
- Cisaprida
- Cleboprida
- Dazoprida
- Domperidona
- Itoprida
- Metoclopramida
- Mosaprida
- Prucaloprida
- Renzaprida
- Trimetobenzamida
- Zacoprida
- Antipsicóticos
- Otros
Referencias
editar- ↑ Número CAS
- ↑ a b c d McMurry, John (2004). «Derivados de ácidos carboxílicos y reacciones de sustitución nucleofílica en el acilo». Química Orgánica (sexta edición). Thompson. pp. 795-797. ISBN 970-686-354-0.
Enlaces externos
editar- Benzamida. Información física y química (en inglés).
- Safety (MSDS) data for benzamide. Archivado el 11 de febrero de 2011 en Wayback Machine.
- Wikimedia Commons alberga una categoría multimedia sobre Benzamida.
