Cebuella pygmaea
Cebuella pygmaea es una especie de primate platirrino de la familia Callitrichidae.[2] Es conocido como tití pigmeo, chichico, tití de bolsillo o de piel roja, tití león o leoncito. Se caracteriza por su diminuto tamaño y es la especie de platirrino más pequeña.
| Tití pigmeo | ||
|---|---|---|
 | ||
| Estado de conservación | ||
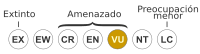 Vulnerable (UICN 3.1)[1] | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Chordata | |
| Clase: | Mammalia | |
| Orden: | Primates | |
| Familia: | Callitrichidae | |
| Género: | Cebuella | |
| Especie: |
C. pygmaea (Spix 1823) Elliot 1913 | |
| Distribución | ||
 | ||
| Sinonimia | ||
| ||
Taxonomía y filogenía
editarEl género Cebuella fue propuesto inicialmente como subgénero de Callithrix por su estrecha relación; sin embargo, posteriormente se consideró como un género distinto, Cebuella, para ser incluido finalmente por análisis morfológicos y genéticos se clasificó finalmente bajo el género Callithrix. Es genéticamente cercano a Callithrix argentata difiriendo de Callithrix jacchus por dos características cromosomales.[3]
Existen dentro de Cebuella pygmaea dos subespecies,[2] basándose en observaciones de campo en el interfluvio de los ríos Purús y Maderia, y especímenes en cautiverio. Se reconoció Cebuella pygmaea niveiventris de pelaje blanquecino en el pecho, abdomen y cara interna de las extremidades ubicado en la orilla sur del Río Solimões; y Cebuella pygmaea pygmaea donde la superficie ventral es ocre. Sin embargo, según otros autores como Hershkovitz[4] exponen argumentos que invalidan el estatus subespecífico dentro de la especie debido a que el color de las extremidades es variable individual y localmente.
En 2009, Cebuella, antes considerado subgénero de Callithrix, se elevó al rango de género, incluyendo como única especie a Cebuella pygmaea.[2]
Distribución y hábitat
editarC. pygmaea prefiere los bosques secundarios cercanos a los cursos de agua. Habita las tierras bajas tropicales de los bosques de la Amazonía occidental. Su distribución y densidad se correlacionan directamente con la presencia y abundancia de especies de árboles y animales que forman parte de su dieta.
Habitan selvas lluviosas de mucha precipitación o bosques maduros compuestos por cañas, hierbas altas, enredaderas, arbustos y árboles jóvenes hasta los 30 o 40 m en los bordes de ríos en llanuras aluviales inundables periódicamente y por más de tres meses, utilizan los estratos verticales desde el suelo hasta los 20 m. Los datos sobre la precipitación y la temperatura se han establecido sobre un sitio de estudio en el Perú en la cuenca del río Maniti donde la temporada de lluvias dura de octubre a mayo y la estación seca se extiende de junio a septiembre. La temperatura se mantiene constante a 27 °C y con un 80 % de humedad.[5][6] Los ríos comienzan a aumentar en el comienzo de la temporada seca, de tal manera que entre febrero y junio la llanura se inunda.
Los rangos de hogar suelen incluir casi 20 a 60 m tierra adentro y varían en tamaño con una media de media hectárea. Dentro de ella, el tamaño poblacional se ve influido por la densidad de depredadores y competidores, especialmente las hormigas arbóreas que invaden los agujeros hechos por este tití para alimentarse con exudados. Además, pueden competir con otros primates de las especies Saguinus fuscicollis, Saguinus mystax, Callicebus moloch, Saimiri sciureus y especies de Aotus.[7]
Habita en América del Sur y se distribuye en la cuenca occidental del Amazonas, al sur del Río Caquetá (Japurá) de Colombia, al oeste en la Amazonía de Ecuador, al sur a través de las tierras bajas del oriente del Perú a la orilla derecha del Río Ucayali, al norte de Bolivia, con una extensión sobre el norte del Río Purús y el río Solimões de Brasil.[8][7][9][4]
Se reconocen dos subespecies separadas por barreras geográficas como los grandes ríos. Cebuella pygmaea pygmaea es encontrado en el Amazonas, Brasil (al norte del Río Solimões), al este de Perú (al norte del Río Marañón), al sur de Colombia, al norte de Bolivia y noreste de Ecuador. Cebuella pygmaea niveiventris se encuentra en el Amazonas, el Brasil, al este de Perú y al sur y norte de Bolivia.
Anatomía y fisiología
editarEs la especie de platirrino más pequeña,[10][11] con una talla de 14 a 18 centímetros, con una cola larga no prensil rodeada parcial o completamente de anillos oscuros sobre un fondo claro, que supera la longitud corporal llegando a 15 o 20 centímetros. Los machos y hembras tienen proporciones similares con un peso promedio de 119 g y una longitud promedio de 136 mm.[12] El pene del adulto no es pigmentado, es liso y cuenta con un báculo de 2,7 mm de longitud y 0,7 de ancho. El escroto es globoso con testículos no pigmentados. Los labios menores femeninos son glandulares, peludos y a veces pigmentados, el clítoris se oculta entre la vulva. Las zonas perineal y anal puede ser pigmentada.[4]
Su pelaje, fino, suave y denso, varía de gris a castaño con algunos tonos amarillos y negros con la parte inferior normalmente naranja variando de rojo a blanco. El pelo largo forma una melena que rodea la cara y la nuca casi en su totalidad, ocultando las orejas. Tienen las más especializadas y numerosas vibrisas sensoriales de los primates, incluyendo conjuntos cubital, carpiano, antebranquial, anconeal, mistacial, mental, interramal, gular y pectoral.[4] Sus patas traseras son generalmente más largas que las delanteras para su desplazamiento sobre los troncos de árboles. Con garras (tégulas) en todos los dígitos a excepción del dedo gordo del pie en el que tienen una uña plana (ungulae). A diferencia de la mayoría de primates, posee dos molares en lugar de tres; para una fórmula dental de incisivos 2/2, caninos 1/1, premolares 3/3 y molares 2/2 para un total de 32 dientes.[4][13][14][15] Su cráneo es convexo hacia la parte frontal y el perfil nasal ligeramente cóncavo, las crestas temporales débilmente definidos y con el borde inferior de la mandíbula en forma de V. El volumen de la caja craneal de 19 individuos fue de 34,8 cm³. El sistema esquelético posterior tiene 7 vértebras cervicales, 13 torácicas, 6–7 lumbares, 3 sacras y 28–29 coxales para un total de 57–59.[4]
Dieta
editarSon omnívoros, alimentándose desde savia de ciertas especies de plantas en los bosques de galería a orillas de ríos y lagunas,[10][16] hasta frutos e insectos emitiendo sonidos cada vez que hallan una fuente de alimento. Abren agujeros característicos en los árboles, absorbiendo la savia, goma y látex y regresando días después a nutrirse del mismo orificio. Los agujeros son de 10 a 20 mm de ancho y de 4 a 18 de profundidad, siendo hechos primero hacia la base del árbol.[17]
Cuentan además con un ciego en su sistema digestivo que permite aumentar el tiempo de exposición de los fluidos vegetales a los ácidos gástricos. Los caninos inferiores son similares en largo a los incisivos inferiores y los caninos superiores son conspicuos similares a los incisivos adyacentes,[4] condición descrita como procumbente,[18] o semiprocumbente[19] posiblemente como una adaptación a la alimentación de exudados.[20] Los incisivos inferiores de C. pygmaea son estrechos y alargados de forma que los cinco dientes en la parte delantera y el centro de la mandíbula inferior son todos la misma longitud, permitiendo roer los árboles y estimular el flujo de savia.
Se alimentan de especies vegetales tales como Quararibea rhombifolia (Bombacaceae), Ficus (Moraceae), Pourouma, Vochysia lomatophylla (Vochysiaceae), Trichilia (Meliaceae), Cheiloclinium cognatum (Hippocrataceae) y Spondias mombin (Anacardiaceae).[17][7] Consumen saltamontes (Orthoptera), abejas silvestres (Hymenoptera), polillas (Lepidoptera), mariposas diurnas (Lepidoptera), libélulas (Odonata) y lagartijas (Anolis, Cnemidophorus lemniscatus, Gonatodes albogularis).[21]
Organización social y comportamiento
editarViven en grupo pequeños, de 3 a 8 individuos, con un promedio de 5, presumiblemente familias lideradas por una pareja de adultos, de 0 a 3 subadultos, 0 a 2 juveniles y de 0 a 2 infantes,[22] abarcando el dosel arbóreo que marcan y defienden con glándulas odoríferas del pecho y el área suprapúbica pigmentada o no enmarcada por pelaje negro, y con llamados constantes que incluyen sonidos muy agudos especialmente cuando muestran hostilidad. Las especies de árboles de los que se alimentan varían de grupo a grupo independientemente de la disponibilidad y abundancia dentro de cada una de las localidades.[22]
Ante un posible depredador exhiben mobbing, en el que todo el grupo se reúne y atacan al intruso hasta que se retira, o se quedan inmóviles hasta que la amenaza ha pasado.[7]
Los sitios electos para dormir son nudos densos o raramente huecos en árboles. Son normalmente diurnos, empezando actividad un poco después de amanecer. Normalmente, se empieza el día con la alimentación (que cuenta con dos picos durante el día, de 6 a 9 y otro de 15 a 18 horas)[23] para dar paso a actividades sociales como el acicalamiento, el aseo y el juego. Son bastante ágiles en el movimiento entre los árboles pese a su tamaño, especialmente en las mañanas y atardeceres. Se mueven cuadrúpedamente a lo largo de las ramas, saltando hasta cinco metros en las más delgadas. Son de carácter dócil y amable, acicalándose y comunicándose mutuamente con expresiones faciales gracias a la percepción de dos manchas ubicadas a los costados de la boca y una línea blanca vertical hacia las crestas nasales[12] que junto al movimiento amplio de la cabeza, la postura y las vocalizaciones confirman sus relaciones sociales. Este movimiento les permite explorar el ambiente en busca de depredadores mientras se aferran verticalmente a los troncos.
Algunos autores creen que existe monogamia en estos grupos, sin embargo, lo observado hasta ahora indica que son grupos poliándricos.[15] La mayoría nacen en dos picos cada año, entre noviembre y enero, y entre mayo y junio. La gestación dura entre dos y tres meses (130 a 150 días) tras los cuales paren en promedio dos crías no idénticas transportadas por los miembros del grupo, siendo entonces, todos los adultos partícipes de la crianza y cuidado. El pelaje de los recién nacidos es distinto al de los adultos, con un color amarillo limón que se perderá tras el primer mes. La madre los amamanta hasta, en promedio, los tres meses de edad, alcanzando la madurez reproductiva en hembras y machos cerca del año o año y medio y viviendo hasta 11 años en estado silvestre.
Ontogenia y reproducción
editarLa reproducción en estado silvestre se ha observado aproximadamente cada 6 meses. La gestación en cautiverio dura entre 19 y 20 semanas. La edad mínima del primer parto en cautividad es de 32 meses con una frecuencia de casi el 67 al 76 % de los nacimientos corresponden a gemelos.[7][24]
El recién nacido cuenta con pelaje, a excepción de su vientre, y sus ojos están abiertos al nacer. El desarrollo de los jóvenes se han clasificado en los siguientes grupos de edad:[7] infante 1 (menor de 1 mes) de pequeño tamaño con dientes de leche y llevado por adultos o juveniles; infantil 2 (de 2 a 5 meses) pequeños con locomoción independiente, comienzan a nacer los dientes permanentes; menores (de 6 a 12 meses), de menor tamaño que un adulto y con genitales pequeños, el círculo negro anogenital comienza a aparecer, para finales del noveno mes todos los dientes permanentes han hecho erupción; subadultos (de 12 a 16 meses), siguen siendo ligeramente más pequeños que un adulto con una pigmentación escrotal incipiente y caninos pequeños; a partir de los 16 meses madura sexualmente y los caninos alcanzan la longitud normal.
La erupción dental y la secuencia de desarrollo es similar a otros calitrícidos (mandíbula 5 m1-i1-m2-i2-p3-p2-p1-c1; maxilar 5 M1-I1-M2-(P3–P2)-(P1–I2)-C1), a excepción del hecho que el segundo incisivo entra en erupción después de que el segundo molar.[25][26] Este retraso en la erupción y el desarrollo de los incisivos es único entre los primates existentes y puede ser correlacionado con la morfología de la corona de los caniniformes. .[27]
Características genotípicas
editarCebuella pygmaea tienen 44 cromosomas diploides. El cromosoma Y es acrocéntrico mientras que el X es metacéntrico.[28][29] El resto de cromosomas (32), los autosomas, son categorizados en 4 grupos basados en el radio y tamaño de los brazos. Se observa que la mayoría son submetacéntricos y 10 son acrocéntricos. La diferencia en el número de cromosomas con su ancestro puede ser causa de la separación ocurrida antes de la diferenciación de Callitrichidae.[30]
A través de la fusión de dos pares de cromosomas acrocéntricos pequeños de Callithrix jacchus, el cariotipo de C. pygmaea pudo haber surgido.[31] Con Callithrix argenata comparte el número de cromosomas (2n=44), mientras que Callithrix jacchus'' tiene el mismo número diploide (2n=46) como los géneros Saguinus y Leontopithecus.[32]
La transferencia de células germinales entre los mellizos es posible gracias a la interconexión de sus placentas vía vasos sanguíneos.[33] Por la ocurrencia de dichos partos múltiples en esta especie se observan quimeras XX/XY por anastomosis placentaria con importantes efectos sobre la fertilidad.[34]
Estado de conservación y amenazas
editarEl papel de los primates es importante para mantener la estructura y dinámica de los ecosistemas tropicales debido a que distintas especies cumplen roles ecológicos diversos e importantes tales como la de polinización, dispersión de semillas y como eslabón importante en la cadena trófica.[10]
Considerando su área de distribución y los problemas como la desaparición de bosques por la ganadería y la agricultura junto con el tráfico ilegal como mascotas hacen que las poblaciones silvestres de esta especie se vean seriamente afectadas, disminuyendo rápidamente,[35] futuro no prometedor a menos de que sean iniciados programas de conservación de los individuos en estado silvestre y de eliminación de las vías de tráfico animal en la selva Amazónica.
Vulnerabilidad y categoría de amenaza
editarLa preferencia por determinadas sustancias para su alimentación es de gran importancia ecológica en la repartición de recursos interespecíficos debido a que prefieren alimentos que otros primates evitan.[36] Esta especialización en la dieta, junto con otras características como el hábitat, hacen que este primate sea particularmente vulnerable a las actividades humanas, estando ausente en ambientes alterados o en baja densidad poblacional y con cambios comportamentales en áreas con presencia humana como lo son las turísticas; sin embargo, debido a su capacidad de adaptación a bosques secundarios, actualmente se clasifica, según la condición jurídica y social, como una especie bajo preocupación menor (LC) en la Lista Roja de la UICN de 2008.[1]
Tratados para su conservación
editarEsta especie está incluida en el Apéndice II de la Convención sobre el Comercio Internacional de Especies Amenazadas (CITES), lo que significa que el comercio internacional de esta especie debe ser monitorizada cuidadosamente.
Para reducir la degradación del hábitat y las perturbaciones humanas, ha habido algunos esfuerzos para crear conciencia en las comunidades locales. Por ejemplo, un programa en Ecuador se inició para educar a los niños en la importancia de la conservación de los primates.[37]
Depredadores y parásitos
editarLos depredadores de C. pygmaea incluyen los capuchinos (Cebus apella), el ocelote (Leopardus pardalis), el tigrillo (Leopardus tigrinus y Leopardus wiedii), el yaguarundí (Herpailurus yaguarondi), algunas aves de presa (que despiertan llamados de atención cuando vuelan sobre el grupo) y grandes serpientes como Bothrops atrox o constrictoras como Boa constrictor o jóvenes de Eunectes murinus.
Adicionalmente con estos animales se relacionan algunos parásitos, entre ellos nemátodos como Strongyloides stercoralis, Pithecostrongylus alatus, Filaroides cebuellae, Enterobius vermicularis, Primatubulura jacchis y Protospirula sp.; y acantocéfalos como Prosthenorchis elegans y Prosthenorchis spirula.[38]
Tráfico ilegal
editarPor su diminuto tamaño y bajos niveles de agresividad estos titíes son capturados como mascotas. Los métodos varían pero el más popular es inmovilizar al animal al tronco del que se alimenta con productos químicos. Esta captura afecta dramáticamente el tamaño del grupo y el comportamiento pues se disminuyen los tiempos de juego e interacciones sociales, evitan usar los estratos bajos del bosque y tienen efectos negativos sobre la tasa de reproducción llevando a la desaparición de los grupos en un área.
Destrucción de su hábitat
editarAdemás de su sensibilidad al aumento en el ruido ambiental y el tráfico humano, otro problema que afecta las poblaciones de esta especie es la destrucción de los bosques de galería en donde los grupos migran o desaparecen debido al agotamiento de las fuentes viejas de exudados y a la ausencia de nuevas fuentes. Por ello, es de importancia proteger las especies de plantas proveedoras de exudados para asegurar la supervivencia de estos primates y de muchas otras especies de animales que también usan esta fuente de alimento.
Referencias
editar- ↑ a b Rylands, A.B. & de la Torre, S. (2008). «Cebuella pygmaea». Lista Roja de especies amenazadas de la UICN 2020.2 (en inglés). ISSN 2307-8235. Consultado el 8 de diciembre de 2020.
- ↑ a b c Anthony B. Rylands; Russell A. Mittermeier (2009). «The Diversity of the New World Primates (Platyrrhini): An Annotated Taxonomy». Developments in Primatology: Progress and Prospects (en inglés) 2: 23-54. doi:10.1007/978-0-387-78705-3_2. Archivado desde el original el 13 de septiembre de 2019. Consultado el 23 de diciembre de 2012.
- ↑ Barroso C.M.L, et al. (1997) Update on the phylogenetic systematics of New World monkeys: further DNA evidence for placing the pygmy marmoset (Cebuella) within the genus Callithrix. International Journal of Primatology 18:651–674.
- ↑ a b c d e f g Hershkovitz, P. (1977) Living New World monkeys (Platyrrhini), with an introduction to primates. University of Chicago Press, Illinois 1:1–1117.
- ↑ Soini, P. (1982) Ecology and population dynamics of the pygmy marmoset, Cebuella pygmaea. Folia Primatologica 39:1–21.
- ↑ Soini, P. (1986). A synecological study of a primate community in the Pacaya Samiria Reserve, Peru. Primate Conservation. (7): 63-71.
- ↑ a b c d e f Soini, P. (1988) The pygmy marmoset, genus Cebuella. Ecology and behavior of Neotropical primates (R. A. Mittermeier, A. B. Rylands, A. Coimbra-Filho y G. A. B. Fonseca, eds.):79-130. World Wildlife Fund, Washington, D.C.
- ↑ Janson, C.H.; Emmons, L.H. (1990) Ecological structure of the nonflying mammal community at Cocha Cashu Biological Station, Manu National Park, Peru. Four Neotropical forests (A. H. Gentry, ed.):314-338. Yale University Press, New Haven, Connecticut.
- ↑ Freese, C.W.; Heltne, P.G.; Castro, N. Whitesides, G. (1982) Patterns and determinants of monkey densities in Peru and Bolivia, with notes on distributions. International Journal of Primatology 3:53–90.
- ↑ a b c De La Torre (2000) Primates of Amazonian Ecuador. Proyecto Petramaz/Simbioe, Quito.
- ↑ Tirira, D. (2004) Nombres de los mamíferos del Ecuador. Ediciones Murciélago Blanco y Museo Ecuatoriano de Ciencias Naturales. Publicación Especial 5. Quito.
- ↑ a b Cawthon K.A. (2005) Primate Factsheets: Pygmy marmoset (Callithrix pygmaea). Primate Info Net, University of Wisconsin, Madison. Consultado el 12 de noviembre de 2010.
- ↑ Mac Donald, D. (1984) Encyclopedia of Mammals. Facts on File Publications, New York.
- ↑ Rathbun, G.B. & Fons, R. (1990) "Grzimek's Encyclopedia of Mammals". Vol. 1. McGraw-Hill Publishing Co., New York.
- ↑ a b Nowak, R.M. (1991) "Walker's Mammals of the World". Fifth Edition. Johns Hopkins University Press, Baltimore.
- ↑ De La Torre, S; Yépez, P.; Snowdon, C. en prensa. Conservation status of pygmy marmosets Callithrix (Cebuella) pygmaea in Amazonian Ecuador. En: The Smallest Anthropoids: the marmoset and callimico radiation. R. Tuttle (ed). Springer Verlag.
- ↑ a b Ramirez, M.; Freese, C.H.; Revilla, J. (1977) Feeding ecology of the pygmy marmoset, Cebuella pygmaea in northeastern Peru. The biology and conservation of the Callitrichidae (D. G. Kleiman, ed.):91-104. Smithsonian Institution Press, Washington, D.C.
- ↑ Moyniham, M. (1976) The New World primates. Princeton University Press, New Jersey.
- ↑ Kinzey, W.G.; Rosemberg, A.L.; Ramirez, M. (1975) Vertical clinging and leaping in a Neotropical anthropoid. Nature 255:327–328.
- ↑ Filho, A.F.; Mittermeier, R.A. (1977) Tree gouging, exudate-eating and the ‘‘short-tusked’’ condition in Callithrix and Cebuella. The biology and conservation of the Callitrichidae (D. Kleiman, ed.):105-115. Smithsonian Institution Press, Washington, D.C.
- ↑ Snowdon, C.T.; Pola, Y.V. (1982) Prey capture by naive pygmy marmosets (Cebuella pygmaea). Laboratory Primate Newsletter 21:4–7.
- ↑ a b De La Torre, Yépez, P.; Snpwdon, C. Payaguaje, A. (2004) Ecología, comportamiento y conservación del leoncillo Callithrix (Cebuella) pygmaea en tierras Secoya. Quito.
- ↑ Yépez, P.; De La Torre, S.; Snowdon, C.T. (2005) Interpopulation differences in exudate feeding of pygmy marmosets in Ecuadorian Amazonia. American Journal of Primatology 66: 145-158.
- ↑ Ziegler, T.E.; Snowdon, C.T.; Bridson, W.E. (1990) Reproductive performance and excretion of urinary estrogens and gonadotropins in the female pygmy marmoset (Cebuella pygmaea). American Journal of Primatology 22:191–203.
- ↑ Byrd, K.E. (1978) Radiographic analysis of dental development and eruption sequences in the pygmy marmoset, Cebuella pygmaea (Spix 1823). American Journal of Physical Anthropology 48:384.
- ↑ Soini, P. De Soini, M. (1990) Desarrollo dentario y la estimación de la edad en Cebuella pygmaea, Saguinus fuscicollis y Saguinus mystax. Primatología en el Perú: investigaciones primatológicas 1973–1985:254-271. Proyecto Peruano de Primatología, Lima.
- ↑ Townsend, W.R. (2001) Callithrix pygmaea. American Society of Mammalogists. Mammalian species 665; 1-6.
- ↑ Benirschke, K.; Brownhill, L.E. (1962) Further observations on marrow chimerism in marmosets. Cytogenetics 1:245–257.
- ↑ Egozcue, J.; Chiarelli, B.; Sarti-Chiarelli, M. (1968) The somatic and meiotic chromosomes of Cebuella pygmaea (Spix, 1823) with special reference to the behavior of the sex chromosome during spermatogenesis. Folia Primatalogica 8:50–57.
- ↑ De Boer Lem (1974) Cytotaxonomy of the Platyrrhini (Primates). Genen en Pnaenen 17:1–115.
- ↑ Wohnus, J.F.; Benirschke, K. (1966) Chromosome analysis of four species of marmosets (Callithrix jacchus, Tamarinus mystax, Tamarinus nigricollis and Cebuella pygmaea). Cytogenetics 5:94–105.
- ↑ Seuanez, H.N.; Foreman, L.; Alvez, G. (1988) Comparative chromosome morphology in three callitrichid genera: Cebuella, Callithrix, and Leontopithecus. Journal of Heredity 79:418–424.
- ↑ Wislocki, G.B. (1939) Observations on twinning in marmosets. American Journal of Anatomy 64:445–483.
- ↑ Bueno, M.L. (2003) Importancia de la caracterización genética de especies silvestres en Zoológicos, Unidades de Rescate de fauna y Centros de acopio. Lyonia 3(1):45-56.
- ↑ Defler, T. (2003) Primates de Colombia. Serie de guías tropicales de campo. Conservación Internacional Colombia. Bogotá D. C.
- ↑ Glaser, D.; Hobi, G. (1985) Taste responses in primates to citric and acetic acid. International Journal of Primatology 6: 395–398.
- ↑ Arkive, Cebuella pygmaea. Archivado el 15 de noviembre de 2010 en Wayback Machine. Consultado el 12 de noviembre de 2010.
- ↑ Hershkovitz, P (1977). Living New World monkeys (Platyrrhini): with an introduction to Primates (en inglés). Living New World monkeys (Platyrrhini): with an introduction to Primates. Consultado el 22 de noviembre de 2010.
Enlaces externos
editar- Video, Pictures and Information on Pygmy Marmosets
- Primate Info Net Callithrix pygmaea Factsheet
- Nacimiento de gemelos albinos tití pigmeo (Inglés) National Geographic. Photo in the News: Albino Pygmy Monkey Twins Born
- Arkive: Images of life on earth
- Callithrix pygmaea (Spix, 1823)
- CITES (June, 2010)
- Primate Info Net. Library and Information Service. National Primate Research Center, University of Wisconsin – Madison