Cloruro de aluminio
El cloruro de aluminio (AlCl3) es un compuesto de aluminio y cloro. El sólido tiene un bajo punto de fusión y de ebullición, y está formado por moléculas que presentan enlace covalente a pesar de que está formado por un metal y un no metal. Su sublimación se produce a los 178° C. El AlCl3 fundido conduce mal la electricidad,[2] a diferencia de muchos haluros iónicos como el cloruro de sodio. Existe en estado sólido como una séxtuple estructura coordinada de rejillas en capas.[3]
| Cloruro de aluminio | ||
|---|---|---|
 | ||
 Dimero Tricloruro de Aluminio | ||
| Nombre IUPAC | ||
| Cloruro de Aluminio | ||
| General | ||
| Otros nombres | Cloruro de Aluminio(III) | |
| Fórmula estructural |
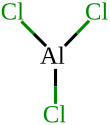 | |
| Fórmula molecular | AlCl3 | |
| Identificadores | ||
| Número CAS | 7446-70-0[1] | |
| Número RTECS | BD0530000 | |
| ChEBI | 30114 | |
| ChemSpider | 22445 | |
| DrugBank | DB11081 | |
| PubChem | 24012 | |
| UNII | LIF1N9568Y | |
|
Cl[Al](Cl)Cl
| ||
| Propiedades físicas | ||
| Apariencia | sólido blanco o amarillo pálido, higroscópico | |
| Densidad | 2,48 kg/m³; 0,00248 g/cm³ | |
| Masa molar | 133,34 g/mol | |
| Punto de fusión | 192,4 °C (466 K) | |
| Punto de ebullición | 120 °C (393 K) | |
| Estructura cristalina | sistema cristalino monoclínico | |
| Riesgos | ||
| LD50 |
anhidro: 380 mg/kg, rat (oral) hexahydrate: 3311 mg/kg, rat (oral) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Carácter ácido-base
editarEste compuesto tiene propiedades ácidas y básicas al mismo tiempo, por lo que es una sustancia anfótera, esto significa que puede actuar como un ácido de Lewis, o una base de Lewis. Por ejemplo, al poner este compuesto en agua destilada, la sal se disociará en sus iones, dando cationes aluminio (Al3+) y aniones cloruro (Cl-). Entonces, el aluminio reaccionará con el agua uniéndose a los oxidrilos y liberando protones, dando como producto hidróxido de aluminio. En cambio, si a la solución preparada anteriormente se le agrega hidróxido de sodio, el ion de aluminio reaccionará con los oxidrilos.
Referencias
editar- ↑ Número CAS
- ↑ N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, Pergamon Press, Oxford, United Kingdom, 1984.
- ↑ (anhidro)
1.3 g/cm³ (hexahidrato) | solubilidad = 43.9 g/100 ml (0 °C)
44.9 g/100 ml (10 °C)
45.8 g/100 ml (20 °C)
46.6 g/100 ml (30 °C)
47.3 g/100 ml (40 °C)
48.1 g/100 ml (60 °C)
48.6 g/100 ml (80 °C)
49 g/100 ml (100 °C)