Condroitín sulfato
El condroitín sulfato o sulfato de condroitina (del griego χόνδρος, «cartílago») es un glucosaminoglucano sulfatado compuesto por una cadena de disacáridos de N-acetilgalactosamina y N-ácido glucurónico alternados. El condroitín sulfato se encuentra habitualmente asociado a proteínas constituyendo agregados de alto peso molecular denominados proteoglicanos. Una cadena de condroitín puede estar constituida por más de 100 azúcares individuales, cada uno de los cuales puede estar sulfatado en posiciones y en número diverso.
Es un importante compuesto de la mayoría de los tejidos de vertebrados e invertebrados y está presente principalmente en aquellos que poseen una gran matriz extracelular, como los que forman los tejidos conectivos del cuerpo, cartílago, piel, vasos sanguíneos, así como los ligamentos y los tendones. El condroitín sulfato aporta al cartílago sus propiedades mecánicas y elásticas, y le proporciona a este tejido mucha de su resistencia a la compresión.
Descripción y propiedades físico-químicas
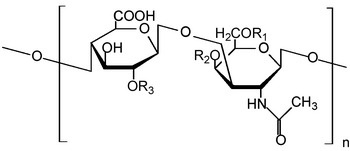
editarLas cadenas de condroitín sulfato son polisacáridos de longitud variable que contienen dos monosacáridos alternados: D-ácido glucorónico (GlcA) y N-acetil-D-galactosamina (GalNac). Cuando algunos residuos de GlcA presentan el epímero de ácido L-idurónico (IdoA), el disacárido resultante se denomina dermatán sulfato.
Adhesión proteica
editarLas cadenas de condroitín sulfato están unidas a los grupos hidroxilo de los residuos de serina de las proteínas. Se desconoce exactamente cómo se seleccionan las proteínas que se van a unir a los glucosaminoglucanos. Empíricamente, las serinas glucosiladas suelen ir seguidas de glicina y tienen residuos acídicos colindantes.
La unión de las cadenas de glucosaminoglicanos empieza con cuatro monosacáridos en un patrón fijo: Xyl - Gal - Gal – GlcA. Cada azúcar se une mediante una enzima específica, permitiendo múltiples niveles de control sobre la síntesis de glucosaminoglicanos. La xilosa empieza a unirse a las proteínas en el retículo endoplasmático, mientras que el resto de los azúcares se unen en el aparato de Golgi.
Sulfatación
editarCada monosacárido puede estar sulfatado una o dos veces. Normalmente los hidroxilos de las posiciones 4 y 6 de la N-acetil-galactosamina están sulfatados. La sulfatación se realiza por sulfotransferasas específicas. El grupo sulfato se fija en la galactosamina en posición 4 y 6, que explica la existencia de dos isómeros del condroitín sulfato. La sulfatación en estas diferentes posiciones confiere las actividades biológicas específicas a las cadenas de condroitín sulfato.
Función
editarLa función del condroitín sulfato en el organismo depende de las propiedades de todo el proteoglicano del cual forma parte. Estas funciones pueden ser de tipo estructural y de tipo regulador. Sin embargo, algunos proteoglicanos poseen ambas funciones (ver versican).
Estructural
editarEl condroitín sulfato es el componente mayoritario de la matriz extracelular de la mayoría de los tejidos vertebrados y representa un elemento importante en el mantenimiento de la integridad estructural de los tejidos con una gran matriz extracelular (tejidos conectivos del cuerpo, cartílago, piel, vasos sanguíneos, así como los ligamentos y los tendones). Esta función es típica de los proteoglicanos de alto peso molecular como el agrecano, versicano, brevicano y neurocano.
Como parte del agrecano, el condroitín sulfato es el componente mayoritario del cartílago. El nivel de agregación y las fuertes cargas de los grupos sulfato del condroitín sulfato le dan la propiedad de retención de agua a estos proteoglicanos, lo que provee al cartílago de su característica de resistencia a la compresión.
En las enfermedades articulares degenerativas, tales como la artrosis, se produce un deterioro y una pérdida del cartílago articular. Una fase clave en el proceso degenerativo artrósico es la pérdida de proteoglicano (formado por condroitín sulfato) del cartílago y la exposición de su red de colágeno a un mal funcionamiento mecánico.
Regulador
editarLa capacidad interactiva de condroitín sulfato con las proteínas de la matriz extracelular se debe a las cargas negativas de la molécula. Estas interacciones son importantes para regular un abanico diverso de actividades celulares. Aunque dichas funciones no están del todo tan bien caracterizadas como las del sulfato de heparina o la heparina, quedan muchos nuevos roles por descubrir para los proteoglicanos del condroitín sulfato. Por ejemplo, cuando existen lesiones en el sistema nervioso central, los niveles de proteoglicanos de condroitín sulfato se ven incrementados, de manera que actúan impidiendo la regeneración de las terminales nerviosas dañadas.
Uso médico de condroitín sulfato
editarEl condroitín sulfato está considerado como Fármaco de Acción Sintomática Lenta para la Artrosis (SYSADOA, Symptomatic Slow Acting Drug for Osteoarthritis) en más de 22 países europeos,[1] mientras que en Estados Unidos es regulado por la FDA (Food and Drug Administration) como suplemento nutricional. Asimismo el condroitín sulfato también se usa en medicina veterinaria para el tratamiento de las patologías articulares de animales como perros, gatos y caballos.
Como fármaco, el condroitín sulfato pertenece al grupo M01AX: Otros antiinflamatorios y antirreumáticos no esteroideos (clasificación ATC -Anatomic Therapeutic Chemical Classification- de la Organización Mundial de la Salud).
El condroitín sulfato se extrae principalmente de cartílago bovino, porcino o marino. El método de la extracción incluye un tratamiento proteolítico seguido de una separación específica y una purificación. El condroitín sulfato usado en la mayoría de estudios se extrae de tráquea bovina (95% de pureza), siendo el mismo que el utilizado en los ensayos clínicos, y por lo tanto, del que se conoce mejor su eficacia y seguridad a nivel clínico.
Dependiendo del origen de la especie animal de la que se extrae el condroitín sulfato (origen terrestre o marino), el condroitín sulfato muestra diferentes proporciones de sulfato en posición 4 o sulfato en posición 6 así como diferentes medias de masa molecular.
Advertencias y precauciones
editarNo se dispone de experiencia en insuficiencias renales y hepáticas, por lo que se recomienda precacución. Se vio algún caso de edema y/o retención de agua en insuficiencia cardiaca y renal. [2]
No se han realizado estudios de interacciones. En caso de utilización concomitante con antiagregantes plaquetarios (AAS, dipiridamol, clopidogrel, ditazol, triflusal y ticlopidina), precaución, ya que en ratas y a dosis muy superiores a las recomendadas, 50 mg/kg/día (lo que equivaldría a 4.000 mg en humanos/día), se ha observado que puede existir una ligera actividad antiagregante plaquetaria de condroitin sulfato. [2]
No existen datos suficientes sobre la utilización de condroítin sulfato en mujeres embarazadas. Los estudios en animales son insuficientes para determinar las reacciones en el embarazo y/o desarrollo embrional, fetal o posnatal. Por tanto, no debe utilizarse en embarazo. En cuanto a la lactancia, no existe información disponible sobre la excreción a través de la leche.[2]
No recomendado en niños y adolescentes menores de 18 años. [2]
Farmacología
editarBiodisponibilidad y propiedades farmacocinéticas
editarVarios estudios farmacocinéticos llevados a cabo en humanos y en animales señalan que el condroitín sulfato se puede absorber oralmente y que la biodisponibilidad de condroitín sulfato oscila entre un 15 y un 24% de la dosis administrada por vía oral. De la fracción absorbida de condroitín sulfato, el 10% se halla en forma de condroitín sulfato y el 90% en forma de derivados despolimerizados de menor peso molecular. Tras la administración oral de condroitín sulfato, la concentración máxima de condroitín sulfato en sangre se alcanza en unas 4 horas.
En sangre, el 85% de la concentración de condroitín sulfato y de los derivados despolimerizados se halla fijada a diversas proteínas plasmáticas. El volumen de distribución de condroitín sulfato es relativamente pequeño, alrededor de 0,3 l/kg.
Al menos el 90% de la dosis de condroitín sulfato es metabolizado. El hígado, los riñones y otros órganos participan en la despolimerización de condroitín sulfato. Condroitín sulfato no es metabolizado por enzimas del citocromo P450, ello es de gran trascendencia ya que implica que condroitín sulfato no puede presentar interacciones con otros medicamentos a nivel metabólico.
El tiempo de vida media oscila entre 5 y 15 horas. La vía de eliminación de condroitín sulfato y de los derivados despolimerizados más importante es el riñón.
La cinética de condroitín sulfato es de primer orden hasta dosis de 3000 mg, lo que implica que no se acumula en el organismo hasta esta dosis.
Toxicidad y seguridad
editarEl condroitín sulfato es una sustancia natural endógena presente en la matriz extracelular de muchos tejidos del cuerpo, entre ellos el cartílago. Los estudios de toxicidad (aguda, subaguda y crónica), mutagenicidad (potencial de provocar mutaciones), carcinogénesis (producción de cáncer) y de toxicidad sobre la reproducción, efectuados con condroitín sulfato, han dado en todos los casos resultados negativos. Se documentan reacciones adversas raras relativas a náuseas y/o alteraciones gastrointestinales.
El condroitín sulfato ha sido ampliamente usado como tratamiento sintomático para la artrosis en Europa durante más de 20 años: en Suiza (desde 1983), en Italia (1990), en Francia (desde 1993), en Italia y Austria (desde 1994), en Suiza (desde 1996) y en Portugal (desde 2000), así como en varios países de la Europa del Este. En España este producto lleva comercializado desde 2003. Durante estos años, los estudios de farmacovigilancia jamás han revelado ningún efecto tóxico importante resultante de la utilización de este compuesto. Por otro lado, tampoco se ha detectado ningún efecto grave derivado del uso de condroitín sulfato tanto a corto como a largo plazo en Estados Unidos, donde lleva mucho tiempo comercializado como complemento nutricional.
La ausencia de problemas graves derivados del uso de este producto es una de las razones por las se comercializa, a pesar de no haber demostrado resultados.
Mecanismos de acción
editarLa acción terapéutica del condroitín sulfato en pacientes artrósicos es debida a su efecto beneficioso sobre el desequilibrio metabólico ocurrido en el cartílago artrósico. Los mecanismos de acción del condroitín sulfato están descritos para los tres niveles de la articulación: cartílago, membrana sinovial y hueso subcondral. A nivel del cartílago, este fármaco actúa favoreciendo la síntesis de proteoglicanos, ácido hialurónico y colágeno II; y por otro lado disminuyendo la actividad catabólica de los condrocitos inhibiendo algunas enzimas proteolíticas (MMP-3, MMP-9, MMP-13, MMP-14, colagenasa, elastasa, fosfolipasa A2, NAG, catepsina B, agrecanasa 1), la formación de otras sustancias que dañan el cartílago (óxido nítrico y radicales libres) y reduciendo la apoptosis. Además está descrita una actividad antiinflamatoria a nivel de los componentes celulares de la inflamación (TNF-α, IL-1β, COX-2, PGE2, NF-ĸB[3]). A nivel de la membrana sinovial, el condroitín sulfato actúa estimulando la síntesis de ácido hialurónico, y reduciendo la inflamación y el derrame articular. A nivel del hueso subcondral, se ha descrito en un trabajo reciente que el condroitín sulfato ejerce un efecto positivo sobre el desequilibrio óseo ocurrido en el hueso subcondral artrósico.[4]
Se ha publicado en la revista Annals of the Rheumatic Diseases una revisión que describe todas las evidencias publicadas en relación con los mecanismos de acción del condroitín sulfato.[5]
Efecto clínico
editarLos ensayos clínicos controlados llevados a cabo con condroitín sulfato para evaluar su eficacia en el tratamiento de la artrosis comparado con placebo o con antiinflamatorios, no han demostrado que este producto sea beneficioso para el alivio del dolor y la mejoría de la incapacidad funcional en estos pacientes.
El Comité de evaluación de nuevos medicamentos de Euskadi, en su Informe de Evaluación n.º 189/2012, realizó una revisión sistemática que valora la eficacia del condroitín sulfato, la glucosamina o su combinación frente a placebo. No se encontraron diferencias clínicamente elevantes frente a placebo ni con glucosamina, ni con condroitín sulfato ni con la combinación. Ni el condroitín, ni la glucosamina ni la combinación de ambos demostraron tener ningún efecto sobre el estrechamiento del espacio intraarticular. La asociación a dosis fijas de los fármacos condroitín/glucosamina, los llamados SYSADOAS (SYmptomatic Slow Acting Drugs for OsteoArthritis), no aporta ningún beneficio significativo en el alivio del dolor ni en la progresión de la enfermedad,.[6] Esta evaluación corrobora los resultados de los estudios del 2007 de Reichenbach et al,[7] del 2010 de Wandel et al.,[8] los Servicios de Salud de Baleares[9] y Cataluña,[10][11] llegando hasta la propuesta de la Sociedad Española de Farmacéuticos de Atención Primaria de su desfinanciación por el Sistema Nacional de Salud[12]
Merece la pena comentar con detalle el estudio GAIT (acrónimo del título en inglés “Glucosamine/Chondroitin Arthritis Intervention Trial”)[13] porque se trata de un ensayo clínico multicéntrico, aleatorio y doble ciego, realizado por el National Institute of Health (NIH) de Estados Unidos en 1583 pacientes con artrosis de rodilla publicado en el New England Journal of Medicine (NEJM). Se comparó el efecto de 5 tratamientos: 1) 500 mg de glucosamina 3 veces al día: 2) 400 mg de condroitín sulfato 3 veces al día; 3) 200 mg de celecoxib al día; 4) 500 mg de glucosamina + 400 mg de condroitín sulfato 3 veces al día; 5) placebo, sobre la reducción del dolor durante 6 meses. Los resultados mostraron que la glucosamina (64.0%), el condroitín sulfato (65.4%) o la combinación de ambos (66.6%) no produjeron una reducción significativa del dolor respecto a placebo (60%) en toda la población del estudio.
Un amplio metaanálisis publicado en 2010 en el British Medical Journal, Wandel et al, 2010,[14] muestra que la glucosamina, el sulfato de condroitina, y su combinación no dan lugar a una reducción relevante de dolor en las articulaciones ni a la disminución del espacio articular en comparación con el placebo. En este metaanálisis se evalúa el efecto sintomático y modificador de la enfermedad tanto de condroitín sulfato como de glucosamina y su combinación, concluyendo que ninguno de los productos presenta eficacia clínica en el tratamiento de la artrosis. [7]
Referencias
editar- ↑ Jordan KM, Arden NK. EULAR Recommendations 2003: an evidence based approach to the management of knee osteoarthritis: Report of a Task Force of the Standing Committee for International Clinical Studies Including Therapeutic Trials (ESCISIT). Ann Rheum Dis, 2003; 62:1145–1155.
- ↑ a b c d Vidal Vademecum. «M01AX25 : CONDROITIN SULFATO». Access Medicina MH Medical. Consultado el 15 de diciembre de 2024. «Redactado teniendo en cuenta la información clínica de todos los medicamentos autorizados y comercializados en España clasificados en dicho código ATC.»
- ↑ Jomphe C, Gabriac M, Hale TM, Heroux L, Trudeau LE, Deblois D, Montell E, Verges J, du Souich P. Chondroitin sulfate inhibits the nuclear translocation of NF-κB in IL-1β stimulated chondrocytes. Basic Clin Pharmacol Toxicol, 2008 Jan;102(1):59-65.
- ↑ Kwan Tat S, Pelletier JP, Verges J, Lajeunesse D, Montell E, Fahmi H, Lavigne M, Martel- Pelletier J. Chondroitin and glucosamine sulfate in combination decrease the pro-resorptive properties of human osteoarthritis subchondral bone osteoblasts: a basic science study. Arthritis Res Ther. 2007 Nov 9;9(6):R117.
- ↑ Monfort J, Pelletier J-P, Garcia-Giralt N, Martel-Pelletier J. Biochemical basis of the effect of chondroitin sulfate on osteoarthritis articular tissues. Ann Rheum Dis, 2008 Jun; 67(6):735-40.
- ↑ Aizpurua et al, 2011, Comité de evaluación de nuevos medicamentos de Euskadi, Informe de Evaluación nº 189/2012, Condroitín sulfato/Glucosamina http://www.osakidetza.euskadi.eus/contenidos/informacion/cevime_nuevo_medicamento/es_nme/adjuntos/condroitin%20sulfato_glucosamina_informe.pdf Archivado el 14 de julio de 2015 en Wayback Machine.
- ↑ a b Reichenbach S, Sterchi R, Scherer M, Trelle S, Bürgi E, Bürgi U, Dieppe PA, Jüni P. Meta-analysis: chondroitin for osteoarthritis of the knee or hip. Ann Intern Med 2007;146:580-90. http://www.ncbi.nlm.nih.gov/pubmed/17438317
- ↑ Groves, T. Report from BMJ post publication review meeting. bmj.com 2011. http://www.bmj.com/content/341/bmj.c4675.full/reply#bmj_el_242776.
- ↑ Cecilia Calvo Pita, Servicios Centrales del Servicio de Salud de las Islas Baleares, Fármacos sintomáticos de acción lenta y administración oral para la artrosis: dudosa eficacia en el control sintomático y nula actividad condroprotectora. El Comprimido, Nº 18 - Abril de 2010 http://www.elcomprimido.com/PDF/SYSADOA%20artrosis_CAST.pdf Archivado el 9 de enero de 2016 en Wayback Machine.
- ↑ Fundació Institut Català de Farmacologia. Hospital Vall d'Hebron, Consulta terapèutica 17722, 10/01/2012 http://www.icf.uab.es/es/pdf/consulta/es17722.pdf Archivado el 24 de septiembre de 2015 en Wayback Machine.
- ↑ Joan-Ramon Laportea y Montserrat Bosch, Crisis y política de medicamentos, Aten Primaria. 2012;44(6):306---308 http://www.elsevier.es/es-revista-atencion-primaria-27-articulo-crisis-politica-medicamentos-90140917 Archivado el 15 de julio de 2015 en Wayback Machine.
- ↑ Propuesta de la Sociedad Española de Farmacéuticos de Atención Primaria de los medicamentos a desfinanciar por el Sistema Nacional de Salud, 2012. http://www.sefap.org/media/upload/pdf/propuesta_sefap_a_desfinanciacion_de_medicamentos_editora_2_122_2.pdf
- ↑ Clegg DO, et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis. N Engl J Med 2006 Feb, 23;354(8):795-808.
- ↑ Wandel S, et al. Effects of glucosamine, chondroitin, or placebo in patients with osteoarthritis of hip or knee: network meta-analysis. BMJ 2010; 341:c4675.