Ketorolaco
El ketorolaco es un antiinflamatorio no esteroideo (AINE) que actúa inhibiendo la síntesis de prostaglandinas. Inhibe las enzimas ciclooxigenasas (COX-1 y COX-2), responsables de convertir el ácido araquidónico en prostaglandinas y tromboxano A2. El ketorolaco es un potente analgésico, que es eficaz en el tratamiento de síntomas mediados por prostaglandinas que causan dolor e inflamación, incluyendo los traumatismos.[1][2]
| Ketorolaco | ||
|---|---|---|
 | ||
 | ||
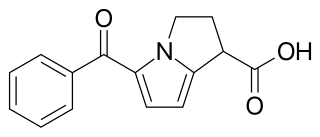
| Nombre (IUPAC) sistemático | ||
| 5-benzoyl-2,3-dihydro-1H-pyrrolizine-1-carboxylic acid | ||
| Identificadores | ||
| Número CAS | 74103-06-3 | |
| Código ATC | M01AB15 | |
| Código ATCvet | QM01AB15 | |
| PubChem | 3826 | |
| DrugBank | DB00465 | |
| ChemSpider | 3694 | |
| UNII | 4EVE5946BQ | |
| KEGG | C07062 | |
| ChEBI | 76223 | |
| ChEMBL | CHEMBL469 | |
| Datos químicos | ||
| Fórmula | C15H13NO3 | |
| Peso mol. | 255.27 g/mol | |
|
C1CN2C(=CC=C2C(=O)C3=CC=CC=C3)C1C(=O)O
| ||
|
InChI=1S/C15H13NO3/c17-14(10-4-2-1-3-5-10)13-7-6-12-11(15(18)19)8-9-16(12)13/h1-7,11H,8-9H2,(H,18,19)
Key: OZWKMVRBQXNZKK-UHFFFAOYSA-N | ||
| Farmacocinética | ||
| Biodisponibilidad | 80 % (vía oral) | |
| Unión proteica | >99 % | |
| Metabolismo | Hepático | |
| Vida media |
2,5 horas (S-enantiómero) 5 horas (R-enantiómero) | |
| Excreción | 92 % por orina, 6 % en heces | |
| Datos clínicos | ||
| Nombre comercial | Lorotec, dolac, entre otros | |
| Uso en lactancia | Moderadamente seguro. Usar solo si el beneficio potencial justifica el riesgo potencial para el bebé. (en todos los países) | |
| Cat. embarazo | C (AU) No hay estudios en humanos. El fármaco solo debe utilizarse cuando los beneficios potenciales justifican los posibles riesgos para el feto. Queda a criterio del médico tratante. (EUA) | |
| Estado legal | S4 (AU) ℞-only (EUA) | |
| Vías de adm. | Oral, IV, IM | |
Historia
editarLa historia de los AINEs se remonta a la antigüedad, cuando la corteza de sauce era utilizada por culturas como los egipcios y sumerios por sus propiedades analgésicas y antipiréticas. Hipócrates, en el siglo V a. C., mencionó su uso para aliviar el dolor y la fiebre. En el siglo XX, el descubrimiento de la inhibición de la ciclooxigenasa llevó al desarrollo de nuevos medicamentos, incluyendo el ketorolaco en la década de 1980. Aprobado por la FDA en 1989, el ketorolaco se convirtió en una herramienta importante para el manejo del dolor agudo, aunque con advertencias por los efectos adversos gastrointestinales, cardiovasculares y renales. Una de las ventajas del ketorolaco es que se puede administrar de forma endovenosa, lo que permite un alivio del dolor más rápido y efectivo en situaciones donde la vía oral no es viable o deseada.[3][4]
Farmacocinética
editarEl ketorolaco puede administrarse por vía oral, nasal, intravenosa o intramuscular. La administración oral debe realizarse solamente posterior al uso de ketorolaco por vía intravenosa o intramuscular, como terapia de continuación del fármaco. La administración del ketorolaco no debe durar más de 5 días, dado un mayor riesgo de eventos trombóticos cardíacos, insuficiencia renal y úlceras pépticas.[5][6]
Absorción
editarEl ketorolaco se administra por vía oral, parenteral, o como solución oftálmica, presentando perfiles farmacocinéticos similares para las dosis parenterales y orales. La absorción es rápida y completa en ambas formas, aunque la intramuscular es más lenta. Tras la administración oral, la concentración plasmática máxima (0.7–1.1 μg/ml) se alcanza en aproximadamente 30 a 44 minutos, mientras que la intramuscular se logra en 45 a 50 minutos.[5][6][7][8]
Los alimentos disminuyen la velocidad de absorción oral, especialmente si son ricos en grasas, retrasando las concentraciones máximas en aproximadamente una hora, pero no afectan la extensión de la absorción. Las formulaciones de ketorolaco en comprimidos con recubrimiento entérico se absorben más lentamente que las formulaciones convencionales, aunque el grado de absorción permanece inalterado.[5][6][7][8]
Distribución
editarEl Ketorolaco se une en más del 99% a las proteínas del plasma y se estima que posee una distribución entre 0,17 L/Kg a 25 L/Kg. Una reducción de la albúmina sérica puede conducir a un aumento de las concentraciones libres del fármaco. La semivida es de 3,5-9,2 horas en adultos jóvenes y 4,7-8,6 horas en los ancianos; en ambos grupos puede aumentarse a más de 10 horas en caso de un paciente con insuficiencia renal.[6][7][8]
La "disponibilidad ocular" de una dosis de 0,25 mg de ketorolaco en el humor acuoso es aproximadamente 13 veces mayor a la alcanzada en plasma por la vía enteral o parenteral.[6][7][8]
El ketorolaco atraviesa la placenta y se distribuye en la leche materna en pequeñas cantidades.[6][7][8]
Metabolismo y metabolitos
editarEl ketorolaco se metaboliza en el hígado principalmente por hidroxilación y conjugación con ácido glucurónico, formando p-hidroxiketorolaco, un metabolito con menos del 1% de la potencia del fármaco original. Las enzimas implicadas en la fase I del metabolismo incluyen CYP2C8 y CYP2C9, mientras que la fase II es llevada a cabo por la UDP-glucuronosiltransferasa (UGT) 2B7. El ketorolaco y sus metabolitos se excretan principalmente en la orina (91%), y el resto se elimina en las heces.[6][7][8][9]
Excreción
editarEl ketorolaco y sus metabolitos se excretan principalmente en la orina (91%), y el resto se elimina en las heces.[6]
Farmacodinámica
editarMecanismo de acción
editarEl ketorolaco, un AINE, ejerce sus efectos analgésicos, antipiréticos y antiinflamatorios mediante la inhibición no selectiva de la enzima ciclooxigenasa (COX). La COX tiene dos isoformas: COX-1 y COX-2, y su inhibición reduce la síntesis de prostaglandinas y eicosanoides, moduladores clave del dolor, fiebre e inflamación.[2][10][11][12][13]
La COX-1 se expresa constitutivamente en la mayoría de los tejidos, desempeñando roles reguladores esenciales como la agregación plaquetaria, la vasodilatación de la arteriola aferente renal y la protección de los ácidos de la mucosa gástrica. La COX-1 posee un papel limitado en la inflamación y la importancia clínica de su inhibición radica en su utilidad en algunas patologías cardiovasculares así como en sus múltiples efectos adversos.[2][10][11][12][13]
La COX-2 es una enzima regulada que se expresa constitutivamente en el cerebro, riñones, huesos y posiblemente en el sistema reproductor femenino, pero es indetectable en otros tejidos. Su expresión aumenta en estados inflamatorios y en respuesta a estímulos mitogénicos como factores de crecimiento e interleucina 1 (IL-1), lo cual aumenta significativamente la producción de prostaglandinas proinflamatorias.[2][10][11][12][13]
Efectos farmacológicos
editarEfecto antipirético
editarDurante un proceso infeccioso, las endotoxinas bacterianas inducen en los macrófagos liberación de IL-1, la cual estimula la generación, en el hipotálamo, de prostaglandinas tipo E, y estas, a su vez, causan la elevación del punto de ajuste para la temperatura. También la IL-1 producida en el endotelio vascular hipotalámico ocasiona inducción de la COX-2. El ketorolaco ejerce su acción antipirética al inhibir la síntesis de prostaglandinas en el hipotálamo.[12]
Efecto analgésico
editarEl ketorolaco es efectivo en el tratamiento del dolor leve a moderado asociado a inflamación o daño tisular, puesto que en los tejidos periféricos, produce una disminución de la síntesis de las prostaglandinas que sensibilizan a los nociceptores frente a mediadores proinflamatorios como la bradicinina. Su capacidad para aliviar la cefalea puede estar relacionada con la disminución del efecto vasodilatador de las prostaglandinas sobre la vasculatura cerebral.[12]
Efecto antiinflamatorio
editarEl ketorolaco reduce la síntesis de prostaglandinas vasodilatadoras, principalmente derivadas de la COX-2, por lo cual, reduce la vasodilatación y por ende el edema de la inflamación (porque la vasodilatación favorece la acción de mediadores como la histamina, que aumentan la permeabilidad de las vénulas poscapilares).[12]
Interacciones
editar| Fármaco | Resultado de la interacción con espironolactona |
|---|---|
| Celecoxib | Sangrado gastrointestinal: El uso de ketorolaco en combinación con otros medicamentos antiinflamatorios no esteroideos (AINE) está contraindicado debido al riesgo aditivo de sangrado y efectos adversos graves relacionados con los AINE |
| Metotrexato | Toxicidad gastrointestinal y hematológica: Ketorolaco no deben administrarse conjuntamente con dosis altas de metotrexato, como los que se usan para el tratamiento del osteosarcoma, debido a la posibilidad de que aumenten los niveles séricos de metotrexato, lo que puede causar toxicidad gastrointestinal y hematológica, que puede ser mortal. |
| Escitalopram | Hemorragia: El aumento de la hemorragia descrito cuando estos agentes se combinan probablemente sea el resultado de una combinación de reducciones mediadas por AINE de las prostaglandinas gastroprotectoras y los efectos antiplaquetarios de los AINE y los ISRS |
| Litio | La combinación de ketorolaco y litio puede hacer que los niveles de litio en la sangre aumentan demasiado. Esto puede ser peligroso. Los niveles altos de litio pueden provocar complicaciones, como confusión y temblores |
| Warfarina | Si se toma solo, el ketorolaco puede aumentar el riesgo de sangrado gastrointestinal. Tomarlo con antitrombóticos hace que este riesgo sea aún mayor, especialmente si recientemente se ha tenido un ataque cardíaco |
| Rivaroxaban | Si se toma solo, el ketorolaco puede aumentar el riesgo de sangrado gastrointestinal. Tomarlo con antitrombóticos hace que este riesgo sea aún mayor, especialmente si recientemente ha tenido un ataque cardíaco |
| Clopidogrel | Si se toma solo, el ketorolaco puede aumentar el riesgo de sangrado gastrointestinal. Tomarlo con antitrombóticos hace que este riesgo sea aún mayor, especialmente si recientemente ha tenido un ataque cardíaco |
Uso clínico
editarInflamación
editarEl ketorolaco es un AINE que actúa inhibiendo la enzima ciclooxigenasa (COX), lo que reduce la síntesis de prostaglandinas responsables de la inflamación. Usualmente se usan dosis únicas de 30 mg de ketorolaco intramuscular seguido de comprimidos orales de 10 a 20 mg.[5]
Dolor agudo
editarEl ketorolaco es eficaz para el manejo del dolor agudo moderado a severo debido a su capacidad para inhibir la COX, lo que reduce la producción de prostaglandinas, mediadores clave del dolor. Usualmente se usan dosis únicas de 30 mg de ketorolaco intramuscular seguido de comprimidos orales de 10 a 20 mg.[5]
Edema macular cistoide
editarEn el tratamiento del edema macular cistoide, el ketorolaco reduce la inflamación intraocular al inhibir la producción de prostaglandinas a través de la inhibición de la COX. Esto ayuda a disminuir el edema y mejorar la visión. Usualmente el tratamiento se hace con solución oftálmica de ketorolaco 0.5%.[5][14]
Efectos adversos
editarPara la evaluación de las reacciones adversas (RAM) se tienen en cuenta los criterios de la CIOSM.
| Grupo CIOSM | Tipo de reacción |
|---|---|
| Muy frecuentes | Úlceras pépticas, gastritis, retención de líquidos |
| Frecuentes | Hemorragia gastrointestinal, hipertensión, erupciones cutáneas, prurito, anemia |
| Poco frecuentes | Nefritis intersticial, insuficiencia renal aguda, insuficiencia cardíaca, leucopenia, trombocitopenia |
| Raros | Hepatitis, perforación gastrointestinal, prolongación del tiempo de sangrado |
| Muy raros | Síndrome Steven Johnson |
Contraindicaciones
editar- Embarazo: el ketorolaco es un medicamento de categoría C para el embarazo. Sin embargo, dado que los medicamentos antiinflamatorios no esteroideos pueden causar una reacción adversa cardiovascular fetal (cierre del conducto arterioso), se debe evitar el uso de ketorolaco durante el embarazo (particularmente en el tercer trimestre). Debe administrarse durante el embarazo sólo si el beneficio potencial supera el riesgo potencial para el feto y no durante el parto, puesto que, el fármaco puede afectar negativamente a la circulación sanguínea fetal y prevenir las contracciones uterinas, lo que aumenta el riesgo de hemorragia uterina.[5]
- Lactancia: No se han reportado eventos adversos sobre el uso de ketorolaco en mujeres lactantes y su efecto en los bebés.[5]
- Pacientes con riesgo de hemorragia: El ketorolaco no debe utilizarse en pacientes con alto riesgo de hemorragia, como aquellos con diátesis hemorrágica, hemorragia cerebrovascular o hemostasia incompleta, debido a su potencial para aumentar significativamente el riesgo de sangrado.[5]
- Pacientes con riesgo gastrointestinal: El ketorolaco aumenta significativamente el riesgo de úlceras pépticas, perforaciones gástricas y hemorragias gastrointestinales debido a sus propiedades antiplaquetarias. Tiene el mayor riesgo relativo (RR 11.5) entre los AINEs, incrementando también el riesgo de hemorragia postoperatoria en comparación con los opioides.[5]
- Pacientes con falla renal: El ketorolaco está asociado con un alto riesgo de daño e insuficiencia renal.[5]
- Pacientes con riesgo cardiovascular: El uso de ketorolaco puede incrementar el riesgo de eventos trombóticos cardiovasculares, infartos de miocardio y accidentes cerebrovasculares hemorrágicos.[5]
Sobredosis
editarEl uso prolongado o en altas dosis de ketorolaco puede llevar a hepatotoxicidad y nefrotoxicidad. Además, el ketorolaco puede ocasionar diversos trastornos cutáneos, como la necrólisis epidérmica tóxica. Las sobredosis de ketorolaco se han asociado con la aparición de shock anafiláctico.[5][15]
El tratamiento para una sobredosis de ketorolaco generalmente incluye cuidados médicos de apoyo y la suspensión del uso del medicamento. No hay un antídoto específico disponible para el ketorolaco y la hemodiálisis no es efectiva debido a su alta unión a las proteínas plasmáticas.[5][15]
Presentaciones
editarLa administración de ketorolaco se puede realizar por vía oral, nasal, IV o IM. La versión oral debe administrarse solo después de ketorolaco por vía intravenosa o IM. Solución inyectable intravenosa de ketorolaco trometamina: 15 mg/ml; 30 mg/m; solución inyectable IM de trometamina de ketorolaco: 60 mg/ml; comprimidos orales: 10 mg
Otros usos
editarUsos no incluidos en el registro sanitario (Off Label)
editarDolor postoperatorio en niños
editarEl ketorolaco trometamol se puede utilizar para el tratamiento a corto plazo del dolor postoperatorio moderado a intenso en niños. En los Estados Unidos, los niños de entre 2 y 16 años pueden recibir una dosis intramuscular única de 1 mg/kg de ketorolaco trometamol hasta un máximo de 30 mg o una dosis intravenosa única de 500 microgramos/kg hasta un máximo de 15 mg.[16]
Artroplastia articular total
editarEl uso de ketorolaco intravenoso disminuye el dolor y reduce el uso de opioides en el período posoperatorio. Se ha demostrado que se puede obtener una analgesia igualmente eficaz con morfina intraarticular.[5][17]
Referencias
editar- ↑ Mallinson, Tom Edward (2 de diciembre de 2017). «A review of ketorolac as a prehospital analgesic». Journal of Paramedic Practice (en inglés) 9 (12): 522-526. ISSN 1759-1376. doi:10.12968/jpar.2017.9.12.522. Consultado el 16 de julio de 2024.
- ↑ a b c d HARDMAN, J.G.; LIMBRID, L.E.; MOLINOFF, P.B.; RUDDON, R.W. y GOODMAN GILMAN, A.: "Las bases farmacológicas de la terapéutica". Editores Goodman & Gilman. Ed. McGraw-Hill Interamericana. 12ª edición. México, 2012
- ↑ Fda.gov. [citado el 3 de julio de 2024]. Disponible en: https://www.accessdata.fda.gov/drugsatfda_docs/nda/99/075284.PDF
- ↑ Oscanoa-Espinoza T. J, Seguridad de los antiinflamatorios no esteroideos. Revista Médica del Instituto Mexicano del Seguro Social [Internet]. 2015;53(2):172-179. Recuperado de: https://www.redalyc.org/articulo.oa?id=457744936012
- ↑ a b c d e f g h i j k l m n ñ Mahmoodi, Ahmad N.; Patel, Preeti; Kim, Peggy Y. (2024). Ketorolac. StatPearls Publishing. Consultado el 16 de julio de 2024.
- ↑ a b c d e f g h «KETOROLAC EN VADEMECUM». www.iqb.es. Consultado el 16 de julio de 2024.
- ↑ a b c d e f Buckley, Micaela M.-T.; Brogden, Rex N. (1990-01). «Ketorolac: A Review of its Pharmacodynamic and Pharmacokinetic Properties, and Therapeutic Potential». Drugs (en inglés) 39 (1): 86-109. ISSN 0012-6667. doi:10.2165/00003495-199039010-00008. Consultado el 16 de julio de 2024.
- ↑ a b c d e f Aemps.es. [citado el 2 de julio de 2024]. Disponible en: https://cima.aemps.es/cima/pdfs/es/ft/70105/FT_70105.pdf
- ↑ Fda.gov. [citado el 2 de julio de 2024]. Disponible en: https://www.accessdata.fda.gov/drugsatfda_docs/label/2013/019645s019lbl.pdf
- ↑ a b c Qureshi, Owais; Dua, Anterpreet (2024). COX Inhibitors. StatPearls Publishing. Consultado el 16 de julio de 2024.
- ↑ a b c Osafo, Newman; Agyare, Christian; Obiri, David Darko; Antwi, Aaron Opoku (23 de agosto de 2017). Al-kaf, Ali Gamal Ahmed, ed. Mechanism of Action of Nonsteroidal Anti-Inflammatory Drugs (en inglés). InTech. ISBN 978-953-51-3443-5. doi:10.5772/68090. Consultado el 16 de julio de 2024.
- ↑ a b c d e f Ritter JM, Flower RJ, Henderson G, Loke YK, MacEwan D, Rang HP. Rang Y Dale. Farmacología. 9a ed. Elsevier; 2020
- ↑ a b c Daniel H Solomon, MD, MPH. AINE (incluida la aspirina): farmacología y mecanismo de acción.Recuperado el 2 de Julio de 2024, de https://www-uptodate-com.bd.univalle.edu.co/contents/nsaids-including-aspirin-pharmacology-and-mechanism-of-action?search=AINE%20%28incluida%20la%20aspirina%29%3A%20farmacolog%C3%ADa%20y%20mecanismo%20de%20acci%C3%B3n&source=search_result&selectedTitle=1%7E150&usage_type=default&display_rank=1#H5
- ↑ Weisz, James M; Bressler, Neil M; Bressler, Susan B; Schachat, Andrew P (1999-09). «Ketorolac treatment of pseudophakic cystoid macular edema identified more than 24 months after cataract extraction». Ophthalmology (en inglés) 106 (9): 1656-1659. doi:10.1016/S0161-6420(99)90366-4. Consultado el 16 de julio de 2024.
- ↑ a b Reinhart, Douglas J. (2000). «Minimising the Adverse Effects of Ketorolac:». Drug Safety (en inglés) 22 (6): 487-497. ISSN 0114-5916. doi:10.2165/00002018-200022060-00007. Consultado el 16 de julio de 2024.
- ↑ Mucklow, J. C. (2000-06). «Martindale: The Complete Drug Reference». British Journal of Clinical Pharmacology (en inglés) 49 (6): 613-613. ISSN 0306-5251. PMC 2015035. doi:10.1046/j.1365-2125.2000.00206.x. Consultado el 16 de julio de 2024.
- ↑ Reuben, Dr. Scott S.; Connelly, Dr. Neil R.. Uso no autorizado de ketorolaco. Anestesia y Analgesia 83(1):p 197, julio de 1996