Metilmalonil-CoA
El metilmalonil-CoA es el tioéster de la coenzima A del ácido metilmalónico. Es un intermedio importante en la biosíntesis de muchos compuestos orgánicos, así como en el proceso de asimilación de carbono.[2]
| Metilmalonil-CoA | ||
|---|---|---|
 | ||
| General | ||
| Otros nombres | Metilmalonil coenzima A | |
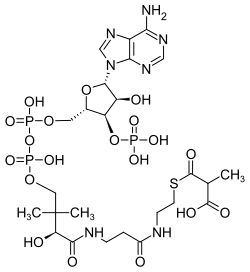
| Fórmula estructural |
 | |
| Fórmula molecular | C25H40N7O19P3S | |
| Identificadores | ||
| Número CAS | 317-66-81264-45-5[1] | |
| ChEBI | 16625 | |
| ChemSpider | 110440 | |
| PubChem | 123909 | |
| KEGG | C02557 | |
|
InChI=InChI=1S/C25H40N7O19P3S/c1-12(23(37)38)24(39)55-7-6-27-14(33)4-5-28-21(36)18(35)25(2,3)9-48-54(45,46)51-53(43,44)47-8-13-17(50-52(40,41)42)16(34)22(49-13)32-11-31-15-19(26)29-10-30-20(15)32/h10-13,16-18,22,34-35H,4-9H2,1-3H3,(H,27,33)(H,28,36)(H,37,38)(H,43,44)(H,45,46)(H2,26,29,30)(H2,40,41,42)/t12?,13-,16-,17-,18+,22-/m1/s1
Key: MZFOKIKEPGUZEN-FBMOWMAESA-N | ||
| Propiedades físicas | ||
| Masa molar | 8676 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El metilmalonil-CoA se produce como un intermediario en la degradación de los ácidos grasos con un número impar de átomos de carbono[3] y algunos aminoácidos (tales como isoleucina, valina, metionina y treonina).[4] El producto formado durante la degradación de metilmalonil-CoA es el succinil-coA producido en el metabolismo y en el ciclo del ácido cítrico, y la reacción con guanosín difosfato (GDP) y fosfato libre es catalizada por la succinil-CoA sintetasa, y suministra el análogo al ATP, el guanosin trifosfato (GTP).
Biosíntesis
editarLos dos enantiómeros, L y D (o R y S), del metilmalonil-CoA intervienen en la degradación de los lípidos a través de la secuencia de reacciones siguiente :
- El D-metilmalonil-CoA deriva del propionil-CoA (que a su vez deriva de la beta-oxidación de los ácidos grasos de número impar de átomos de carbono) por la acción de la propionil-CoA carboxilasa, que requiere de biotina (vitamina B7 o B8) como coenzima.[3]
- El D-metilmalonil-CoA se isomeriza a L-metilmalonil-CoA mediante la acción de la enzima metilmalonil-CoA epimerasa.
- La L-metilmalonil-CoA se convierte en succinil-coA a través de la acción de la metilmalonil-CoA mutasa con adenosilcobalamina (vitamina B12) como coenzima, lo que le permite entrar en el ciclo de Krebs.
El siguiente diagrama muestra las reacciones antes mencionadas:
- Propionil-CoA → Metilmalonil CoA → Succinil-coA
También está implicado en la degradación de ciertos aminoácidos tales como isoleucina, metionina, treonina y valina.
Isómeros
editarEstructura del L-metilmalonil-CoA (a la izquierda) y del D-metilmalonil-CoA (a la derecha). Si usamos las reglas de Cahn-Ingold-Prelog (CIP), tenemos que el enantiómero L se llamaría R, y el D sería el S.
Enfermedades relacionadas
editarEn la enfermedad metabólica aciduria malónica y metilmalónica combinada (CMAMMA) debida a la deficiencia de ACSF3, se reduce la metilmalonil-CoA sintetasa, que convierte el ácido metilmalónico tóxico en metilmalonil-CoA y lo suministra así al ciclo de Krebs.[5][6] El resultado es una acumulación de ácido metilmalónico.
Bibliografía
editar- ↑ Número CAS
- ↑ Tabita, F. Robert (2009). «The hydroxypropionate pathway of CO2 fixation: Fait accompli». PNAS 106 (50): 21015-21016. doi:10.1073/pnas.0912486107.
- ↑ a b H. Robert Horton, Laurence A. Moran, K. Gray Scrimgeour, J. David Rawn, Marc D. Perry: Biochemie. 4. Auflage, Pearson Education, 2008, ISBN 978-3-8273-7312-0, S. 674–675
- ↑ R. Witkowski, O. Prokop, E. Ullrich: Lexikon der Syndrome und Fehlbildungen: Ursachen, Genetik, Risiken. 7. Auflage, Springer, 2003, ISBN 978-3-540-44305-6, S. 818
- ↑ Gabriel, Marie Cosette; Rice, Stephanie M.; Sloan, Jennifer L.; Mossayebi, Matthew H.; Venditti, Charles P.; Al‐Kouatly, Huda B. (2021-04). «Considerations of expanded carrier screening: Lessons learned from combined malonic and methylmalonic aciduria». Molecular Genetics & Genomic Medicine (en inglés) 9 (4). ISSN 2324-9269. PMC 8123733. PMID 33625768. doi:10.1002/mgg3.1621.
- ↑ Bowman, Caitlyn E.; Wolfgang, Michael J. (2019-01). «Role of the malonyl-CoA synthetase ACSF3 in mitochondrial metabolism». Advances in Biological Regulation (en inglés) 71: 34-40. PMC 6347522. PMID 30201289. doi:10.1016/j.jbior.2018.09.002.