Núcleo celular
En biología, el núcleo celular es una estructura membranosa que se encuentra normalmente en el centro de las células eucariotas. Contiene la mayor parte del material genético celular, organizado en varias moléculas extraordinariamente largas y lineales de ADN, con una gran variedad de proteínas, como las histonas, lo cual conforma lo que llamamos cromosomas. El conjunto de genes de esos cromosomas se denomina genoma nuclear. La función del núcleo es mantener la integridad de esos genes y controlar las actividades celulares regulando la expresión génica.[1] Por ello se dice que el núcleo es el centro de control de la célula.
| Núcleo celular | ||
|---|---|---|
 Dibujo esquemático de la célula eucariota:
1. Nucleolo | ||
| Archivo:Tremendo | ||
| Nombre y clasificación | ||
| Latín | Nucleus | |
| TH | H1.00.01.0.00003 | |
| TH | H1.00.00.0.00003 y H1.00.01.2.00001 | |
| Estudiado (a) por | karyology | |
|
| ||
La principal estructura que constituye el núcleo es la envoltura nuclear, una doble membrana que rodea completamente al orgánulo y separa ese contenido del citoplasma,[2] además de contar con poros nucleares que permiten el paso a través de las membranas para la correcta regulación de la expresión genética y el mantenimiento cromosómico.
Aunque el interior del núcleo no contiene ningún subcompartimento membranoso, su contenido sí está en cierta medida compartimentado, existiendo un número de cuerpos subnucleares compuestos por tipos exclusivos de proteínas, distintos tipos de moléculas de ARN y segmentos particulares de los cromosomas, divididos normalmente por la intensidad con que se expresan. El mejor conocido de todos ellos es el nucléolo, que principalmente está implicado en la síntesis de los ribosomas. Tras ser producidos en el nucléolo, estos se exportan al citoplasma, donde, entre otras cosas, traducen el ARNm.
Historia
editarEl núcleo fue el primer orgánulo en ser descubierto. Probablemente, el dibujo más antiguo que se conserva de este orgánulo se remonta a uno de los primeros microscopistas, Anton van Leeuwenhoek (1632–1723). Este investigador observó un hueco o "lumen", el núcleo, en eritrocitos de salmón.[3] Al contrario que los eritrocitos de mamífero, los del resto de vertebrados son nucleados. El núcleo también fue descrito en 1804 por Franz Bauer, y posteriormente con más detalle por el botánico escocés Robert Brown en una charla dictada ante la Sociedad linneana de Londres en 1831.[4] Brown estaba estudiando la estructura microscópica de orquídeas cuando observó un área opaca, que llamó areola o núcleo, en las células de la capa externa de la flor, si bien no sugirió una función potencial para tal estructura.[5] En 1838 Matthias Schleiden propuso que el núcleo desempeñaba un papel en la generación de células, denominándolo por ello "citoblasto" (constructor de células). Pensaba que había observado células nuevas alrededor de estos "citoblastos". Franz Meyen fue un fuerte opositor de esta opinión habiendo descrito previamente células que se multiplicaban por división y creyendo que muchas células carecerían de núcleo. La idea de que las células podían generarse de novo, bien por el "citoblasto" o bien de otro modo, contradecía los trabajos de Robert Remak (1852) y Rudolf Virchow (1855) quienes propagaron decisivamente el nuevo paradigma de que las células solo eran generadas por otras células ("Omnis cellula e cellula"). La función del núcleo permanecía sin aclarar.[6]
Entre 1876 y 1878 Oscar Hertwig publicó varios estudios sobre la fecundación de huevos de erizo de mar, mostrando que el núcleo del espermatozoide entraba en el oocito, fusionándose con su núcleo. Esta fue la primera vez que se sugirió que un individuo se desarrollaba a partir de una sola célula nucleada. Esto estaba en contradicción con la teoría de Ernst Haeckel que enunciaba que se repetía la filogenia completa de una especie durante el desarrollo embrionario, incluyendo la generación de la primera célula nucleada a partir de una "monerula", una masa desestructurada de moco primordial ("Urschleim", en alemán). Por tanto, la necesidad del núcleo espermático para la fecundación estuvo en discusión por un tiempo. No obstante, Hertwig confirmó su observación en otros grupos animales, como por ejemplo en anfibios y moluscos. Eduard Strasburger obtuvo los mismos resultados en plantas (1884). Esto allanó el camino para la asignación de un papel importante del núcleo en la herencia. En 1873 August Weismann postuló la equivalencia de las células germinales paternas y maternas en la herencia. La función del núcleo como portador de información genética se hizo patente solo después, tras el descubrimiento de la mitosis y el redescubrimiento de la herencia mendeliana a principios del siglo XX. Esto supuso el desarrollo de la teoría cromosómica de la herencia.[6]
Estructuras
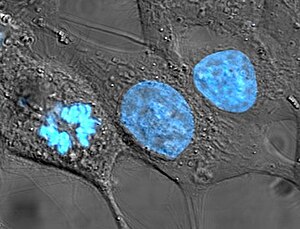
editarEl núcleo es el orgánulo de mayor tamaño en las células animales.[7] En las células de mamífero, el diámetro promedio del núcleo es de aproximadamente 6 micrómetros (μm), lo cual ocupa aproximadamente el 10 % del total del volumen celular.[8] En los vegetales, el núcleo generalmente presenta entre 5 a 25 µm y es visible con microscopio óptico. En los hongos se han observado casos de especies con núcleos muy pequeños, de alrededor de 0,5 µm, los cuales son visibles solamente con microscopio electrónico. En las oósferas de Cycas y de coníferas alcanza un tamaño de 0,6 mm, es decir que resulta visible a simple vista.[9]
El líquido viscoso de su interior se denomina nucleoplasma y su composición es similar a la que se encuentra en el citosol del exterior del núcleo.[10] A grandes rasgos tiene el aspecto de un orgánulo denso y esférico.
Envoltura y poros nucleares
editarLa envoltura nuclear, es a veces llamada membrana nuclear indebidamente, porque se compone de, entre otras cosas, dos membranas, una interna y otra externa, dispuestas en paralelo una sobre la otra. Se encuentra perforada por poros, gracias a estos poros nucleares existe un movimiento bidireccional establecido entre el citosol de la célula y el núcleo. Evita que las macromoléculas difundan libremente entre el nucleoplasma y el citoplasma.[11] La membrana nuclear externa es continua con la membrana del retículo endoplásmico rugoso (RER), y está igualmente tachonada de ribosomas. El espacio entre las membranas se conoce como espacio o cisterna perinuclear y es continuo con la luz del RER.
Los poros nucleares, que proporcionan canales acuosos abiertos por los que pueden difundir por transporte pasivo moléculas pequeñas (que van de 5000 a 44000 Da) y solubles en agua, también prohíbe el paso hacia el núcleo a proteínas globulares mayores de 60kDa. El tamaño de los canales permite que el compartimiento nuclear y el citosol mantengan diferentes conjuntos de proteínas, están formados por subunidades denominadas nucleoporinas (participando alrededor de 30 nucleoporinas distintas en la formación de un solo poro nuclear), que a su vez están agrupadas en sub-complejos multiproteicos ubicados dentro de la envoltura nuclear o asociados a su cara externa o interna respecto al nucleoplasma. Los poros tienen 125 millones de daltons de peso molecular y se componen de aproximadamente 50 (en levaduras) a 100 proteínas (en vertebrados).[7] Los poros tienen un diámetro total de 100 nm; no obstante, el hueco por el que difunden libremente las moléculas es de 9 nm de ancho debido a la presencia de sistemas de regulación en el centro del poro. Este tamaño permite el libre paso de pequeñas moléculas hidrosolubles mientras que evita que moléculas de mayor tamaño entren o salgan de manera inadecuada, como ácidos nucleicos y proteínas grandes. Estas moléculas grandes, en lugar de ello, deben ser transportadas al núcleo de forma activa. El núcleo típico de una célula de mamífero dispone de entre 3000 y 4000 poros a lo largo de su envoltura,[12] cada uno de los cuales contiene una estructura en anillo con simetría octal en la posición en la que las membranas, interna y externa, se fusionan.[13] Anclada al anillo se encuentra la estructura denominada cesta nuclear que se extiende hacia el nucleoplasma, y una serie de extensiones filamentosas que se proyectan en el citoplasma. Ambas estructuras median la unión a proteínas de transporte nucleares.[7]
La mayoría de las proteínas, subunidades del ribosoma y algunos ARNs se transportan a través de los complejos de poro en un proceso mediado por una familia de factores de transportes conocidas como carioferinas. Entre éstas se encuentran las importinas, que intervienen en el transporte en dirección al núcleo, y las que realizan el transporte en sentido contrario, que se conocen como exportinas. La mayoría de las carioferinas interactúan directamente con su carga, aunque algunas utilizan proteínas adaptadoras.[14] Las hormonas esteroideas como el cortisol y la aldosterona, así como otras moléculas pequeñas hidrosolubles implicadas en la señalización celular, pueden difundir a través de la membrana celular y en el citoplasma, donde se unen a proteínas que actúan como receptores nucleares que son conducidas al núcleo. Sirven como factores de transcripción cuando se unen a su ligando. En ausencia de ligando muchos de estos receptores funcionan como histona deacetilasas que reprimen la expresión génica del organismo.[7]
Lámina nuclear
editarEn las células animales existen dos redes de filamentos intermedios que proporcionan soporte mecánico al núcleo: la lámina nuclear forma una trama organizada en la cara interna de la envoltura, mientras que en la cara externa este soporte es menos organizado. Ambas redes de filamentos intermedios también sirven de lugar de anclaje para los cromosomas y los poros nucleares.[8]
La lámina nuclear está compuesta por proteínas que se denominan laminas o proteínas laminares. Como todas las proteínas, éstas son sintetizadas en el citoplasma y más tarde se transportan al interior del núcleo, donde se ensamblan antes de incorporarse a la red preexistente.[15][16] Las laminas también se encuentran en el interior del nucleoplasma, donde forman otra estructura regular conocida como velo nucleoplásmico,[17] que es visible durante la interfase.[18] Las estructuras de las láminas que forman el velo se unen a la cromatina y mediante la disrupción de su estructura inhiben la transcripción de genes que codifican para proteínas.[19]
Como los componentes de otros filamentos intermedios, los monómeros de lámina contienen un dominio alfa helicoidal, utilizado por dos monómeros para enroscarse el uno con el otro, formando un dímero con un motivo en hélice arrollada. Dos de esas estructuras dimétricas se unen posteriormente lado con lado dispuestos de modo antiparalelo para formar un tetrámero denominado protofilamento. Ocho de esos protofilamentos se disponen lateralmente para formar un filamento. Esos filamentos se pueden ensamblar o desensamblar de modo dinámico, lo que significa que los cambios en la longitud del filamento dependen de las tasas en competición de adición y desplazamiento.[8]
Las mutaciones en los genes de las laminas conducen a defectos en el ensamblaje de los filamentos conocidas como laminopatías. De éstas, la más destacable es la familia de enfermedades conocida como progerias, que dan la apariencia de un envejecimiento prematuro a quienes la sufren. Se desconoce el mecanismo exacto por el que los cambios bioquímicos asociados dan lugar al fenotipo progeroide.[20]
En caso de que la lámina nuclear desaparezca el núcleo desaparece, y en caso de volverse a formar el núcleo volverá a estar; esta es una propiedad muy importante especialmente en la mitosis.
Cromosomas
editarEl núcleo celular contiene la mayor parte del material genético celular en forma de múltiples moléculas lineales de ADN conocidas como cromatina, y durante la división celular ésta aparece en la forma bien definida que se conoce como cromosoma. Una pequeña fracción de los genes se sitúa en otros orgánulos, como las mitocondrias o los cloroplastos de las células vegetales.
Cabe destacar que la composición química de la fibra de cromatina radica en segmentos de ADN asociados a proteínas histónicas y no histónicas, quienes se duplican en la fase S de la interfase. Las proteínas histónicas son: H1, H2A, H2B, H3 y H4; dos H2A se ligan con dos H2B por medio de la proteína no histónica nucleoplasmina, mientras que dos H3 y dos H4 se unen con ayuda de la proteína N1, conformando así un octámero, el cual es rodeado por una dos vueltas y media de ADN para consolidar nucleosoma. Este último, al estar sujetado por la H1 pasa a llamarse cromatosoma, y ante la proximidad de la fase M estas H1 entran en contacto directo para consolidar un solenoide de 30 nm de diámetro.
Existen dos tipos de cromatina: la eucromatina es la forma de ADN menos compacta, y contiene genes que son frecuentemente expresados por la célula.[21] El otro tipo, conocido como heterocromatina, es la forma más compacta, y contiene ADN que se transcribe de forma infrecuente. Esta estructura se clasifica a su vez en heterocromatina facultativa, que consiste en genes que están organizados como heterocromatina solo en ciertos tipos celulares o en ciertos estadios del desarrollo, y heterocromatina constitutiva, que consiste en componentes estructurales del cromosoma como los telómeros y los centrómeros.[22] Durante la interfase la cromatina se organiza en territorios individuales discretos, los territorios cromosómicos.[23][24] Los genes activos, que se encuentran generalmente en la región eucromática del cromosoma, tienden a localizarse en las fronteras de los territorios cromosómicos.[25]
Se han asociado anticuerpos a ciertos tipos de organización cromatínica, en particular los nucleosomas con varias enfermedades autoinmunes como el lupus eritematoso sistémico.[26] Estos son conocidos como anticuerpos antinucleares (ANA) y también se han observado en concierto con la esclerosis múltiple en el contexto de una disfunción inmune generalizada.[27] Como el caso antes mencionado de la progeria, el papel que desempeñan los anticuerpos en la inducción de los síntomas de la enfermedad autoinmune no está todavía aclarado.
Nucléolo
editarEl nucléolo es una estructura discreta que se tiñe densamente y se encuentra en el núcleo. No está rodeado por una membrana, por lo que en ocasiones se dice que es un suborgánulo. Se forma alrededor de repeticiones en tándem de ADNr, que es el ADN que codifica el ARN ribosómico (ARNr). Estas regiones se llaman organizadores nucleolares. El principal papel del nucléolo es sintetizar el ARNr y ensamblar los ribosomas. La cohesión estructural del nucléolo depende de su actividad, puesto que el ensamblaje ribosómico en el nucléolo resulta en una asociación transitoria de los componentes nucleolares, facilitando el posterior ensamblaje de otros ribosomas. Este modelo está apoyado por la observación de que la inactivación del ARNr da como resultado en la "mezcla" de las estructuras nucleolares.[28]
El primer paso del ensamblaje ribosómico es la transcripción del ADNr por la ARN polimerasa I, formando un largo pre-ARNr precursor. Este es escindido en las subunidades 5,8S, 18S, y 28S ARNr.[29] La transcripción, procesamiento post-transcripcional y ensamblaje del ARNr tiene lugar en el nucléolo, ayudado por moléculas de ARN pequeño nucleolar, algunas de las cuales se derivan de intrones ayustados de ARN mensajero relacionados con la función ribosomal. Estas subunidades ribosomales ensambladas son las estructuras más grandes que pasan a través de los poros nucleares.[7]
Cuando se observa bajo el microscopio electrónico, se puede ver que el nucléolo se compone de tres regiones distinguibles: los centros fibrilares (FCs), rodeados por el componente fibrilar denso (DFC), que a su vez está bordeado por el componente granular (GC). La transcripción del ADNr tiene lugar tanto en el FC como en la zona de transición FC-DFC, y por ello cuando la transcripción del ADNr aumenta, se observan más FC's. La mayor parte de la escisión y modificación de los ARNr tiene lugar en el DFC, mientras que los últimos pasos que implican el ensamblaje de proteínas en las subunidades ribosómicas tienen lugar en el GC.[29]
Otros cuerpos subnucleares
editar| Nombre de la estructura | Diámetro de la estructura |
|---|---|
| Cuerpos de Cajal | 0,2-2,0 µm[30] |
| PIKA | 5 µm[31] |
| Cuerpos PML | 0,2–1,0 µm[32] |
| Paraspeckles | 0,2–1,0 µm[33] |
| Speckles | 20–25 nm[31] |
Además del nucléolo, el núcleo contiene una cierta cantidad de cuerpos delimitados no membranosos. Entre estos se encuentran los cuerpos de Cajal (cuerpos enrollados), los llamados "Géminis de los cuerpos enrollados" (Gemini of coiled bodies, en inglés), la denominada Asociación Cariosómica Polimórfica Interfásica (PIKA, por sus siglas en inglés de Polymorphic Interphase Karyosomal Association), los Cuerpos de la Leucemia Promielocítica (PMLs, por sus siglas en inglés de promyelocytic leukaemia), los "paraspeckles" y los "specles de ayuste" o "motas de empalme" ("splicing speckles" en inglés). Aunque se sabe poco sobre el número de estos dominios subnucleares, son significativos en cuanto que muestran que el nucleoplasma no es una mezcla uniforme, sino que más bien contiene subdominios funcionales organizados.[32]
Otras estructuras subnucleares aparecen como parte de procesos patológicos. Por ejemplo, se ha visto la presencia de pequeños bastones intranucleares en algunos casos de miopatía nemalínica. Esta enfermedad se produce típicamente por mutaciones en el gen de la actina, y los bastones en sí mismos están constituidos por la actina producida a partir de tales genes mutantes, así como otras proteínas del citoesqueleto.[34]
Cuerpos de Cajal y GEMs
editarEl núcleo típico posee de 1 a 10 estructuras compactas denominadas Cuerpos de Cajal o cuerpos enrollados (CBs, por sus siglas en inglés de Coiled Bodies), cuyo diámetro mide entre 0,2 µm y 2,0 µm dependiendo del tipo celular y especie.[30] Cuando se observan bajo el microscopio electrónico, se asemejan a ovillos de hilos enmarañados,[31] y son focos densos de distribución de la proteína coilina.[35] Los CBs están implicados en varios tipos distintos de funciones relacionadas con el procesamiento de ARN, específicamente en la maduración del ARN nucleolar pequeño (snoRNA) y el ARN nuclear pequeño (snRNA), y modificación del ARNm de histonas.[30]
Semejantes a los cuerpos de Cajal se encuentran los "Géminis de cuerpos enrollados o GEMs (por sus siglas en inglés de Gemini of Coiled Bodies), cuyo nombre se deriva de la constelación de Géminis por su relación casi como de gemelos con los Cuerpos de Cajal. Los GEMs son similares en forma y tamaño a estos últimos, y de hecho son virtualmente indistinguibles al microscopio.[35] A diferencia de los cuerpos de Cajal, no contienen snRNPs, pero contienen una proteína que se denomina motoneurona superviviente (SMN, por sus siglas en inglés de survivor of motor neurons), cuya función se relaciona con la biogénesis del snRNP. Se cree que los GEMs ayudan a los CBs en la biogénesis del snRNP,[36] aunque también se ha sugerido a partir de evidencias de microscopía que los CBs y los GEMs son diferentes manifestaciones de la misma estructura.[35]
Dominios PIKA y PTF
editarLos dominios PIKA, o Asociaciones Cariosómicas Polimórficas de Interfase, fueron descritos por primera vez en estudios de microscopía en 1991. Su función era y permanece poco clara, aunque no se piensa que estén asociados con la replicación activa de ADN, transcripción o procesamiento de ARN.[37] Se ha visto que frecuentemente se asocian con dominios discretos definidos por localizaciones densas del factor de transcripción PTF, que promueve la transcripción del ARNnp.[38]
Cuerpos PML
editarLos cuerpos PML o de la proteína de la leucemia promielocítica (PML, por sus siglas en inglés de Promyelocytic leukaemia) son cuerpos esféricos que se encuentran dispersos en el nucleoplasma, y que miden alrededor de 0,2–1,0 µm. Se conocen por otros nombres, como dominio «nuclear 10» (ND10), «cuerpos de Kremer», y «dominios oncogénicos PML». A menudo se ven en el núcleo asociados con los cuerpos de Cajal. Se ha sugerido que desempeñan un papel en la regulación de la transcripción. Se los suele identificar en células tumorales (como en casos de Leucemia promielocítica aguda) por lo que también actúan como marcadores tumorales.[32]
Paraspeckles
editarDescubiertos en 2002, los paraspeckles son compartimentos de forma irregular del espacio intercromatínico del núcleo.[39] Fueron documentados por primera vez en células HeLa, donde por lo general se encuentran entre 10–30 por núcleo,[40] actualmente se sabe que los paraspeckles también existen en todas las células primarias humanas, los linajes de células transformadas y las secciones de tejidos.[41] Su nombre se deriva de su distribución en el núcleo. El prefijo "para" es una apócope de "paralelo" y "speckles" (mancha o mota, en inglés) se refiere a su proximidad a los "splicing speckles" o motas de ayuste.[40]
Los paraspeckles son estructuras dinámicas que se alteran en respuesta a cambios en la actividad celular metabólica. Son dependientes de la transcripción,[39] y en ausencia de transcripción de la ARN Pol II, los paraspeckles desaparecen, y todas las proteínas asociadas que lo componen (PSP1, p54nrb, PSP2, CFI(m)68 y PSF) forman un tapón perinucleolar en forma de cuarto creciente en el nucléolo. Este fenómeno se manifiesta durante el ciclo celular, en el que están presentes en interfase y durante toda la mitosis, excepto en telofase. Durante la telofase, cuando los dos núcleos hijos se forman, no hay transcripción por parte de la ARN polimerasa II, de modo que los componentes proteicos forman en su lugar un tapón perinucleolar.[41]
Speckles
editarEn ocasiones denominados agrupaciones de gránulos intercromatínicos o compartimentos de factores de ayuste, los speckles, manchas o motas, son ricos en ARNnps procedentes del ayuste y otras proteínas del mismo proceso que se necesitan en el procesamiento del pre-ARNm.[42] Debido a los requerimientos variables de la célula, la composición y localización de estos cuerpos cambia de acuerdo a la transcripción de ARNm y a la regulación vía fosforilación de proteínas específicas.[43]
Cuerpos de escisión
editarLlamados Cleavage bodies, en inglés, se suelen encontrar asociados a los cuerpos de Cajal, con un diámetro de 0,2 a 1,0 μm y en número de 1-10 por núcleo. A diferencia de otros cuerpos nucleares, aparecen solamente durante determinados periodos del ciclo celular. Algunos de estos contienen el complejo CPSF-100 (por sus siglas en inglés de cleavage and polyadenylation specificity factor: factor de especificidad para el corte y la poliadenilación), y se pueden observar predominantemente durante las fases S y G, mientras que los que contienen el factor de poliadenilación CstF-64-containing se observan principalmente en la fase S. Están asociados con el clúster de genes de la histona.[44]
Cuerpos DDX1
editarLos cuerpos DDX1 son agregados de la proteína DDX1, perteneciente a la familia de helicasas de ARN que contienen el motivo "DEAD box", se encuentran en un número que varía de dos a cuatro. Puesto que parece que estos cuerpos son reclutados en lugares en los que se ha producido daño en el ADN que está hibridando con ADN, parece que estos cuerpos desempeñan un papel en la reparación de zonas con rupturas de doble cadena, facilitando la reparación guiada por patrón de regiones del genoma transcripcionalmente activas.[44]
Función
editarLa principal función del núcleo celular es controlar la expresión genética y mediar en la replicación del ADN en el ciclo celular. El núcleo proporciona un emplazamiento para la transcripción en el citoplasma, permitiendo niveles de regulación que no están disponibles en procariotas. Tiene diferentes funciones:
- En el núcleo se guardan los genes en forma de cromosomas (durante la mitosis) o cromatina (durante la interfase)
- Transporta los factores de regulación a través de los poros nucleares
- Produce ácido ribonucleico mensajero (ARNm) que codifica proteínas.
- Produce pre-ribosomas (ARNr) en el nucléolo.
Compartimentalización celular
editarLa envoltura nuclear permite al núcleo controlar su contenido y separarlo del resto del citoplasma cuando sea necesario. Esto es importante para controlar procesos en cualquiera de los lados de la membrana nuclear. En algunos casos, cuando se precisa restringir un proceso citoplasmático, un participante clave se retira al núcleo, donde interactúa con factores de transcripción para reprimir la producción de ciertas enzimas de la ruta. Este mecanismo regulador tiene lugar en el caso de la glucólisis, una ruta celular en la que se utiliza la glucosa para producir energía. La hexoquinasa es la enzima responsable del primer paso de la glucólisis, produciendo glucosa-6-fosfato a partir de la glucosa. A altas concentraciones de fructosa-6-fosfato, una molécula que se forma posteriormente a partir de la glucosa-6-fosfato, una proteína reguladora retira la hexoquinasa al núcleo,[45] donde forma un complejo con otras proteínas nucleares que reprime la transcripción de los genes implicados en la glucólisis.[46]
Para controlar qué genes se deben transcribir, la célula impide el acceso físico de algunos factores de transcripción responsables de regular la expresión génica hasta que son activados por otras rutas de señalización. Esto impide que se den incluso pequeños niveles de expresión génica inadecuada. Por ejemplo, en el caso de los genes controlados por NF-κB, que están implicados en la mayor parte de las respuestas inflamatorias, la transcripción se induce en respuesta a una cascada de señalización celular como la que se inicia con la molécula señalizadora TNF-α uniéndose a un receptor de la membrana celular, lo que produce el reclutamiento de proteínas señalizadoras y finalmente la activación del factor de transcripción NF-κB. Una señal de localización nuclear que posee la proteína NF-κB le permite ser transportada a través del poro nuclear al núcleo, donde estimula la transcripción de los genes diana.[8]
La compartimentalización permite a la célula impedir la traducción de ARNm no ayustado.[47] El ARNm contiene intrones que se deben retirar antes de ser traducidos para producir proteínas funcionales. El ayuste se efectúa en el interior del núcleo antes de que el ARNm pueda acceder a los ribosomas para su traducción. Sin el núcleo los ribosomas traducirían ARNm recién transcrito y sin procesar, lo que produciría proteínas mal plegadas y deformadas.
Expresión génica
editarLa expresión génica implica en primer lugar la transcripción, en la que el ADN se utiliza como molde para producir ARN. En el caso de los genes que codifican proteínas, el ARN generado por este proceso es el ARN mensajero (ARNm), que posteriormente precisa ser traducido por los ribosomas para formar una proteína. Puesto que los ribosomas se localizan fuera del núcleo, el ARNm sintetizado debe ser exportado.[48]
Puesto que el núcleo es el lugar donde se da la transcripción, está dotado de un conjunto de proteínas que, o bien están implicadas directamente en este proceso, o en su regulación. Entre éstas encontramos las helicasas, que desenrollan la molécula de ADN de doble cadena para facilitar el acceso de la maquinaria de síntesis, la ARN polimerasa, que sintetiza el ARN a partir del molde de ADN, la topoisomerasa, que varía la cantidad de superenrollamiento del ADN, así como una amplia variedad de factores de transcripción que regulan la expresión génica.[49]
Procesamiento del pre-ARNm
editarLas moléculas de ARNm recién sintetizadas se conocen como transcritos primarios o pre-ARNm. Posteriormente se deben someter a modificación post-transcripcional en el núcleo antes de ser exportados al citoplasma. El ARNm que aparece en el núcleo sin estas modificaciones acaba degradado en lugar de utilizarse para la traducción en los ribosomas. Las tres modificaciones principales son: La del extremo 5' (5' caping), la poliadenilación del extremo 3' y el ayuste de ARN. Mientras permanece en el núcleo, el pre-ARNm se asocia con varias proteínas en complejos conocidos como ribonucleoproteínas heterogéneas nucleares o hnRNPs. La adición de las modificaciones del extremo 5' tiene lugar en el momento de la transcripción y es el primer paso en las modificaciones postranscripcionales. La cola de poliadenina 3' solo se añade una vez que la transcripción está completa.
El ayuste (splicing o corte y empalme) de ARN, llevado a cabo por un complejo denominado espliceosoma es el proceso por el que los intrones se retiran del pre-ARNm, permaneciendo únicamente los exones conectados para formar una sola molécula continua. Este proceso normalmente finaliza tras los dos anteriores, pero puede comenzar antes de que la síntesis esté completa en transcritos con muchos exones.[7] Muchos pre-ARNm's, incluyendo los que codifican anticuerpos, se pueden cortar y empalmar de múltiples formas para producir diferentes ARNm maduros, que por ello codifican diferentes secuencias de proteínas. Este proceso se conoce como ayuste alternativo, y permite la producción de una gran variedad de proteínas a partir de una cantidad limitada de ADN.
Dinámica y regulación
editarTransporte nuclear
editarEl transporte de moléculas hacia el exterior e interior del núcleo, puede llevarse a cabo gracias a que en todas las células eucariotas la envoltura nuclear está perforada por poros nucleares, constituidos por grandes complejos multiproteicos. La entrada y salida de grandes moléculas del núcleo está estrictamente controlada por los complejos de poros nucleares. Aunque las pequeñas moléculas pueden entrar en el núcleo sin regulación,[50] las macromoléculas como el ARN y las proteínas requieren asociarse a carioferinas llamadas importinas para entrar en el núcleo, y exportinas para salir. Las proteínas cargadas que deben ser translocadas desde el citoplasma al núcleo contienen cortas secuencias de aminoácidos conocidas como señales de localización nuclear que están unidas a las importinas, mientras que las transportadas desde el núcleo al citoplasma poseen señales de exportación nuclear unidas a las exportinas. La capacidad de las importinas y las exportinas para transportar su carga está regulada por GTPasas, enzimas que hidrolizan GTP liberando energía. La GTPasa clave en el transporte nuclear es Ran, que puede unir o bien GTP o bien GDP (guanosina difosfato), dependiendo de si está localizada en el núcleo o en el citoplasma. Mientras que las importinas dependen de Ran-GTP para disociarse de su carga, las exportinas necesitan Ran-GTP para unirse a su carga.[14]
Señales de localización necesarias para el transporte
editarLas señales de localización nuclear hacen que el flujo de proteínas del citosol al núcleo sea selectivo. Estas señales únicamente están presentes en las proteínas nucleares, consisten en una secuencia corta que va entre 4 y 8 aminoácidos. Cuando hay importación nuclear esta señal se denomina señal de localización nuclear (NLS), y cuando hay exportación nuclear se denomina señal de exportación nuclear (NES).
Existen dos tipos de NLS: las monopartitas y las bipartitas. Las NLS monopartitas están formadas por un solo grupo de residuos básicos y las NLS bipartitas están formadas por dos grupos de residuos de lisinas y argininas. Este tipo de señales son reconocidas específicamente por la Importina α y las proteínas que las contienen son transportadas al núcleo por el heterodímero Importina α/Importina β1. Por otro lado, las NES son secuencias cortas de aminoácidos hidrofóbicos, principalmente leucinas.
A estas señales de localización nuclear, que se localizan en los poros nucleares, se unen una o más nucleoporinas, que son proteínas citosólicas, que contienen la N-acetilglucosamina, un azúcar simple que ayuda a su identificación mediante el uso de lectinas y anticuerpos específicos. Las nucleoporinas colaboran dirigiendo a la proteína nuclear hacia el centro del complejo de poro, donde se une a las fibrillas que están extendidas hacia el citosol y que se proyectan a partir del anillo del complejo. Estas fibrillas guían a las proteínas nucleares hacia el centro del complejo de poro, donde es transportada activamente hacia el interior nuclear mediante un proceso que requiere la hidrólisis de GTP.
Carioferinas
editarSon proteínas mediadoras del transporte a través del complejo del poro nuclear. Su clasificación depende de la dirección del transporte para el que fueron inicialmente descritas, se les ha clasificado como importinas y exportinas.
Las importinas, en su mayoría, pertenecen a la superfamilia de las importinas β y se encargan de regular el transporte de la mayor parte de las proteínas y de diferentes especies de ARN, excepto ARNm.
Exportación nuclear
editarSucede en condiciones de alta concentración de Ran-GTP, reconoce una proteína que contiene una NES (señal de exportación nuclear) junto a una molécula de Ran-GTP. El complejo es entonces capaz de interaccionar con el complejo del poro nuclear y atravesarlo hasta el citoplasma. Una vez allí, otras proteínas Ran promueven la actividad GTPasa de Ran, que hidroliza el GTP y pasa a convertirse en Ran-GDP. La hidrólisis produce un cambio conformacional en Ran, produciéndose el desensamblaje de la exportina-carga, quedando la carga libre en el citoplasma. Las moléculas de Ran-GDP y exportina se reciclan para un nuevo ciclo de transporte.
Las proteínas especializadas de exportación sirven para la traslocación de ARNm maduro y ARNt al citoplasma después de que la modificación postranscripcional se completa. Este mecanismo de control de calidad es importante debido al papel central de esas moléculas en la traducción de proteínas. La expresión inadecuada de una proteína debido a una escisión de exones incompleta o la incorporación impropia de aminoácidos podría tener consecuencias negativas para la célula. Por ello, el ARN no modificado por completo que alcanza el citoplasma es degradado en lugar de ser utilizado en la traducción.[7]
Importación nuclear
editarLa importación nuclear depende de que la importina se una a su carga en el citoplasma y lo transporte a través del poro nuclear al núcleo. Las importinas interaccionan en el citoplasma, en condiciones de baja concentración de RanGTP, con la proteína con una NLS (señal de localización nuclear), y entra al interior del núcleo mediante asociación con proteínas del complejo del poro nuclear. Una vez en el nucleoplasma, la presencia de altos niveles de RanGTP causa la destrucción del complejo importina-carga, liberándose la carga en el interior del núcleo. La Importina α es transportada de nuevo al citoplasma mediante su interacción reiniciándose de nuevo el proceso.
Regulación del transporte entre el núcleo y el citosol
editarEl transporte entre el citosol y el núcleo puede regularse inactivando la señal de localización nuclear de las proteínas nucleares por fosforilación o cuando dichas proteínas se unan a proteínas citosólicas inhibidoras que las retienen en el citosol mediante interacciones con el citoesqueleto o con organelos específicos, o enmascaran sus señales de localización nuclear. Sin embargo, cuando la célula recibe el estímulo necesario, la proteína nuclear es liberada y es transportada hacia el núcleo.
De una forma similar, puede estar controlada la exportación de ARN desde el núcleo. Como en la importación activa hacia el núcleo, la exportación requiere una señal. Es probable que las señales de exportación nuclear se localicen en las subunidades proteicas de dichos complejos, y que se activen después de ensamblarse correctamente con los componentes del ARN.
Por todo esto puede concluirse que el mecanismo de transporte de macromoléculas a través del poro nuclear, es muy distinto al mecanismo que ocurre a través de las membranas de otros organelos, pues el transporte nuclear no ocurre por un transportador proteico que atraviesa una o más bicapas lipídicas sino mediante un poro con un canal acuoso regulado. También, mientras que las proteínas nucleares son transportadas a través de los poros manteniendo su conformación completamente plegada, en el transporte a otros organelos, las proteínas tienen que desplegarse. Por último, las señales de localización nuclear no se eliminan después del transporte hacia el núcleo, pues las proteínas nucleares han de ser importadas al núcleo varias veces, después de cada división celular. Pero, cuando una proteína ha sido importada a cualquier otro organelo membranoso, el péptido señal es a menudo eliminado después de la translocación proteica.
Ensamblaje y desensamblaje
editarDurante su periodo de vida un núcleo puede desensamblarse, o bien en el transcurso de la división celular, o como consecuencia de la apoptosis, una forma regulada de muerte celular. Durante estos acontecimientos, los componentes estructurales del núcleo —la envoltura y la lámina— son sistemáticamente degradados.
Durante el ciclo celular la célula se divide para formar dos células. Para que este proceso sea posible, cada una de las nuevas células hija debe adquirir un juego completo de genes, un proceso que requiere la replicación de los cromosomas, así como la segregación en juegos separados. Esto se produce cuando los cromosomas ya replicados, las cromátides hijas, se unen a los microtúbulos, los cuales a su vez se unen a diferentes centrosomas. Las cromátides hija pueden ser fraccionadas hacia localizaciones separadas en la célula. No obstante, en muchas células el centrosoma se localiza en el citoplasma, fuera del núcleo, por lo que los microtúbulos serían incapaces de unirse a las cromátides en presencia de la envoltura nuclear.[51] Por tanto, en los estadios tempranos del ciclo celular, comenzando en profase y hasta casi la prometafase, se desmantela la membrana nuclear.[17] De forma similar, durante el mismo periodo se desensambla la lámina nuclear, un proceso que está regulado por la fosforilación de las láminas.[52] Hacia el final del ciclo celular se reforma la membrana nuclear, y en torno al mismo tiempo, la lámina nuclear se reensambla desfosforilando las proteínas laminares.[52]
La apoptosis es un proceso controlado en el que los componentes estructurales de la célula son destruidos, lo que produce la muerte de la célula. Los cambios asociados con la apóptosis afectan directamente al núcleo y a sus contenidos, por ejemplo en la condensación de la cromatina y la desintegración de la envoltura nuclear y la lámina. La destrucción de las redes de lámina está controlada por proteasas apoptóticas especializadas denominadas caspasas, que desintegran la lámina nuclear y de ese modo degradan la integridad estructural del núcleo. La desintegración de la lámina nuclear se utiliza en ocasiones en los laboratorios como indicador de la actividad de la caspasa en ensayos de actividad apoptótica temprana.[17] Las células que expresan láminas resistentes a las caspasas son deficientes en los cambios nucleares relacionados con la apoptosis, lo que sugiere que las láminas desempeñan un papel importante en el inicio de los eventos que conducen a la degradación apoptótica del núcleo.[17] La inhibición del propio ensamblaje de la lámina nuclear es por sí misma un inductor de la apoptosis.[53]
La envoltura nuclear actúa como una barrera que evita que virus de ADN o ARN penetren en el núcleo. Algunos virus precisan acceder a proteínas dentro del núcleo para replicarse o ensamblarse. Los virus de ADN, como el herpesvirus se replican y ensamblan en el núcleo celular, y salen brotando a través de la membrana nuclear interna. Este proceso se acompaña del desensamblaje de la lámina nuclear en la cara nuclear de la membrana interna.[17]
Células anucleadas y polinucleadas
editarAunque la mayor parte de las células tienen un único núcleo, algunos tipos celulares carecen de él, en tanto que otros poseen múltiples núcleos. Esto puede ser un proceso normal, como es en el caso de la maduración de los eritrocitos, o bien el resultado de una división celular defectuosa.
Las células anucleadas carecen de núcleo, y por lo mismo son incapaces de dividirse para producir células hijas. El caso mejor conocido de célula anucleada es el eritrocito de mamífero, que también carece de otros orgánulos como mitocondrias, y sirven en principio como vehículos de transporte de oxígeno desde los pulmones a los tejidos. Los eritrocitos maduran gracias a la eritropoyesis en la médula ósea, donde pierden su núcleo, orgánulos y ribosomas. El núcleo es expulsado durante el proceso de diferenciación de eritroblasto a reticulocito, el cual es el precursor inmediato del eritrocito maduro.[54] mutágenos puede inducir la liberación de algunos eritrocitos inmaduros "micronucleados" al torrente sanguíneo.[55][56] También pueden aparecer células anucleadas a partir de una división celular defectuosa en la que una célula hija carece de núcleo, mientras que la otra posee dos.
Las células polinucleadas contienen múltiples núcleos. La mayor parte de los protozoos de la clase Acantharea,[57] y algunos hongos que forman micorrizas,[58] tienen células polinucleadas de forma natural. Otros ejemplos serían los parásitos intestinales del género Giardia, que posee dos núcleos en cada célula.[59] En los seres humanos, el músculo esquelético posee células, llamadas miocitos, que se convierten en polinucleadas durante su desarrollo. La disposición resultante de los núcleos en la región periférica de la célula permite un espacio intracelular máximo para las miofibrillas.[7] Las células multinucleadas también pueden ser anormales en humanos. Por ejemplo, las que surgen de la fusión de monocitos y macrófagos, conocidas como células multinucleadas gigantes, pueden ser observadas en ocasiones acompañando a la inflamación,[60] y también están implicadas en la formación de tumores.[61]
Evolución
editarAl ser la mejor característica que define la célula eucariota, el origen evolutivo del núcleo ha sido objeto de mucha especulación. Entre las teorías propuestas, se pueden considerar cuatro como las principales, aunque ninguna de ellas ha encontrado un amplio apoyo.[62]
Teorías endosimbioticas
editarLa teoría conocida como "modelo sintrófico" propone que una relación simbiótica entre arqueas y bacterias creó la primera célula eucariota nucleada. Se establece la hipótesis de que la simbiosis tuvo lugar cuando una arquea antigua similar a los actuales metanógenos fueron invadidos y parasitados por bacterias similares a las actuales myxobacteria, formando finalmente el núcleo primitivo. Esta teoría es análoga a teoría aceptada del origen de las mitocondrias y cloroplastos eucariotas, de los que se piensa que se han desarrollado por una relación endosimbionte similar entre protoeucariotas y bacterias aerobias.[63] El origen arqueano del núcleo está apoyado por la circunstancia de que tanto arqueas como eucariotas tienen genes similares en ciertas proteínas, incluyendo las histonas. Al observar que las myxobacterias son móviles, pueden formar complejos multicelulares y poseen proteínas G similares a las de eucariotas, también se puede aceptar un origen bacteriano de la célula eucariota.[64] Una propuesta similar establece que una célula similar a la eucariota, el cronocito, apareció en primer lugar, y posteriormente fagocitó arqueas y bacterias para dar lugar al núcleo y a la célula eucariota.[65]
Un modelo más controvertido, conocido como eucariogénesis viral afirma que muchos rasgos de la célula eucariota como la presencia de un núcleo que se continúa con la membrana surgieron por la infección de un antepasado procariota por un gran virus de ADN (posiblemente de un Virus nucleocitoplasmáticos de ADN de gran tamaño). Esto está sugerido sobre la base de similitudes entre eucariotas y virus como las hebras lineales de ADN, el procesamiento "caping" del extremo 5' del ARNm y la fuerte unión a proteínas del ADN (haciendo a las histonas análogas de la envoltura vírica). Una versión de esta propuesta sugiere que el núcleo evolucionó concertadamente con la fagocitosis para dar lugar a un depredador celular primitivo.[66] Otra variante propone que los eucariotas se originaron de arqueas primitivas infectadas por poxvirus, basándose en la similitud de las modernas ADN polimerasas entre estos y los eucariotas.[67][68] Se ha sugerido que la cuestión no resuelta de la evolución de la sexualidad pudo estar relacionada con la hipótesis de la eucariogénesis viral.[69]
Teorías no endosimbioticas
editarEste modelo propone que las células protoeucariotas evolucionaron a partir de bacterias sin que se diera un estadio simbionte. Este modelo se basa en la existencia de una bacteria moderna perteneciente al filo de las planctomycetes que poseen una estructura nuclear con poros primitivos y otras estructuras compartimentalizadas por membrana.[70]
Finalmente, una propuesta muy reciente sugiere que las variantes tradicionales de las teorías endosimbiontes son insuficientes para explicar el origen del núcleo eucariota. Este modelo, denominado la hipótesis de la exomembrana, sugiere que el núcleo se originó en lugar de ello a partir de una célula ancestral original que desarrolló una segunda membrana celular exterior. La membrana interior que encerraba la célula original se convirtió entonces en la membrana nuclear evolucionando para desarrollar estructuras de poro cada vez más elaboradas para el paso de componentes celulares sintetizados internamente, como las subunidades ribosómicas.[71]
Referencias
editar- ↑ Cediel, Juan Fernando; Cárdenas, María Helena; García, Ananías (2009). Manual de histología: Tejidos fundamentales. Universidad del Rosario. ISBN 9789588378893. Consultado el 19 de febrero de 2018.
- ↑ LÓPEZ, MARÍA BELÉN YÉLAMOS; FERNÁNDEZ, MARÍA INMACULADA FERNÁNDEZ (2016). Biología. 2º Bachillerato. Ediciones Paraninfo, S.A. ISBN 9788428337878. Consultado el 19 de febrero de 2018.
- ↑ Leeuwenhoek, A. van: Opera Omnia, seu Arcana Naturae ope exactissimorum Microscopiorum detecta, experimentis variis comprobata, Epistolis ad varios illustres viros. J. Arnold et Delphis, A. Beman, Lugdinum Batavorum 1719–1730. Citado por: Dieter Gerlach, Geschichte der Mikroskopie. Verlag Harry Deutsch, Frankfurt am Main, Germany, 2009. ISBN 978-3-8171-1781-9.
- ↑ Harris, H (1999). The Birth of the Cell. New Haven: Yale University Press.
- ↑ Brown, Robert (1866). «On the Organs and Mode of Fecundation of Orchidex and Asclepiadea». Miscellaneous Botanical Works I: 511-514.
- ↑ a b Cremer, Thomas (1985). Von der Zellenlehre zur Chromosomentheorie. Berlin, Heidelberg, New York, Tokyo: Springer Verlag. ISBN 3-540-13987-7. Online Version here
- ↑ a b c d e f g h Lodish, H; Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipursky SL, Darnell J. (2004). Molecular Cell Biology (5th edición). New York: WH Freeman.
- ↑ a b c d Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter, ed. (2002). Molecular Biology of the Cell, Chapter 4, pages 191-234 (4th edición). Garland Science.
- ↑ González, A.M. Núcleo Archivado el 2 de julio de 2011 en Wayback Machine.. Morfología de Plantas Vasculares. Facultad de Ciencias Agrarias, Universidad Nacional del Nordeste. Consultado el 30 de octubre de 2009.
- ↑ Clegg JS (febrero de 1984). «Properties and metabolism of the aqueous cytoplasm and its boundaries». Am. J. Physiol. 246 (2 Pt 2): R133-51. PMID 6364846.
- ↑ Paine P, Moore L, Horowitz S (1975). «Nuclear envelope permeability». Nature 254 (5496): 109-114. ISSN 0028-0836. PMID 1117994. doi:10.1038/254109a0.
- ↑ Rodney Rhoades, Richard Pflanzer, ed. (1996). «Ch3». Human Physiology (3rd edición). Saunders College Publishing.
- ↑ Shulga N, Mosammaparast N, Wozniak R, Goldfarb D (2000). «Yeast nucleoporins involved in passive nuclear envelope permeability». J Cell Biol 149 (5): 1027-1038. PMID 10831607. doi:10.1083/jcb.149.5.1027.
- ↑ a b Pemberton L, Paschal B (2005). «Mechanisms of receptor-mediated nuclear import and nuclear export». Traffic 6 (3): 187-198. PMID 15702987. doi:10.1111/j.1600-0854.2005.00270.x.
- ↑ Stuurman N, Heins S, Aebi U (1998). «Nuclear lamins: their structure, assembly, and interactions». J Struct Biol 122 (1–2): 42-66. PMID 9724605. doi:10.1006/jsbi.1998.3987.
- ↑ Goldman A, Moir R, Montag-Lowy M, Stewart M, Goldman R (1992). «Pathway of incorporation of microinjected lamin A into the nuclear envelope». J Cell Biol 119 (4): 725-735. PMID 1429833. doi:10.1083/jcb.119.4.725.
- ↑ a b c d e Goldman R, Gruenbaum Y, Moir R, Shumaker D, Spann T (2002). «Nuclear lamins: building blocks of nuclear architecture». Genes Dev 16 (5): 533-547. PMID 11877373. doi:10.1101/gad.960502.
- ↑ Moir RD, Yoona M, Khuona S, Goldman RD. (2000). «Nuclear Lamins A and B1: Different Pathways of Assembly during Nuclear Envelope Formation in Living Cells». Journal of Cell Biology 151 (6): 1155-1168. PMID 11121432. doi:10.1083/jcb.151.6.1155.
- ↑ Spann TP, Goldman AE, Wang C, Huang S, Goldman RD. (2002). «Alteration of nuclear lamin organization inhibits RNA polymerase II–dependent transcription». Journal of Cell Biology 156 (4): 603-608. PMID 11854306. doi:10.1083/jcb.200112047.
- ↑ Mounkes LC, Stewart CL (2004). «Aging and nuclear organization: lamins and progeria». Current Opinion in Cell Biology 16: 322-327. PMID 15145358. doi:10.1016/j.ceb.2004.03.009.
- ↑ Ehrenhofer-Murray A (2004). «Chromatin dynamics at DNA replication, transcription and repair». Eur J Biochem 271 (12): 2335-2349. PMID 15182349. doi:10.1111/j.1432-1033.2004.04162.x.
- ↑ Grigoryev S, Bulynko Y, Popova E (2006). «The end adjusts the means: heterochromatin remodelling during terminal cell differentiation». Chromosome Res 14 (1): 53-69. PMID 16506096. doi:10.1007/s10577-005-1021-6.
- ↑ Schardin, Margit; T. Cremer, H. D. Hager, M. Lang (diciembre de 1985). «Specific staining of human chromosomes in Chinese hamster x man hybrid cell lines demonstrates interphase chromosome territories». Human Genetics (Springer Berlin / Heidelberg) 71 (4): 281-287. PMID 2416668. doi:10.1007/BF00388452. Archivado desde el original el 13 de septiembre de 2019. Consultado el 23 de julio de 2009.
- ↑ Lamond, Angus I.; William C. Earnshaw (24 de abril de 1998). «Structure and Function in the Nucleus». Science 280: 547-553. PMID 9554838. doi:10.1126/science.280.5363.547.
- ↑ Kurz, A; S Lampel, JE Nickolenko, J Bradl, A Benner, RM Zirbel, T Cremer and P Lichter (1996). «Active and inactive genes localize preferentially in the periphery of chromosome territories». The Journal of Cell Biology (The Rockefeller University Press) 135: 1195-1205. PMID 8947544. doi:10.1083/jcb.135.5.1195. Archivado desde el original el 29 de septiembre de 2007.
- ↑ NF Rothfield, BD Stollar (1967). «The Relation of Immunoglobulin Class, Pattern of Antinuclear Antibody, and Complement-Fixing Antibodies to DNA in Sera from Patients with Systemic Lupus Erythematosus». J Clin Invest 46 (11): 1785-1794. PMID 4168731.
- ↑ S Barned, AD Goodman, DH Mattson (1995). «Frequency of anti-nuclear antibodies in multiple sclerosis». Neurology 45 (2): 384-385. PMID 7854544.
- ↑ Hernandez-Verdun, Daniele (2006). «Nucleolus: from structure to dynamic». Histochem. Cell. Biol 125 (125): 127-137. doi:10.1007/s00418-005-0046-4.
- ↑ a b Lamond, Angus I.; Judith E. Sleeman. «Nuclear substructure and dynamics». Current Biology 13 (21): R825-828. PMID 14588256. doi:10.1016/j.cub.2003.10.012.
- ↑ a b c Cioce M, Lamond A. «Cajal bodies: a long history of discovery». Annu Rev Cell Dev Biol 21: 105-131. PMID 16212489. doi:10.1146/annurev.cellbio.20.010403.103738.
- ↑ a b c Pollard, Thomas D.; William C. Earnshaw (2004). Cell Biology. Philadelphia: Saunders. ISBN 0-7216-3360-9.
- ↑ a b c Dundr, Miroslav; Tom Misteli (2001). «Functional architecture in the cell nucleus». Biochem. J. (356): 297-310. PMID 11368755. doi:10.1146/annurev.cellbio.20.010403.103738.
- ↑ Fox, Archa (7 de marzo de 2007). Paraspeckle Size. Entrevista con R. Sundby. E-mail Correspondence.
- ↑ Goebel, H.H.; I Warlow (enero de 1997). «Nemaline myopathy with intranuclear rods—intranuclear rod myopathy». Neuromuscular Disorders 7 (1): 13-19. PMID 9132135. doi:10.1016/S0960-8966(96)00404-X.
- ↑ a b c Matera AG, Frey MA. (1998). «Coiled Bodies and Gems: Janus or Gemini?». American Journal of Human Genetics 63 (2): 317-321. PMID 9683623. doi:10.1086/301992.
- ↑ Matera, A. Gregory (1998). «Of Coiled Bodies, Gems, and Salmon». Journal of Cellular Biochemistry (70): 181-192. PMID 9671224. doi:10.1086/301992.
- ↑ Saunders WS, Cooke CA, Earnshaw WC (1991). «Compartmentalization within the nucleus: discovery of a novel subnuclear region.». Journal of Cellular Biology 115 (4): 919-931. doi:10.1083/jcb.115.4.919. PMID 1955462
- ↑ Pombo A, Cuello P, Schul W, Yoon J, Roeder R, Cook P, Murphy S (1998). «Regional and temporal specialization in the nucleus: a transcriptionally active nuclear domain rich in PTF, Oct1 and PIKA antigens associates with specific chromosomes early in the cell cycle». EMBO J 17 (6): 1768-1778. PMID 9501098. doi:10.1093/emboj/17.6.1768.
- ↑ a b Fox, Archa et al. (2002). «Paraspeckles:A Novel Nuclear Domain». Current Biology 12: 13-25. doi:10.1016/S0960-9822(01)00632-7. Archivado desde el original el 8 de diciembre de 2012. Consultado el 28 de julio de 2009.
- ↑ a b Fox, Archa; Wendy Bickmore (2004). «Nuclear Compartments: Paraspeckles». Nuclear Protein Database. Archivado desde el original el 2 de mayo de 2006. Consultado el 6 de marzo de 2007.
- ↑ a b Fox, A. et al. (2005). «P54nrb Forms a Heterodimer with PSP1 That Localizes to Paraspeckles in an RNA-dependent Manner». Molecular Biology of the Cell 16: 5304-5315. PMID 16148043. doi:10.1091/mbc.E05-06-0587. PMID 16148043
- ↑ Lamond AI, Spector DL (agosto de 2003). «Nuclear speckles: a model for nuclear organelles». Nat. Rev. Mol. Cell Biol. 4 (8): 605-12. PMID 12923522. doi:10.1038/nrm1172.
- ↑ Handwerger, Korie E.; Joseph G. Gall (enero de 2006). «Subnuclear organelles: new insights into form and function». TRENDS in Cell Biology 16 (1): 19-26. PMID 16325406. doi:10.1016/j.tcb.2005.11.005.
- ↑ a b Li, L; Roy K, Katyal S, Sun X, Bléoo S, Godbout R. (marzo de 2006). «Dynamic nature of cleavage bodies and their spatial relationship to DDX1 bodies, Cajal bodies, and gems». Mol Biol Cell 17 (3): 1126-40. PMID 16371507. doi:10.1091/mbc.E05-08-0768.
- ↑ Lehninger, Albert L.; David L. Nelson, Michael M. Cox. (2000). Lehninger principles of biochemistry (3rd edición). New York: Worth Publishers. ISBN 1-57259-931-6.
- ↑ Moreno F, Ahuatzi D, Riera A, Palomino CA, Herrero P. (2005). «Glucose sensing through the Hxk2-dependent signalling pathway.». Biochem Soc Trans 33 (1): 265-268. PMID 15667322. doi:10.1042/BST0330265. PMID 15667322
- ↑ Görlich, Dirk; Ulrike Kutay (1999). «Transport between the cell nucleus and the cytoplasm». Ann. Rev. Cell Dev. Biol. (15): 607-660. PMID 10611974. doi:10.1042/BST0330265.
- ↑ Nierhaus, Knud H.; Daniel N. Wilson (2004). Protein Synthesis and Ribosome Structure: Translating the Genome. Wiley-VCH. ISBN 3527306382.
- ↑ Nicolini, Claudio A. (1997). Genome Structure and Function: From Chromosomes Characterization to Genes Technology. Springer. ISBN 0792345657.
- ↑ Watson, JD; Baker TA, Bell SP, Gann A, Levine M, Losick R. (2004). «Ch9–10». Molecular Biology of the Gene (5th edición). Peason Benjamin Cummings; CSHL Press.
- ↑ Lippincott-Schwartz, Jennifer (7 de marzo de 2002). «Cell biology: Ripping up the nuclear envelope». Nature 416 (6876): 31-32. PMID 11882878. doi:10.1038/416031a.
- ↑ a b Boulikas T (1995). «Phosphorylation of transcription factors and control of the cell cycle». Crit Rev Eukaryot Gene Expr 5 (1): 1-77. PMID 7549180.
- ↑ Steen R, Collas P (2001). «Mistargeting of B-type lamins at the end of mitosis: implications on cell survival and regulation of lamins A/C expression». J Cell Biol 153 (3): 621-626. PMID 11331311. doi:10.1083/jcb.153.3.621.
- ↑ Skutelsky, E.; Danon D. (junio de 1970). «Comparative study of nuclear expulsion from the late erythroblast and cytokinesis». J Cell Biol (60(3)): 625-635. PMID 5422968. doi:10.1083/jcb.153.3.621.
- ↑ Torous, DK; Dertinger SD, Hall NE, Tometsko CR. (2000). «Enumeration of micronucleated reticulocytes in rat peripheral blood: a flow cytometric study». Mutat Res (465(1–2)): 91-99. PMID 10708974. doi:10.1083/jcb.153.3.621.
- ↑ Hutter, KJ; Stohr M. (1982). «Rapid detection of mutagen induced micronucleated erythrocytes by flow cytometry». Histochemistry (75(3)): 353-362. PMID 7141888. doi:10.1083/jcb.153.3.621.
- ↑ Zettler, LA; Sogin ML, Caron DA (1997). «Phylogenetic relationships between the Acantharea and the Polycystinea: A molecular perspective on Haeckel's Radiolaria». Proc Natl Acad Sci USA (94): 11411-11416. PMID 9326623. doi:10.1083/jcb.153.3.621.
- ↑ Horton, TR (2006). «The number of nuclei in basidiospores of 63 species of ectomycorrhizal Homobasidiomycetes». Mycologia (98(2)): 233-238. PMID 16894968. doi:10.1083/jcb.153.3.621.
- ↑ Adam RD (diciembre de 1991). «The biology of Giardia spp». Microbiol. Rev. 55 (4): 706-32. PMC 372844. PMID 1779932.
- ↑ McInnes, A; Rennick DM (1988). «Interleukin 4 induces cultured monocytes/macrophages to form giant multinucleated cells». J Exp Med (167): 598-611. PMID 3258008. doi:10.1083/jcb.153.3.621.
- ↑ Goldring, SR; Roelke MS, Petrison KK, Bhan AK (1987). «Human giant cell tumors of bone identification and characterization of cell types». J Clin Invest (79(2)): 483-491. PMID 3027126. doi:10.1083/jcb.153.3.621.
- ↑ Pennisi E. (2004). «Evolutionary biology. The birth of the nucleus». Science 305 (5685): 766-768. PMID 15297641. doi:10.1126/science.305.5685.766.
- ↑ Margulis, Lynn (1981). Symbiosis in Cell Evolution. San Francisco: W. H. Freeman and Company. pp. 206–227. ISBN 0-7167-1256-3.
- ↑ Lopez-Garcia P, Moreira D. (2006). «Selective forces for the origin of the eukaryotic nucleus». Bioessays 28 (5): 525-533. PMID 16615090. doi:10.1002/bies.20413.
- ↑ Hartman H, Fedorov A. (2002). «The origin of the eukaryotic cell: a genomic investigation». Proc Natl Acad Sci U S A. 99 (3): 1420-1425. PMID 11805300. doi:10.1073/pnas.032658599.
- ↑ Bell PJ. (2001). "Viral eukaryogenesis: was the ancestor of the nucleus a complex DNA virus?" J Mol Biol Sep;53(3):251–256. PMID 11523012
- ↑ Takemura M. (2001). Poxviruses and the origin of the eukaryotic nucleus. J Mol Evol 52(5):419–425. PMID 11443345
- ↑ Villarreal L, DeFilippis V (2000). «A hypothesis for DNA viruses as the origin of eukaryotic replication proteins». J Virol 74 (15): 7079-7084. PMID 10888648. doi:10.1128/JVI.74.15.7079-7084.2000.
- ↑ Bell PJ (7 de noviembre de 2006). «Sex and the eukaryotic cell cycle is consistent with a viral ancestry for the eukaryotic nucleus». J Theor Biol 243 (1): 54-63. PMID 16846615.
- ↑ Fuerst JA. (2005). «Intracellular compartmentation in planctomycetes». Annu Rev Microbiol. 59: 299-328. PMID 15910279. doi:10.1146/annurev.micro.59.030804.121258.
- ↑ de Roos AD (2006). «The origin of the eukaryotic cell based on conservation of existing interfaces». Artif Life 12 (4): 513-523. PMID 16953783. doi:10.1162/artl.2006.12.4.513.
Enlaces externos
editar- Wikimedia Commons alberga una categoría multimedia sobre Núcleo celular.
- Hipertextos de biología: El núcleo celular.