Proceso isobárico
Un proceso isobárico es un proceso termodinámico en el que la presión se mantiene constante: ΔP = 0. El calor transferido al sistema realiza trabajo, pero también cambia la energía interna del sistema. Este artículo utiliza la convención de signos de física para el trabajo, donde el trabajo positivo es el trabajo realizado por el sistema. Usando esta convención, por la primera ley de la termodinámica,
donde W es trabajo, U es energía interna y Q es calor.[1] El trabajo de presión-volumen por el sistema cerrado se define como:
donde Δ significa cambio en todo el proceso, mientras que d denota un diferencial. Dado que la presión es constante, esto significa que
Aplicando la ley de los gases ideales, esto se convierte en
Suponiendo que la cantidad de gas permanece constante, por ejemplo, no hay transición de fase durante una reacción química. Según el teorema de equipartición,[2] el cambio en la energía interna está relacionado con la temperatura del sistema por
donde cV, m es la capacidad calorífica molar a volumen constante.
La sustitución de las dos últimas ecuaciones en la primera ecuación produce:
donde cP es la capacidad calorífica molar a presión constante.
Capacidad calorífica específica
editarPara encontrar la capacidad calorífica específica molar del gas involucrado se aplican las siguientes ecuaciones para cualquier gas general que sea calóricamente perfecto. La propiedad γ se denomina índice adiabático o relación de capacidad calorífica. Algunas fuentes publicadas pueden usar k en lugar de γ.
Calor específico isocórico molar:
Calor específico isobárico molar:
Los valores de γ son γ = 7 para gases diatómicos como aire y sus componentes principales, y γ = 5 para los gases monoatómicos tales como los gases nobles. Las fórmulas para calores específicos reducirían en estos casos especiales:
- y
Diatómico:
- y
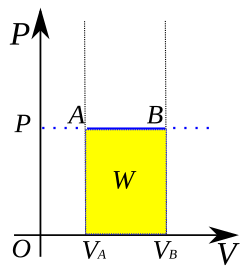
Un proceso isobárico se muestra en un diagrama P - V como una línea horizontal recta, que conecta los estados termostáticos inicial y final. Si el proceso se mueve hacia la derecha, entonces es una expansión. Si el proceso se mueve hacia la izquierda, entonces es una compresión.
Convención de signos para el trabajo
editarLa motivación de las convenciones de signos específicos de la termodinámica proviene del desarrollo temprano de los motores térmicos. Al diseñar un motor térmico, el objetivo es que el sistema produzca y entregue el rendimiento del trabajo. La fuente de energía en un motor térmico es un aporte de calor.
- Si el volumen se comprime (ΔV = volumen final - volumen inicial < 0), luego W < 0. Es decir, durante la compresión isobárica, el gas realiza un trabajo negativo o el medio ambiente realiza un trabajo positivo. Reiterado, el medio ambiente hace un trabajo positivo sobre el gas.
- Si el volumen se expande (ΔV = volumen final - volumen inicial> 0), luego W > 0. Es decir, durante la expansión isobárica, el gas realiza un trabajo positivo o, de manera equivalente, el entorno realiza un trabajo negativo. Reiterado, el gas hace un trabajo positivo sobre el medio ambiente.
- Si se agrega calor al sistema, entonces Q > 0. Es decir, durante la expansión/calentamiento isobárico, se agrega calor positivo al gas o, de manera equivalente, el ambiente recibe calor negativo. Reiterado, el gas recibe calor positivo del ambiente.
- Si el sistema rechaza el calor, entonces Q < 0. Es decir, durante la compresión/enfriamiento isobárico, se agrega calor negativo al gas o, de manera equivalente, el ambiente recibe calor positivo. Reiterado, el ambiente recibe calor positivo del gas.
Definición de entalpía
editarUn proceso isocórico se describe mediante la ecuación Q = ΔU. Sería conveniente tener una ecuación similar para los procesos isobáricos. Sustituyendo la segunda ecuación en la primera se obtiene
La cantidad U + pV es una función de estado, por lo que se le puede dar un nombre. Se llama entalpía y se denota como H. Por lo tanto, un proceso isobárico puede describirse más sucintamente como
La entalpía y la capacidad calorífica específica isocórica son construcciones matemáticas de gran utilidad, ya que al analizar un proceso en un sistema abierto, la situación de trabajo cero ocurre cuando el fluido fluye a presión constante. En un sistema abierto, la entalpía es la cantidad que es útil utilizar para realizar un seguimiento del contenido de energía del fluido.
Ejemplos de procesos isobáricos
editarLa expansión reversible de un gas ideal se puede utilizar como ejemplo de un proceso isobárico.[3] De particular interés es la forma en que el calor se convierte en trabajo cuando la expansión se lleva a cabo a diferentes presiones de gas de trabajo / gas circundante.
En el primer ejemplo de proceso, una cámara cilíndrica de 1 m² de área encierra 81.2438 mol de un gas diatómico ideal de masa molecular 29 g mol-1 a 300 K. El gas circundante está a 1 atm y 300 K, y está separado del gas del cilindro por un pistón delgado. Para el caso límite de un pistón sin masa, el gas del cilindro también está a 1 atm de presión, con un volumen inicial de 2 m³. Se agrega calor lentamente hasta que la temperatura del gas es uniformemente de 600 K, después de lo cual el volumen de gas es de 4 m³ y el pistón está 2 m por encima de su posición inicial. Si el movimiento del pistón es suficientemente lento, la presión del gas en cada instante tendrá prácticamente el mismo valor (psis = 1 atm) en todo momento.
Para un gas diatómico térmicamente perfecto, la capacidad de calor específico molar a presión constante (cp) es 7/2 o 29,1006 J mol -1 ° -1. La capacidad calorífica molar a volumen constante (c v) es 5/2 o 20,7862 J mol -1 ° -1. El radio de las dos capacidades caloríficas es 1,4.[4]
El calor Q requerido para llevar el gas de 300 a 600 K es
El aumento de la energía interna es
Por lo tanto,
también
, que por supuesto es idéntica a la diferencia entre ΔH y ΔU.
Aquí, el trabajo se consume enteramente por la expansión contra el entorno. Del calor total aplicado (709,3 kJ), el trabajo realizado (202,7 kJ) es aproximadamente el 28,6% del calor suministrado.
El segundo ejemplo de proceso es similar al primero, excepto que el pistón sin masa se reemplaza por uno que tiene una masa de 10,332.2 kg, que duplica la presión del cilindro de gas a 2 atm. El volumen de gas del cilindro es entonces de 1 m³ a la temperatura inicial de 300 K. Se agrega calor lentamente hasta que la temperatura del gas es uniformemente de 600 K, después de lo cual el volumen de gas es de 2 m³ y el pistón está 1 m por encima de su posición inicial. Si el movimiento del pistón es lo suficientemente lento, la presión del gas en cada instante tendrá prácticamente el mismo valor (p sis = 2 atm) en todo momento.
Dado que la entalpía y la energía interna son independientes de la presión,
- y
Como en el primer ejemplo, aproximadamente el 28,6% del calor suministrado se convierte en trabajo. Pero aquí, el trabajo se aplica de dos formas diferentes: en parte expandiendo la atmósfera circundante y en parte levantando 10,332.2 kg una distancia h de 1 m.[5]
Así, la mitad del trabajo levanta la masa del pistón (trabajo de gravedad o trabajo "utilizable"), mientras que la otra mitad expande el entorno.
Los resultados de estos dos ejemplos de procesos ilustran la diferencia entre la fracción de calor convertida en trabajo utilizable (mg Δ h) frente a la fracción convertida en trabajo de presión-volumen realizado contra la atmósfera circundante. El trabajo útil se acerca a cero cuando la presión del gas de trabajo se acerca a la del entorno, mientras que el trabajo útil máximo se obtiene cuando no hay presión de gas circundante. La relación entre todo el trabajo realizado y la entrada de calor para la expansión del gas isobárico ideal es
Densidad variable
editarUna cantidad dada (masa m) de gas en un volumen cambiante produce un cambio en la densidad ρ. En este contexto se escribe la ley de los gases ideales
donde T es la temperatura termodinámica y M es la masa molar. Cuando R y M se toman como constantes, la presión P puede permanecer constante mientras el cuadrante densidad-temperatura (ρ,T) somete a un mapeo de compresión.[6]
Etimología
editarEl adjetivo "isobárico" se deriva de las palabras griegas ἴσος (isos) que significa "igual", y βάρος (baros) que significa "peso".
Véase también
editarReferencias
editar- ↑ «First Law of Thermodynamics». www.grc.nasa.gov. Consultado el 19 de octubre de 2017.
- ↑ Eyland, Peter. «Lecture 9 (Equipartition Theory)». www.insula.com.au.
- ↑ Gaskell, David R., 1940- (2008). Introduction to the thermodynamics of materials (5th ed edición). New York: Taylor & Francis. p. 32. ISBN 978-1-59169-043-6. OCLC 191024055.
- ↑ «Heat Capacity of Ideal Gases». ccrma.stanford.edu. Consultado el 5 de octubre de 2018.
- ↑ DeVoe, Howard. (2001). Thermodynamics and chemistry. Upper Saddle River, NJ: Prentice Hall. p. 58. ISBN 0-02-328741-1. OCLC 45172758.
- ↑ Olver, Peter J. (1999). Classical invariant theory. Cambridge, UK: Cambridge University Press. p. 217. ISBN 978-1-107-36236-9. OCLC 831669750.





