Reactivo de Edman
La degradación de Edman, desarrollada por Pehr Edman en la década de 1950, es un método de secuenciación de aminoácidos en un péptido. En este método se derivatiza y separa el residuo amino-terminal, lo que permite identificar su naturaleza y obtener el siguiente con el grupo amino libre, para continuar con el siguiente ciclo de reacción. Cada residuo es consecutivamente aislado y derivatizado sin afectar a los enlaces peptídicos entre los otros residuos. Para esta secuenciación se requiere el reactivo de Edman, también denominado fenilisotiocianato o PITC.[2]
| Fenilisotiocianato | ||
|---|---|---|
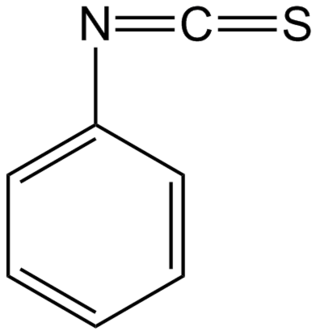 | ||
| General | ||
| Otros nombres | Isotiocianatobenceno / Reactivo de Edman / PITC | |
| Fórmula molecular | C7H5NS | |
| Identificadores | ||
| Número CAS | 103-72-0[1] | |
| Propiedades físicas | ||
| Apariencia | líquido transparente, entre incoloro y amarillo pálido. | |
| Densidad | 1130 kg/m³; 1,13 g/cm³ | |
| Masa molar | 13 519 g/mol | |
| Punto de fusión | −21 °C (252 K) | |
| Punto de ebullición | 218 °C (491 K) | |
| Presión de vapor | 0,17 mm Hg | |
| Propiedades químicas | ||
| Solubilidad en agua | Insoluble | |
| Familia | Aminas primarias | |
| Peligrosidad | ||
| SGA |
 | |
| Punto de inflamabilidad | 361 K (88 °C) | |
| NFPA 704 |
2
3
0
| |
| Frases R |
R23 R24 R25 R34 R42 R43 R63 | |
| Frases S | S23 S26 S28 S36 S37 S39 S38 S45 | |
| Frases H |
H301 H314 H317 H334 | |
| Frases P | P261 P272 P280 P303 P304 P305 P310 P338 P340 P351 P353 P361 | |
| Riesgos | ||
| Piel | Se absorbe muy fácilmente por la piel y las mucosas. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Mecanismo
editarEn 1950, Pehr Victor Edman describió un método para poder llevar a cabo la secuenciación de péptidos por medio del uso de fenilisotiocianato (PITC por sus siglas en inglés).[3] El reactivo de Edman (fenilisotiocianato o PITC) reacciona con el aminoácido del extremo N-terminal de un polipéptido en condiciones alcalinas para la formación de feniltricarbamilo (PITC), el producto obtenido se trata con TFA lo cual corta el residuo N-terminal y genera un derivado de tiazolinona ,se utiliza un solvente orgánico para convertir la tiazolinona-aminoácido al derivado de feniltiohidantoina (PTH) para después ser identificado por métodos cromatográficos. El método de secuenciación por degradación de Edman es utilizado en péptidos de 10 a 50 residuos de aminoácidos. Sin embargo, si se utiliza para la secuenciación de proteínas mayores a 50 residuos de aminoácidos, la degradación ya no es eficaz por lo que la proteína se debe de fraccionar en segmentos más pequeños para que se pueda llevar a cabo.
La reacción química de Edman es un proceso cíclico que consta de tres pasos.
- El reactivo de Edman o fenilisotiocianato (PITC) se acopla al grupo amino N-terminal libre.
- El residuo N-terminal se corta mediante el uso de ácido, dejando intacta el resto de la cadena peptídica con un nuevo extremo N-terminal susceptible de iniciar un segundo ciclo.
- El derivado aminoacídico (anilinotiazolinona) formado a partir del aminoácido cortado es inestable y por ello, se introduce en medio ácido para convertirse en el derivado PTH (feniltiohidantoina) estable. El resto de la cadena polipeptídica se somete a nuevos ciclos de degradación de Edman para obtener la secuencia de aminoácidos del resto de la proteína.[4]
Actualmente, el análisis de cada uno de los aminoácidos separados del péptido inicial puede realizarse mediante cromatografías HPLC/MS[5] (cromatografía líquida de alta resolución acoplada a la espectrometría de masas) de fase inversa por hidrofobicidad (se comparan los tiempos de retención de los diferentes aminoácidos cortados con una muestra patrón), por espectrometría de masas MALDI-TOF, o por análisis de aminoácidos.[6]
No es posible secuenciar péptidos cuyo extremo N-terminal se encuentre bloqueado (grupo amino acetilado, formilado, etc). Alrededor del 50% de las proteínas tienen el extremo amino bloqueado, bien por naturaleza o por su preparación, en tampones con sustancias susceptibles de reaccionar con este: (cianato, ácido acrílico, acetilo, aldehído...). Otra limitación de la degradación de Edman es que el rendimiento no es del 100% y por tanto cuando ya se llevan hechos muchos ciclos (más de 50 aminoácidos analizados) se obtienen errores.
Referencias
editar- ↑ Número CAS
- ↑ https://www.sigmaaldrich.com/ES/es/sds/aldrich/139742. Consultado el 23 de mayo de 2023.
- ↑ «https://febs.onlinelibrary.wiley.com/doi/epdf/10.1111/j.1432-1033.1967.tb00047.x». Consultado el 15 de marzo de 2023.
- ↑ «http://actachemscand.org/pdf/acta_vol_04_p0283-0293.pdf». Consultado el 15 de marzo de 2023.
- ↑ «https://www.cib.csic.es/sites/default/files/inline-files/Generalidades.pdf». Consultado el 31 de marzo de 2023.
- ↑ «https://digital.csic.es/bitstream/10261/23028/4/Granados_Carmen_4.pdf». Consultado el 30 de marzo de 2023.



