Sinaptobrevina
La sinaptobrevina (isoformas de sinaptobrevina 1-2) es una pequeña proteína integral de membrana de vesículas secretoras con un peso molecular de 18 kilodalton (kDa) y un punto isoeléctrico de aproximadamente 6,6 que forma parte de la familia de las proteínas de membrana asociadas a vesículas (VAMP). Son, concretamente, VAMP1 y VAMP2.
La Sinaptobrevina es una de las proteínas SNARE, en inglés “SNAP (Soluble NSF Attachment Protein) REceptor”, más concretamente V-SNARE, que actúan como proteínas transmembrana de las vesículas de transporte, en este caso sinápticas y participan en la exocitosis sináptica (liberación de neurotransmisores).[1] La encontramos en pequeñas vesículas sinápticas del cerebro de los mamíferos.
En las neuronas, dichas vesículas son liberadas en el retículo endoplasmático y más tarde se incorporan al ciclo vesicular sináptico donde son reusadas en posteriores sinapsis.
| Sinaptobrevina | ||
|---|---|---|
 | ||
| General | ||
| Otros nombres | VAMP1, VAMP2 | |
| Propiedades físicas | ||
| Peso | 18 kilodalton (2,88e-29 kg) | |
| Propiedades químicas | ||
| Punto isoeléctrico | 6,6 | |
| Referencias | ||
| Símbolo | Sinaptobrevina | |
| Pfam | PF00957 | |
| InterPro | IPR001388 | |
| PRO SITE | PDOC00368 | |
| SCOP | 1sfc | |
| SUPER FAMILY | 1sfc | |
| OPM superfamily | 218 | |
| OPM protein | 3hdt | |
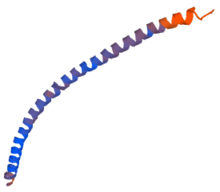 | ||
Estructura
editarLa sinaptobrevina consiste en una hélice alfa que se expande desde el C-terminal hasta dos terceras partes de la región citoplastmática; éstas, junto con otras tres hélices forman la estructura cristalina del complejo principal muy estable, el complejo de SNARE. Este está formado por cuatro hélices alfa; una de sinaptobrevina, otra de sintaxina, y dos de SNAP-25. La sinaptobrevina aislada en solución está prácticamente desplegada pero para disociar este complejo se necesita una solución de Dodecilsulfato sódico (SDS) en ebullición. Esta proteína tiene una hélice TM C-terminal y es capaz de interaccionar con el C-Terminal de la sintaxina del complejo pero solamente unos pocos residuos se unen a la región citoplasmática de larga duración de la sintaxina.[2] La proteína de la vesícula sináptica sinaptobrevina se acopla con la sintaxina y la SNAP-25 para formar el complejo SNARE. En el motivo SNARE de la sinaptobrevina se forma una hélice de 55 residuos con dos hélices formadas por los segmentos N-terminal y C-terminal de SNAP-25; pero su forma es inestructurada antes de la fusión de membranas en la exocitosis neuronal. Como la sinaptobrevina está fijada en la membrana de la vesícula y la sintaxina y SNAP-25 están fijadas en la membrana diana, este complejo central une con firmeza entre sí las dos membranas.
[3]
Las cuatro Hélices del complejo las encontramos unas alrededor de otras con una torsión suave hacia la izquierda. La secuencia de cada hélice en su mayor parte tiene la repetición de siete residuos normal (a-b-c-d-e-f-g), con los residuos a y d hidrófobos (característica propia de los haces de 4 y 3 hélices). Sin embargo, la capa central de las cadenas laterales a lo largo de la extensión del haz de cuatro hélices presenta un residuo arginina de la sinaptobrevina que está unido por un puente de hidrógeno a tres cadenas glutamina, una de la sintaxina y una de cada una de las hélices de SNAP-25. Estos residuos polares muy conservados están separados del medio acuoso de modo que sus interacciones se facilitan por la baja constante dieléctrica de su medio. Estas interacciones sirven para llevar a estas cuatro hélices a su registro correcto.
[2] En estudios realizados utilizando RMN (resonancia magnética nuclear) los datos obtenidos al investigar sobre la longitud completa de la sinaptobrevina en las micelas dodecilfosfocolina (DPC), elemento útil como modelo de los sistemas de membrana en solución para RMN que en solución amfipática tiende a formar micelas, se revelan dos segmentos helicoidales transitorios flanqueados por regiones desordenadas y un tercio de hélice más estable. La hélice transitoria I comprende la parte N-terminal del complejo SNARE, la hélice transitoria II extiende el complejo SNARE en la región yuxtamembrana y la hélice III, la más estable, forma el dominio transmembrana. Estas hélices pueden tener importantes consecuencias en el plegamiento y fusión del complejo SNARE: La hélice I es propensa a formar un punto de nucleación, un C-terminal alterado en el complejo puede actuar como señal de detención de plegado. La hélice II, por otro lado, empareja la fusión y el plegamiento del complejo.
[4] Mientras que hay elementos que la forman que no son estrictamente necesarios, existen unos requisitos estructurales para que la sinaptobrevina siga realizando su función exocitótica. Estudios realizados comprueban que la sustitución de glutamina por arginina en la capa cero del complejo SNARE no afecta significativamente a la exocitosis dependiente de sinaptobrevina. Si que encontramos, en cambio, que la inserción de 12 o 24 residuos entre el complejo SNARE y la región transmembrana anula la capacidad de la sinaptobrevina para mediar con el Ca2+.
Aun y así la sinaptobrevina con el residuo 12 pero sin la inserción del residuo 24 restaura la liberación espontánea en las neuronas con deficiencia de la proteína. Se sugiere que la sinaptobrevina media con el ion calcio produciendo una exocitosis disparada por un estrecho acoplamiento del complejo SNARE con la región transmembrana, forzando entonces las membranas hacia una estrecha proximidad para la fusión. Por otra parte las reacciones de fusión y liberación espontáneas difieren de manera mecánica.
Función
editarLas proteínas SNARE (sinaptobrevina, sintaxina y SNAP-25) son componentes clave de la maquinaria molecular que actúa en la fusión de membranas en la exocitosis.[5] Se ha comprobado que se encuentran en las terminaciones nerviosas, concentradas en las membranas de las pequeñas vesículas sinápticas porque intervienen en la liberación de neurotransmisores (concretamente entre la fase de acoplamiento molecular (docking) y la fusión) y el reciclado de estas vesículas sinápticas. También pueden estar implicadas en la regulación del flujo de la membrana en terminales nerviosos. En este proceso de regulación de flujo interactúan con proteínas de unión a GTP de bajo peso molecular (Rab).
También actúan en la transmisión sináptica. En este proceso, las vesículas están destinadas a unirse a zonas activas presinápticas mediante la asociación de sinaptobrevina (v-SNARE), que cumple la misión de facilitar la identificación del lugar donde se va a producir la fusión de membranas, con sintaxina (t-SNARE), que se encuentra en la membrana diana (diana = target, de ahí la t de t-SNARE), que es la membrana a la cual se dirige la vesícula. Una vesícula puede inspeccionar muchas membranas potencialmente diana antes de que su v-SNARE encuentre una t-SNARE complementaria. Para completar el proceso de unión, las proteínas Rab, controlan que la interacción entre v-SNARE y t-SNARE sea correcta. Estas proteínas Rab se encuentran en la superficie de la vesícula donadora. Cuando la vesícula ha encontrado su membrana diana, la unión de v-SNARE y t-SNARE permite que la vesícula se mantenga unida durante el tiempo necesario para que la proteína Rab hidrolice el GTP que lleva unido. Esto ancla aún más la vesícula a la membrana, que ya estará lista para la fusión.[6] La sinaptobrevina y la sintaxina se anclan a las membranas por unos pocos aminoácidos que no llegan a atravesar completamente la bicapa lipídica.
En un principio se pensaba que la falta de cualquiera de estas dos proteínas bloqueaba completamente la transmisión sináptica. Ahora se ha demostrado que, aun habiendo ausencia de sinaptobrevina, las vesículas entran en contacto con la membrana presináptica y se unen de manera normal al sitio indicado para la exocitosis. Estas vesículas están maduras y son funcionales y persisten en el intento de fusionarse con la membrana. Por otro lado, a falta de sintaxina, la fusión con la membrana la desencadenan soluciones salinas hiperosmóticas. Por lo tanto, no podemos decir que conocemos al completo la función de la sinaptobrevina, es decir, estamos tratando una hipótesis. Lo que sí podemos decir es que tiene un papel diferente a la sintaxina.
La liberación de neurotransmisores a través de exocitosis de vesículas sinápticas está regulada por una secuencia de interacciones proteína-proteína que se están empezando a caracterizar en términos estructurales. Se cree que los homólogos de sinaptobrevina, sintaxina y SNAP-25 participan en todos los tipos de tráfico de membrana intercelular. Estas tres proteínas que forman el complejo SNARE, conocido también como Núcleo, proporcionan la fuerza motriz para la fusión de membranas.
Clasificación
editar[7] Inicialmente las proteínas SNARE se clasificaron siguiendo la nomenclatura V/T, es decir "v-SNAREs" donde se incluyen pretinas homólogas a la synaptobrevina y "t-SNAREs" incluyendo proteínas homólogas a la syntaxina-1 y la SNAP-25, basándose en si se encontraban en la vesícula (v) o en la membrana diana ("target", t). Sin embargo, esta nomenclatura se consideró poco exacta, por lo que se propuso la clasificación Q/R. En la nomenclatura Q/R, se casifican las SNARE se denominan R-SNARE si proporcionan arginina (R) o Q-SNARE si proporcionan glutamina (Q). Las VAMP/familia de las sinaptobrevinas, son clasificadas como R-SNARE,debido a la presencia de la arginina en una posición específica en la primera secuencia de la proteína.
Relevancia clínica
editarLa sinaptobrevina puede ser degradada por la tetanoespasmina, una proteína derivada de la bacteria Clostridium tetani, que es la causante del tétanos.
Una bacteria similar, la Clostridium botulinum produce una toxina que hidroliza la sinaptobrevina causando una enfermedad denominada botulismo.
La cadena H de la toxina se une a receptores en la membrana presináptica, a continuación penetra por un mecanismo activo y una vez se encuentra en el interior de la célula interviene en la liberación de la acetilcolina (neurotransmisor), imprescindible para la excitación del músculo. La toxina impide esta liberación actuando como peptidasa de proteínas que forman la vesícula sináptica encargadas de la exocitosis, entre ellas la sinaptobrevina: el fragmento A de la toxina divide la sinaptobrevina, impidiendo que se produzca la exocitosis del neurotransmisor acetilcolina y bloqueado el impulso nervioso, produciendo así síntomas como parálisis muscular o incluso el fallecimiento del individuo afectado.[8] La sinaptobrevina no sólo puede verse involucrada en enfermedades producidas por patógenos externos, sino que está involucrada en la Miastenia gravis. Esta es una enfermedad autoinmune neuromuscular y crónica. También está producida por el impedimento de la transmisión del neurotransmisor acetilcolina, encargada de la contracción muscular, esta vez por culpa los anticuerpos. Estos bloquean, alteran o destruyen la sinaptobrevina y por tanto la acetilcolina no se transmite.[9] Pese a que las proteínas SNARE se consideran componentes centrales de las reacciones de fusión de membranas su función exacta aún no se conoce con exactitud. Hasta ahora se barajaban hipótesis como: mediadoras de especificidad de la fusión, catalizadores de la fusión o simplemente ejecutoras de la fusión. Para concretar e investigar sobre cual era exactamente, se llevó a cabo experimentos en los que se extraía la sinaptobrevina (knockout) en ratones, concretamente VAMP2. En ausencia de esta proteína, tanto la fusión espontánea de vesículas como la fusión inducida por sacarosa hipertónica se redujeron en una décima parte y la fusión desencadenada por Calcio (Ca2+) se vio reducida en una centésima parte. Por lo tanto, se describió que la sinaptobrevina 2 tiene la función de canalizar las reacciones en el proceso de fusión y estabilizar los intermediarios durante el proceso, pero no es estrictamente necesaria para que la fusión se produzca.
Bibliografía
editarReferencias
editar- ↑ TC, Südhof; M, Baumert; MS, Perin; R, Jahn (1982). «A synaptic vesicle membrane protein is conserved from mammals to Drosophila». Howard Hughes Medical Institute, University of Texas Southwestern Medical Center, Dallas 2 (5): 1475-1481. PMID 2560644.
- ↑ a b Ellena, Jeffrey F.; Liang, Binyong; Wiktorb, Maciej; Steind, Alexander; Cafisoe, David S.; Tammb, Lukas K. (27 de julio de 2009). Dynamic structure of lipid-bound synaptobrevin suggests a nucleation-propagation mechanism for trans-SNARE complex formation 106 (48). pp. 20306-20311. Consultado el 17 de octubre de 2015.
- ↑ Voet, Donald. Bioquímica. Editorial Médica Panamericana. ISBN 9788428209069.
- ↑ Deák, Ferenc; Shin, Ok Ho; Kavalali, Ege T.; Südhof, Thomas C. (21 de junio de 2006). «Structural determinants of synaptobrevin 2 function in synaptic vesicle fusion». The journal of neuroscience: 6668-6676.
- ↑ Arcario, MJ; Blanchard, AE; Schulten, K; Tajkhorshid, E. A highly tilted membrane configuration for the prefusion state of synaptobrevin.. PMID 25418096. doi:10.1016/j.bpj.2014.09.013.
- ↑ Latorre, Ramon; Lopez-Barneo, Jose; Bezanilla, Francisco; Llinàs (edits.), Rodolfo (1996). «Biofísica y fisiologia celular». Universidad de Sevilla.
- ↑ Fasshauer, Dirk; Sutton, R. Bryan; Brunger, Axel T.; Jahn, Reinhard (22 Decembre 1998). «Conserved structural features of the synaptic fusion complex: SNARE proteins reclassified as Q- and R-SNAREs». Proceedings of National Academy of Science of the U S A: 15781-15786.
- ↑ «Miastenia gravis». National Institute of Neurological Disorders and Stroke.
- ↑ Mozhayeva, Marina; Königstorfer, Andreas; Deák, Ferenc; Schoch, Susanne; Sara, Yildirim; Südhof, Thomas C.; Kavalali, Ege T. (2 de noviembre de 2001). «SNARE Function Analyzed in Synaptobrevin/VAMP Knockout Mice». SCIENCE 294: 1117. Consultado el 27 de octubre de 2015.