Benzofurano
El Benzofurano o más específicamente, 1-benzofurano o Benzo[b]furano, es un compuesto orgánico heterocíclico aromático de cinco miembros con un átomo de oxígeno fusionado un anillo de benceno. Es un líquido incoloro, oleoso y de olor dulce, inmiscible en agua pero soluble en benceno, éter y alcohol. El benzofurano es un análogo del indol.
| Benzofurano | ||
|---|---|---|
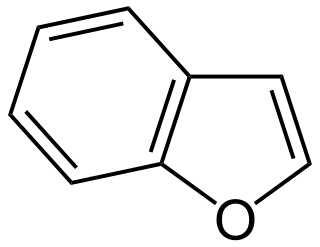 | ||
| Nombre IUPAC | ||
| 2,3-Benzofurano | ||
| General | ||
| Otros nombres | benzofurano, cumarona | |
| Fórmula semidesarrollada | C8H6O | |
| Fórmula estructural |
 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | [271-89-6][1] | |
| ChEBI | 35260 | |
| ChEMBL | CHEMBL363614 | |
| ChemSpider | 8868 | |
| DrugBank | DB04179 | |
| PubChem | 9223 | |
| UNII | LK6946W774 | |
| KEGG | C14512 | |
| Propiedades físicas | ||
| Apariencia | incoloro | |
| Densidad | 1090 kg/m³; 1,09 g/cm³ | |
| Masa molar | 1181 g/mol | |
| Punto de fusión | 255 K (−18 °C) | |
| Punto de ebullición | 447 K (174 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 0 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Producción y síntesis
editarEl benzofurano es extraído del carbón de hulla y se produce sobre todo durante la transformación del carbón en aceite mineral, aunque también se puede producir en otros usos del carbón o del petróleo. También se puede obtener de la deshidrogenación del 2-etilfenol.
El benzofurano puede ser preparado por O-alquilación del salicilaldehído con ácido cloroacético seguido por deshidratación del éter resultante.
Si no se emplea el ácido y el anhídrido al final, el método se denomina síntesis de Rap-Stoermer.
Existe otro método denominado Transposición de Perkin, en donde se utiliza una 3-halocumarina que se trata con un hidróxido alcalino:
- Por reacción de Diels–Alder de un furano nitrovinílico con dienófilos:[2]
- Heterociclización de un orto-alquinilfenol:[3]
Reactividad
editarLa sustitución electrofílica de estos sistemas es mucho menos regioselectiva que la del indol (el cual presenta selectividad principal en C-3), incluso en la medida en que las posiciones de anillo heterocíclico son sólo un poco más reactivas que algunas de las posiciones del anillo de benceno. El benzofurano muestra una tendencia menor a la sustitución de 3.
La nitración con mezcla acetonítrica (ácido nítrico/ácido acético) produce 2-nitrobenzofurano, aunque en todos los estudios en los que se describe el aislamiento de un producto principal,[4] particularmente aquellos realizados antes el advenimiento de técnicas analíticas modernas, se debe considerar que la presencia de otros isómeros de menor proporción no fueron caracterizados. Un estudio posterior con tetróxido de dinitrógeno encontró que se formaba también 3-nitrobenzofurano como un producto principal junto con un porcentaje menor del isómero.[5]
El tratamiento del benzofurano con halógenos da como resultado los productos de adición 2,3; a partir de este producto de adición, mediante la eliminación de haluro de hidrógeno promovido con base, se pueden obtener 2- y 3-monohalobenzofuranos con altos rendimientos.
La yodación del benzofurano se realiza con yodo molecular en presencia de una base fuerte, como un alquil litio:
La formilación del benzofurano sólo forma el derivado 2-formilado, el 1-benzofurano-2-carbaldehído.
La reacción de Friedel-Crafts es difícil para los benzofuranos heterosustituidos en el anillo porque los catalizadores típicos tienden a causar resinificación, pero las acilaciones en 3 se han obtenido usando cloruro férrico como catalizador.
Métodos de análisis
editarEl medio ambiente o sustancias biológicas que contienen benzofurano también contienen otros compuestos orgánicos con propiedades físicas y químicas similares. En muchos casos la espectroscopia infrarroja de la transformada de Fourier (FT-IR), es un buen método para identificar y caracterizar las funcionalidades de una molécula de resina. Para muchas resinas de hidrocarburos en las que hay numerosas estructuras, la resonancia magnética nuclear (NMR) se usa para cuantificar la aromaticidad que contiene la resina. La FT-IR, la cromatografía de gases (GC) y la NMR se usan para identificar y cuantificar funcionalidades particulares de los monómeros presentes en la resina.
Aplicaciones
editarEl benzofurano no tiene usos comerciales, pero la porción del petróleo que contiene el benzofurano, concretamente el 2,3-benzofurano, se utiliza para fabricar un plástico llamado resina de cumarona-indeno que está hecha por medio de polimerización de 1 o más compuestos de un tipo representado por cumarona, indeno, sus homólogos y derivados. Se usa en envases de alimentos, en la fabricación de pinturas y barnices resistentes a la corrosión y al agua y, como plastificante en cauchos sintéticos. Las resinas de hidrocarburos son muy usadas como modificadoras en adhesivos, pinturas y barnices, plásticos,etc. En muchos casos están mezcladas con elástomeros, plásticos, ceras o aceites. La selección de una resina para una aplicación particular depende de la composición, peso molecular, color, y también del precio. Raramente se usan solas. Las resinas de cumareno-indeno y las resina aromáticas de estireno modificado representan entre el 20-30% de la porción de cemento que se usa en la producción de asfalto.
Presencia en la naturaleza
editarEl núcleo de benzofurano se encuentra en una amplia gama de productos naturales derivados de plantas y microorganismos, que varían en complejidad desde el 5-metoxibenzofurano, hasta las auronas, un grupo de pigmentos vegetales isoméricos con los flavonoides.
Efectos sobre la salud
editarEl benzofurano se encontró en el aire y en el agua cerca de fábricas procesadoras de combustible. Puede entrar en el cuerpo por medio de los alimentos, del agua o por exposición aérea (inhalación). Los efectos sobre la salud dependen de la cantidad de benzofurano que haya en el cuerpo. Aunque no se hicieron estudios para evaluar sus efectos en los humanos, estudios realizados en animales mostraron que el benzofurano puede dañar los sistemas hepáticos, respiratorios, cardiovasculares, ... e incluso llegar a ser mortal en períodos no muy largos de exposición.
Efectos sobre el medio ambiente
editarLa información que hay es insuficiente para predecir los efectos del benzofurano sobre el medio ambiente. El benzofurano puede liberarse al medio ambiente en la producción de coque, de envases y en la gasificación del carbón. Debido a su alto punto de ebullición(174 °C) su volatilización es lenta y su potencial es moderado ya que es bioconcentrado por organismos acuáticos. Los niveles de benzofurano en el medio ambiente no son cuantitativos aunque se sabe que está presente en el aire, agua y suelo de algunas zonas. Una vez que el benzofurano está introducido en el medio ambiente, actúa sobre los organismos vivos y produce en ellos efectos adversos que dependen de la concentración y del tiempo de exposición.
Referencias
editar- ↑ [271-89-6 Número CAS]
- ↑ Kusurkar, R. S.; Bhosale, D. K. (1990). «Novel Synthesis of Benzosubstituted Benzofurans Via Diels-Alder Reaction». Synthetic Communications 20 (1): 101-109. doi:10.1080/00397919008054620. Consultado el 11 de febrero de 2014.
- ↑ Fürstner, Alois & Davies, Paul (2005). «Heterocycles by PtCl2-Catalyzed Intramolecular Carboalkoxylation or Carboamination of Alkynes». Journal of the American Chemical Society 127 (43): 15024-15025. doi:10.1021/ja055659p. Consultado el 11 de febrero de 2014.
- ↑ Stoermer, R. and Richter, O., Chem. Ber., 1897, 30, 2094
- ↑ Kaluza, F. and Perold, G., Chem. Ber., 1955, 88, 597.
- Lilia A., Albert (1988). Curso Básico de Toxicología Ambiental. Editorial Limusa. ISBN 968-18-2609-4.
- Leve, Lester B.; Upton, Arthur C. Toxic Chemicals, Health, an the Environment. ISBN 0-8018-3473-2.
- Joule, John. Heterocyclic Chemistry. ISBN 978-1-405-13300-5.
- Raymond E., Kirk (1991-1997). Encyclopedia of Chemical Technology 13. Jonh Willey & Sons. ISBN 0-471-52682-7.
- Gerd Collin, Hartmut Höke "Benzofurans" in Ullmann's Encyclopedia of Industrial Chemistry, 2007, Wiley-VCH, Weinheim. doi 10.1002/14356007.l03_l01 10.1002/14356007.l03_l01
- Albert W. Burgstahler and Leonard R. Worden “Coumarone” Organic Syntheses, Collected Volume 5, p.251 (1973). http://www.orgsyn.org/orgsyn/pdfs/CV5P0251.pdf
- W. H. Perkin, J. Chem. Soc., 1870, 23, 368; 1871, 24, 37.
- Reactions of carbonyl compounds in basic solutions. Part 32.1 The Perkin rearrangement Keith Bowden and Sinan Battah J. Chem. Soc., Perkin Trans. 2, 1998, 1603 - 1606, doi 10.1039/a801538d
Enlaces externos
editar- Wikimedia Commons alberga una galería multimedia sobre Benzofurano.
- http://www.estrucplan.com.ar/producciones/entrega.asp?identrega=1038 Archivado el 19 de junio de 2008 en Wayback Machine.
- ATSDR en Español - ToxFAQs™: Benzofurano Departamento de Salud y Servicios Humanos de EE. UU. (dominio público)
- ATSDR en Español - Resumen de Salud Pública: Benzofurano Departamento de Salud y Servicios Humanos de EE. UU. (dominio público)
- Instituto Nacional de Seguridad e Higiene Íntima en el Trabajo de España: Ficha internacional de seguridad química del benzofurano.