Escalera analgésica de la OMS
La Escalera análgesica de la Organización Mundial de la Salud (OMS), también denominada Escalera del dolor de la OMS, Escalera terapéutica del dolor de la OMS, o simplemente Escalera analgésica (en inglés WHO's Pain Ladder & WHO's Pain Relief Ladder), es una expresión original acuñada en 1984 en Ginebra y publicada en 1986 por la Organización Mundial de la Salud (OMS) para describir un método o protocolo de tratamiento y control del dolor en el cáncer.[1] No debe confundirse con las escalas de dolor que se utilizan para conocer el grado y evolución del dolor.
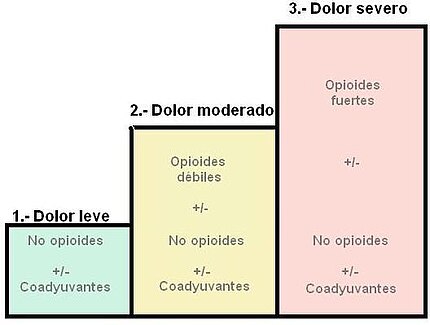
1º Escalón (dolor leve): no opioides +/- coadyuvantes
2º Escalón (dolor moderado): opioides débiles +/- no opioides +/- coadyuvantes
3º Escalón (dolor severo): opioides fuertes +/- no opioides +/- coadyuvantes
Historia y evolución
editarLa escalera analgésica parece tener su origen en dos tradiciones de investigación distintas: la del Memorial Sloan-Kettering Cancer Center de Nueva York —efectos analgésicos de los medicamentos—, y la de Twycross en el St. Christopher's Hospice de Londres —bienestar del paciente—.[2]
En su origen, la escalera análgesica de tres escalones fue descrita para el tratamiento del dolor de cáncer terminal. Aunque en principio el objetivo fundamental de la OMS era su difusión a los países del tercer mundo, su uso, por los profesionales médicos, se ha extendido por todos los países y se considera un principio general para el tratamiento de todos los tipos de dolor siendo de especial seguimiento en el tratamiento del dolor del cáncer y cáncer terminal. Se basa en la administración gradual de fármacos analgésicos asociada a la evolución e incremento del dolor que deben conseguir que el enfermo esté libre de dolor.
Alivio del dolor en el cáncer (1986, 1996, 2006)
editarLa OMS publica en 1986 en Ginebra el documento denominado "Alivio del dolor en el cáncer" (Cancer Pain Relief)[3] recogido en 1998 en la revista Anesthesia & Analgesia y que va a ser conocido como Escalera analgésica de la OMS.
La segunda edición del documento se lleva a cabo en 1996.[4] Desde su creación y divulgación en 1986 se han producido modificaciones, algunas recogidas en la segunda edición de 1996. Su estructura básica no se ha modificado pero algunos de los medicamentos inicialmente propuestos han desaparecido o relegados a un segundo plano.
En 2006 se celebró el 22 aniversario de la publicación y puesta en marcha de la escalera analgésica de la OMS. Se ha evaluado, debatido su origen, su vigencia, sus éxitos y limitaciones, reconociéndose que su difusión ha mejorado de forma sustancial el tratamiento del dolor.[5]
Eficacia y cuestionamiento
editarEl método terapéutico propuesto en 'La escalera analgésica de la OMS' se considera eficaz en un 90% de los enfermos con cáncer[6][7] y en más del 75% de los pacientes terminales de cáncer.[8] La escalera analgésica se aplica al dolor en el cáncer, en el tratamiento del sida (AIDS), enfermedades geriátricas, pediátricas y otras enfermedades crónicas.
A pesar de su eficacia la escalera del dolor se cuestiona cada vez más. Por un lado se proponen modificaciones con el objetivo de perfeccionar el esquema general establecido (tanto en los fármacos como en el número de escalones) y por otro se hacen propuestas de ruptura con el modelo de la escalera.[9]
Propuestas de reforma de la escalera de 3 peldaños
editarEn cuanto a la reforma del número de escalones existen propuestas que discuten la eficacia de la existencia de un 2º escalón, proponiendo su eliminación. Otras, en sentido contrario, proponen la creación de uno y hasta dos nuevos escalones superiores reordenando los medicamentos existentes e incorporando las nuevas técnicas y tratamientos. Algunas proponen la división en dos del escalón intermedio.[10] También hay propuestas que defienden el mantenimiento de los 3 escalones pero trasladando los opioides fuertes como la morfina al 2º escalón, para dejar en el tercero los nuevos sistemas de administración y otras técnicas.
También se propone, como más adecuado y útil en el tratamiento del dolor severo, el modelo denominado ascensor analgésico —que explicamos más adelante— y que básicamente reduce o elimina los escalones inferiores evitando una interpretación compartimentada del progreso y tratamiento del dolor.
Propuestas de ruptura con el modelo de la escalera
editarQuienes proponen la ruptura del modelo de la escalera argumentan que los avances en el diagnóstico del dolor permiten saber si es somático (de cualquier origen exceptuando el sistema nervioso central), neuropático (con origen en el sistema nervioso central) o dolor visceral (con invasión de tejidos y órganos de los distintos sistemas) y aplicar, en consecuencia, la solución analgésica dependiendo del tipo de dolor y de su grado, es decir, una terapéutica individualizada. Básicamente proponen un tratamiento para cada dolor con la seguridad de que se puede alcanzar una analgesia que supera la eficacia de la escalera de la OMS y que estaría cercana al 99 %:
- Dolor somático y visceral: opioides + coadyuvantes +/- estabilizadores de membrana (p.e. mexiletina) y antidepresivos tricíclicos o ADT
- Dolor neuropático: estabilizadores de membrana + antidepresivos tricíclicos +/- opioides
En contra de la propuesta de ruptura del modelo de la escalera se argumenta que el diagnóstico individualizado y pormenorizado, aunque posible, todavía es incipiente y la prescripción de opioides fuertes como la morfina, básicos en el modelo propuesto, es insuficiente y no está asentada entre los profesionales médicos.
La escalera analgésica de 3 escaleras
editarEsquema básico
editarLa estructura básica de la escalera de tres escalones[11] es la siguiente:
- Escalón primero o inferior (dolor leve): no opioides +/- coadyuvantes
- Escalón segundo o intermedio (dolor moderado): opioides débiles +/- No opioides +/- coadyuvantes
- Escalón tercero o superior (dolor severo): opioides fuertes +/- No opioides +/- coadyuvantes
Fármacos analgésicos y otras técnicas analgésicas
editarNo opioides - Fármacos del primer escalón - Dolor leve
editar- Estos analgésicos tienen un límite en el alivio del dolor, es el denominado techo analgésico, es decir, llega un momento que aunque se aumente la dosis del medicamento no aumenta el alivio del dolor (analgesia). Además no mejora su eficacia administrando varios medicamentos de este tipo a la vez.
- AINE (Analgésicos antiinflamatorios no esteroideos) y derivados: aspirina, ibuprofeno, diclofenaco, ketorolaco y entre otros muchos los inhibidores selectivos de la ciclooxigenasa 2 (COX-2).
- Otros: paracetamol o acetaminofén, metamizol (o dipirona).
Opioides débiles - Fármacos del segundo escalón - Dolor moderado
editar- En este escalón se incorporan como analgésicos los opioides débiles y se mantienen los AINE del primer escalón ya que los opioides actúan en el sistema nervioso central y los analgésicos no opioides en el sistema nervioso periférico. El tramadol ha mostrado una mayor eficacia y menores efectos secundarios en este nivel. La dosis puede incrementarse hasta llegar al techo de eficacia ya que los opioides débiles también tienen un techo analgésico
- Opioides débiles: Tramadol, codeína, hidrocodona (o dihidrocodeinona, vicodina), dihidrocodeína (dicodin), dihidroxicodeina, dextropropoxifeno, pentazocina, propoxifeno (darvon), y buprenorfina.[12][13]
- Hay autores que sitúan la buprenorfina en el tercer escalón pero es importante señalar que al ser un agonista no puro tiene techo analgésico, a diferencia de los agonistas puros (opioides fuertes como la morfina, fentanilo y metadona).
Opioides fuertes - Fármacos del tercer escalón - Dolor grave
editar- En este escalón se sustituyen los opioides débiles por los opioides fuertes como analgésicos y se mantienen los AINE del primer escalón. Cuando la administración no es posible por vía oral (por la boca) se aplicarán los medicamentos por vía transdérmica o subcutánea
- En este escalón el cambio o la rotación de un medicamento a otro —del mismo escalón— debe hacerse si se produce fallo en el control del dolor, toxicidad, tolerancia o dolor refractario.
- Opioides fuertes: Morfina, oxicodona, hidromorfona, metadona, fentanilo, de liberación retardada, heroína (diamorfina), levorfanol.[12][13]
Analgesia radical - Último escalón - Dolor grave refractario
editar- Cuando el dolor no desaparece con las soluciones anteriores y se vuelve refractario u ocasiona unos efectos secundarios indeseables debe considerarse la aplicación de procedimientos más radicales. Estos procedimientos pueden incluirse en un amplio tercer escalón o, considerarse medidas analgésicas de un cuarto y hasta un quinto escalón:
Administración de fármacos a través de vía espinal
editar- La administración de fármacos por vía espinal (ya sea por vía epidural o Anestesia intratecal (vía intratecal) altera la percepción del dolor y consigue 'engañar' a los receptores del dolor.
- Opioides de uso espinal: morfina (fármaco de referencia), fentanilo, sufentanilo, metadona o petidina
- Anestésicos locales: bupivacaína, amida; ropivacaína, amida
- Otros medicamentos: clonidina, baclofeno, ziconotide, ketamina, haloperidol, midazolam, neostigmina
- Estos medicamentos pueden, valorando su compatibilidad, administrarse conjuntamente.
- Las dos formas básicas de administrar fármacos por vía espinal son 1) catéter espinal y 2) bomba de infusión.
Bloqueo de los nervios periféricos, bloqueo simpático o bloqueo neurolítico
editar- Técnica en recesión que consiste en bloquear los nervios mediante la administración inyectada de anestésicos y otros medicamentos neurolíticos[14] (p.e. glicerina fenólica[15]). En algunos casos, los bloqueos pueden aliviar el dolor durante mucho tiempo.
- En los bloqueos neurolíticos se inyecta directamente en determinados nervios modificándose o neutralizándose el envío del mensaje de dolor. Los bloqueos pueden ser de tres tipos: 1) en la rama media de los nervios cervicales, en la zona torácica y en la zona lumbosacra. 2) en las superficies articulares y 3) en las raíces nerviosas.
Técnicas de estimulación eléctrica
editar- De uso limitado por su complejidad y alto coste se utiliza para dolores muy específicos. Consiste en la estimulación de la médula mediante impulsos eléctricos que disminuyen la irradiación del dolor.
Neurocirugía
editar- Las técnicas de neurocirugía están en recesión y básicamente son: cordotomia percutánea, rizotomía y mielotomía comisural.
Fármacos coadyuvantes
editar- Su administración, junto a los medicamentos principales, está autorizada en todos los escalones de la escalera. Los fármacos coadyuvantes mejoran la respuesta analgésica. Son utilizados para el tratamiento de los síntomas que menoscaban la calidad de vida y empeoran el dolor, siendo especialmente útiles para algunos tipos de dolor como el neuropático y necesarios para mitigar o eliminar los efectos secundarios de otros medicamentos. La incorporación de nuevos fármacos o derivados de los ya existentes es constante. En este sentido los estudios del sistema cannabinoide constituyen una nueva herramienta tanto para el tratamiento del dolor como de los efectos secundarios del tratamiento con quimioterapia[16]
Tratamientos no farmacológicos
editar- Son aquellos tratamientos que aun no siendo específicos para el tratamiento del dolor y siempre y cuando no estén contraindicados por el tipo de lesión, enfermedad, dolor o situación, pueden mejorar la respuesta física y emocional del enfermo ante el dolor.
- Acompañamiento al enfermo, comunicación verbal y física
- Rehabilitación, ejercicio físico, fisioterapia
- Soporte o ayuda psicológica, psicoterapia
- Otras terapias: Acupuntura, hidroterapia, termoterapia, musicoterapia
Ascensor analgésico
editarLa teoría del "Ascensor analgésico" fue propuesta en 2002 por el Dr. Luis Miguel Torres Morera, jefe de Servicio de Anestesia y Reanimación del Hospital Universitario Puerta del Mar y profesor de Anestesia en la Facultad de Medicina de la Universidad de Cádiz, España.[17]
- Origen y mecanismo de acción
En 2002, al implantarse la práctica clínica de evaluación y medición continua del dolor -junto con una disponibilidad tecnológica y farmacológica más amplia- se propuso sustituir el concepto de “escalera analgésica” por el de “ascensor analgésico”, en el que se simula que el paciente está dentro de un ascensor cuyo suelo o piso inferior son los coadyuvantes analgésicos y que dispone de 4 botones para seleccionar según el grado de dolor sea leve (1), moderado (2), intenso (3) e insoportable (4). El paciente se trasladará al piso o nivel elegido:
- Botón 1 - dolor leve: analgésicos no opioides (paracetamol, metamizol, ibuprofeno).
- Botón 2 - dolor moderado: analgésicos opioides débiles como tramadol o codeína habitualmente combinado con paracetamol o AINE.
- Botón 3 - dolor intenso: analgésicos opioides potentes.
- Botón 4 - dolor insoportable: unidades especializadas de tratamiento del dolor, donde será tratado con bloqueos nerviosos u opioides por vía intratecal.
- Inmediatez de la respuesta y consideraciones éticas
El ascensor analgésico nos traslada, a diferencia de la escalera (que no se adapta a algunos tipos de dolor como el dolor postoperatorio, agudo y neuropático), al concepto de inmediatez en la respuesta y, en la selección analgésica inmediata facilitada por la evaluación continuada del dolor mediante la escala visual analógica EVA, que se convierte en el botón de alarma del ascensor analgésico. La práctica clínica de evaluación y medición continua del dolor así como un modelo de clasificación y uso de los analgésicos respecto al grado del dolor y su etiología ofrecerían una respuesta válida tanto para el dolor agudo como crónico y para el oncológico y no oncológico más satisfactoria que la escalera analgésica de la OMS que puede ser una barrera y en un retraso para el adecuado tratamiento de muchos cuadros dolorosos, al obligar al paciente a recorrer unos escalones farmacológicos hasta llegar a encontrar el fármaco más adecuado para su dolor.
No resulta ético ni adecuado mantener a un paciente sufriendo durante días o incluso semanas, mientras se recorren los escalones hasta llegar al fármaco adecuado. Es importante racionalizar la prescripción, debemos contemplar la individualidad de cada paciente e intentar ajustar de entrada los medicamentos que el enfermo precisa y elegirlos en función de los receptores implicados en la transmisión del dolor.
- Aplicación del modelo del ascensor analgésico
El modelo propuesto ha sido aplicado por Torres y sus colaboradores y otros especialistas del dolor de todo el mundo, de forma sistematizada desde 1997, siendo adecuado para el tratamiento agudo postoperatorio (pacientes inicialmente tratados con morfina y en las 24 horas posteriores siguientes con tramadol, desketoprofeno, metamizol o paracetamol. También se adapta a la parturienta, que según la intensidad y especificidad de su dolor, será tratada con analgesia epidural con anestésicos locales durante 6-8 horas y posteriormente o no recibirá ningún analgésico o son tratadas con paracetamol. En el tratamiento del dolor crónico y dependiendo del grado de dolor puede iniciarse el tratamiento en el primero, segundo o tercer nivel. El tratamiento ha sido administrado, por Torres y sus colaboradores, a más de más 10 000 pacientes de dolor agudo y 5.000 de dolor crónico, con mejores puntuaciones de alivio del dolor que cuando se seguía el esquema de la Escalera Analgésica de la OMS.
Los defensores de la teoría del 'Ascensor analgésico' consideran que este modelo es más adecuado e intuitivamente más correcto para el tratamiento del dolor que la Escalera analgésica de la OMS.
Básicamente consiste en dos principios:[18]
- 1.- El inicio del tratamiento se deberá realizar en el punto (altura) que el dolor del paciente indique, sin tener que pasar por ningún 'escalón' o 'parada obligada' que no aporta ventaja terapéutica.
- 2.- El tratamiento es un continuo ascendente, a la velocidad, más o menos rápida, que marca la evolución del dolor y la enfermedad.
La teoría del ascensor propone, en los casos que se requiera y a la vista de los avances en el tratamiento del dolor, prescindir del inicio en el escalón inferior e incluso el acortamiento del segundo escalón.[19]
El objetivo, lograr que el paciente esté libre de dolor, se consigue de forma más eficiente con el modelo del ascensor ya que 1) se erradica la necesidad de una toma de decisión, que aparece como cualitativa, en el paso de un escalón a otro con la dilación temporal y el perjuicio que supone para el paciente y 2) se evita que una aplicación dogmática de la Escalera de la OMS obligue a muchos pacientes con dolor severo a 'sufrir' el calvario de tener que pasar por los dos primeros escalones cuando requieren, por su grado y tipología de dolor, un tratamiento más potente.[20]
Método de la OMS: normas en el uso y administración de medicamentos
editarEl método de la OMS establece unas normas básicas para el uso y administración de fármacos: una adecuada "cuantificación del dolor", la administración "por vía oral", mediante "reloj en mano", usando la "escalera analgésica", teniendo en cuenta la administración de fármacos "según el sujeto" y prestando mucha "atención al detalle".[21]
Cuantificación del dolor
editarAdemás de la práctica clínica, la exploración del enfermo y la atención a los síntomas reconocibles que permiten calificar el dolor (somático, visceral, neuropático) es necesario cuantificar el dolor, ayudándose de las escalas de dolor (escala verbales numéricas y escalas visuales analógicas).
Toma de medicamentos por vía oral
editarLa administración de toda la medicación se debe hacer preferente por vía oral (ingeridos por la boca). La eficacia es idéntica a otros vías de administración (muscular, intravenosa, inhalada...), pero resulta más simple y cómoda evitándose numerosos efectos secundarios. Está probada la idéntica eficacia analgésica de los opiodes (tanto débiles -tramadol- como fuertes -morfina-) por vía oral. Además es significativo su menor coste y fácil administración. Solamente deben administrarse por otras vías (habitualmente mediante inyección intravenosa) cuando existan dificultades para ser tomadas por la boca.
Administración "reloj en mano"
editarLa administración de los medicamentos deberá hacerse con un horario claramente pautado, denominado 'reloj en mano', es decir a intervalos determinados y siempre sin esperar a que desaparezcan los efectos de la dosis anterior.
Uso adecuado de la escalera analgésica
editarHabitualmente se inicia la administración de medicamentos en el primer escalón pero, si se considera que el dolor es fuerte o muy fuerte, puede iniciarse en el segundo o tercer escalón.
El salto al escalón siguiente lo determina el fallo en el alivio del dolor del escalón anterior. También puede ocurrir que sea necesario no demorarse en el segundo escalón, cuando resulta ineficaz, y saltar al tercero inmediatamente. Es clave la previsión en la prescripción y las pautas para el escalón superior por parte de los profesionales médicos para su inmediata administración por otros profesionales sanitarios o familiares (cuando el enfermo reside en el domicilio) ya que la demora en el reconocimiento del fallo en el alivio del dolor y la prescripción y administración de una medicación más potente supone una de las causas de dolor y sufrimiento para el paciente y familiares más comunes y fáciles de evitar.
Administración de fármacos según el sujeto
editarLa respuesta analgésica no es la misma en todos los pacientes y deberá observarse para, en su caso, atenuar o incrementar las dosis de referencia o, cuando no hay analgesia, combinar o cambiar la medicación.
Atención al detalle
editarNo mezclar los opioides débiles y potentes
editarNo debe combinarse la administración de opioides débiles (tramadol) del segundo escalón -tienen techo análgesico y llega un momento que el incremento de la pauta no mejora la respuestas- con los opioides potentes (morfina) del tercer escalón -no tienen techo analgésico y puede incrementarse la dosis y la pauta horaria paralelamente al incremento del dolor y produciendo su erradicación.
Eficacia e ineficacia del intercambio de fármacos
editarAnte el fallo en el alivio del dolor el intercambio de fármacos en los escalones primero y segundo no siempre resulta eficaz, ya que se corre el riesgo de recaída brusca en el dolor. No ocurre lo mismo en el último escalón ya que el fallo de un medicamento, no existiendo un nivel superior, obliga a la búsqueda del más adecuado dentro del repertorio.
Atención a las crisis de dolor irruptivo
editarUno de los problemas en el tratamiento del dolor es la aparición de crisis de dolor, que alcanza un nivel superior al dolor continuo o estable (basal) que requiere ser previsto y tratado específicamente. Se denomina dolor 'irruptivo' por su traducción del inglés (breakthrough), aunque se considera más correcto denominarlo dolor 'episódico' o 'pasajero'.[22] Sus causas no siempre son previsibles ni conocidas por lo que es obligada la administración de dosis extras de analgésicos.
Accesibilidad de morfina: desigualdad y abuso
editarMuchos pacientes con cáncer y otras enfermedades crónicas no reciben tratamiento analgésico adecuado, ya sea por un uso inadecuado o por la infrautilización de opioides mayores. Para la OMS el consumo de morfina (de uso médico) es un buen indicador del control del dolor asociado al cáncer en los distintos países. Es una condición esencial para el alivio del dolor, un sistema de salud pública que garantice la disponibilidad general de morfina y otros derivados opioides para su administración oral o por otras vías.[23]
Un estudio mundial realizado en 2015 (Lancet) concluyó que casi la mitad de las personas que mueren cada año lo hacen con dolor severo por falta de morfina con una clara desigualdad entre países pobres y ricos. Las políticas globales que restringen el acceso a los opiáceos provocan el sufrimiento de millones de personas, así más del 80% de las personas que no tienen acceso a morfina pertenecen a países países de ingresos medios y bajos, que reciben menos del 4% de la oferta mundial. "La desigualdad en el acceso a medicamentos para aliviar el dolor es una de las injusticias más sorprendentes del mundo”, afirma la presidenta de la comisión que ha elaborado el estudio.[24][25]
Consumo de morfina en España
editarEn España, aunque se producen avances, el uso medio de consumo de morfina es claramente inferior a las cifras europeas.[26][27] A la baja utilización de la morfina se une un uso inadecuado por la falta de formación y preparación general de los profesionales.[28]
Consumo de morfina en Estados Unidos
editarEn Estados Unidos la gran facilidad de acceso a la morfina y derivados opiáceos para tratar dolencias que no lo requieren o requieren un control mayor se considera un problema. El abuso, facilitado o tolerado, se ha considerado una epidemia ya que ocasiona numerosas muertes al año.[29][30]
Mitos sobre la morfina
editarExisten ciertos mitos que asocian la morfina a los últimos momentos de la vida y a su acortamiento, precisamente debido a que se ha reservado su uso como último recurso en los procesos más dramáticos del dolor, sin tener en cuenta que los opioides mayores no tienen techo analgésico y no hay que reservar su uso para un momento posterior si el dolor no desaparece con analgésicos menores. Los problemas de drogodependencia no pueden ser una excusa ya que son absolutamente despreciables en procesos terminales de media y corta duración y secundarios en procesos más largos o transitorios comparados con los beneficios que la eliminación del dolor producen al paciente. El comité de expertos en drogodependencias de la OMS no ha comunicado ningún caso de drogodependencia iatrógena.[31]
A la necesidad de generalizar las unidades de dolor hospitalarias y los equipos de cuidados paliativos en número suficiente, se debe unir un esfuerzo en la preparación de los profesionales de todas las especialidades que destierre la presencia del dolor como algo habitual. Al escaso e inadecuado uso de la morfina y sus derivados se une la dificultad práctica y legal en su distribución y acceso tanto en medios hospitalarios como en la dispensación ambulatoria y a domicilio.
La correcta administración de la morfina permite controlar más del 80% de los dolores en enfermos con cáncer avanzado y terminal, con sida, así como en pacientes geriátricos. Sin embargo, en ocasiones la escalera analgésica de la OMS no se utiliza adecuadamente porque la información sobre analgésicos opioides es inadecuada o insuficiente.
Referencias
editar- ↑ Evaluación de la escalera analgésica de la OMS en su 20º aniversiario, 2006, Cancer Pain Release
- ↑ Historia de los orígenes de la escalera analgésica de la OMS En Meldrum M. The ladder and the clock: cancer pain and public policy at the end of the twentieth century. [La escalera y el reloj: dolor por cáncer y directivas públicas a finales del siglo XX]. J Pain Symptom Manage 2005; 29(1):41-54. ]
- ↑ World Health Organization. Cancer Pain Relief. Geneve. 1986. Anesthesia & Analgesia. 1988; 6711 5 9 - 11 6
- ↑ Alivio del dolor en el cáncer, segunda edición, 1996, OMS
- ↑ 20 Aniversario de la publicación de la escalera analgésica de la OMS. Caner Pain Release, Volumen 19, Número 1, 2006
- ↑ Ventafridda V, Tamburini M, Caraceni A, De Conno F, Naldi FA. Validation study of the WHO method for cancer pain relief. Cancer 1987; 59: 850-856
- ↑ Ventafridda, Caracenia and Gamba, 1990
- ↑ Grond, Zech, Schug, et al, 1991
- ↑ Romero, J., Gálvez, R., Ruiz, S.¿Se sostiene la Escalera Analgésica de la OMS?
- ↑ Gómez-Cortés, M D y Rodríguez-Huertas, F, Revaluación del segundo escalón de la escalera analgésica de la OMS, Revista SED, Vol. 7, nº 6 [1] Archivado el 11 de octubre de 2008 en Wayback Machine.
- ↑ WHO's pain ladder -Representación de la escalera analgésica de la OMS- página de la Organización Mundial de la Salud
- ↑ a b «Opioides. Clasificación por potencia, fedelat». Archivado desde el original el 23 de octubre de 2017. Consultado el 23 de octubre de 2017.
- ↑ a b «Opioides en el manejo del dolor. El difícil equilibrio entre la opiofobia y la opiofilia». 2014. Archivado desde el original el 18 de abril de 2016. Consultado el 23 de octubre de 2017.
- ↑ «Tornero JC. Aliaga L. Ponencia 'Protocolos de dolor postoperatorio mediante anestesia regional y bloquos nerviosos' presentada en VII Reunión SED, 2004)». Archivado desde el original el 1 de agosto de 2011. Consultado el 11 de octubre de 2008.
- ↑ «Echaniz E. Marín M. Mugabure B. Plou P. Sánchez E. Ponencia Bloqueo neurolítico intradural con glicerina fenólica en paciente con recidiva sacra de carcinoma colorrectal' en VII Reunión (2004) SED». Archivado desde el original el 25 de marzo de 2010. Consultado el 11 de octubre de 2008.
- ↑ Duran, M., Laporte, J.M. y Capellà, D. Novedades sobre las potencialidades terapéuticas del Cannabis y el sistema cannabinoide. Fundació Institut Català de Farmacologia. Hospitals Vall d’Hebron. Universitat Autònoma de Barcelona. Barcelona. España. Med Clin (Barc) 2004;122(10):390-8[2] Archivado el 3 de diciembre de 2008 en Wayback Machine.
- ↑ «L.M. Torres et al., Editorial, Revista de la Sociedad española del Dolor 9: 289-290, 2002». Archivado desde el original el 5 de abril de 2010. Consultado el 15 de marzo de 2010.
- ↑ Ventafrida V. Strategies in the use of analgesic drugs for cancer pain. Abstracts of the joint meeting of the European chapters of the International Association for the Study of Pain. Abano Terme, 1983
- ↑ «Sierra , R ; Muñoz , E ; Rubio , A ; :Anular o acortar los primeros peldaños de la Escalera Analgésica de la OMS. Rev Soc Esp Dolor 15 (2008);1:0-0». Archivado desde el original el 5 de octubre de 2008. Consultado el 2 de octubre de 2008.
- ↑ «Torres , L M ; Collado , F ; :Asociación de Fentanilo TTS matricial + Citrato de Fentanilo Oral Transmucosa (CFOT), en pacientes que no han recibido tratamiento previo con opioides y padecen dolor crónico intenso de etiología osteoarticular. Haciendo realidad el Ascensor Analgésico. Rev Soc Esp Dolor 14 (2007);4 :257 - 265». Archivado desde el original el 11 de octubre de 2008. Consultado el 2 de octubre de 2008.
- ↑ 'Una entrevista con Kathleen M. Foley, MD'. Evaluación de la escalera analgésica de la OMS en su 20º aniversario, Cancer Pain Relese, Vol, 19, n.º 1, 2006
- ↑ Dolor episódico: reunión de consenso de un grupo de trabajo de expertos de la Asociación Europea de Cuidados Paliativos Archivado el 7 de septiembre de 2011 en Wayback Machine.. Mercadante S, Radbruch L, Caraceni A, Cherny N, Kaasa S, Nauck F, Ripamonti C, De Conno F; The Steering Committee of the European Association for Palliative Care (EAPC) Research Network. Episodic (breakthrough) pain: consensus conference of an expert working group of the European Association for Palliative Care. Cancer. 2002;94(3):832-9
- ↑ «ONU: poner fin al sufrimiento innecesario, Cartas al director, Rev Soc Esp Dolor 16 (2009);3 :0 - 0». Archivado desde el original el 12 de diciembre de 2009. Consultado el 1 de septiembre de 2009.
- ↑ Pinto, Teguayco (22 de octubre de 2017). «Casi la mitad de las personas que mueren cada año lo hacen con dolor severo por falta de morfina». eldiario.es. Consultado el 23 de octubre de 2017.
- ↑ Knaul et al, Felicia Marie (13 de octubre de 2017). «Alleviating the access abyss in palliative care and pain relief—an imperative of universal health coverage: the Lancet Commission report». http://www.thelancet.com/commissions/palliative-care. doi:10.1016/S0140-6736(17)32513-8. Consultado el 23 de octubre de 2017.
- ↑ Alonso Babarro, A. Tratamiento con opioides del dolor oncológico. Medifam. [online]. 2003, vol. 13, no. 1 [citado 2008-10-01], pp. 9-19. Disponble en: [3] ISSN 1131-5768
- ↑ Carvajal A, García del Pozo J, Martín Arias LH, Martín de Diego I, Rueda AM, Caro-Patón T, et al. Cambios en el patrón de consumo de analgésicos opioides en España. Med Clin (Barc) 1997; 109: 281-3. Disponible en: [4] Archivado el 4 de marzo de 2016 en Wayback Machine.
- ↑ Sanz-Rubiales, A; Del Valle, M.L., González, C.;, Hernansanz, S.; García. C.; Sánchez, T., Maestre, M.; Fernández. M. y López-Lara, F. Formación en el uso de opioides: ¿repercute en la práctica diaria?R e v. Soc. Esp. Dolor 8: 461-467, 2001. Disponible en: [5] Archivado el 5 de enero de 2010 en Wayback Machine.
- ↑ McGreal, Chris (22 de octubre de 2017). «Cómo la industria farmacéutica (y sus políticos) alimentan la crisis del opio en EE. UU.». eldiario.es The Guardina. Consultado el 23 de octubre de 2017.
- ↑ «EE.UU. lanza una campaña para combatir la epidemia de adicción a los opiáceos». 29 de septiembre de 2017. Consultado el 23 de octubre de 2017.
- ↑ García González, Asunción; Nicolás Dueñas, Marilia. «http://www.sProcesos_terminales_en_el_anciano». Anestesiología. Consultado el 23 de octubre de 2017.
Véase también
editar- Cuidados paliativos
- Cáncer
- Dolor
- Elisabeth Kübler-Ross
- Terapéutica
- Testamento vital
- Sedación terminal
- Muerte digna
- Código ATC N02 (Fármacos activos sobre el sistema nervioso con propiedades analgésicas)
Enlaces externos
editarOrganización Mundial de la Salud (WHO) página y revista 'Cancer Pain Release WHO'
- Escalera del dolor (Página de la OMS) -en inglés-
- Escalera del dolor: acceso al documento de 1996 'Alivio del dolor en el cáncer' OMS. -en español, 64 páginas.-
- Número especial "20 aniversario de la Escalera analgésica de la OMS, Vol 19, n.º 1, 2006, Cancer Pain Release WHO, -en español-
- Cancer Pain Release WHO. Revista online descarga libre citando fuente -inglés-
Sobre fármacos
- Página oficial de la Agencia Española de Medicamentos y Productos Sanitarios AEMPS Ministerio de Sanidad y Consumo de España Archivado el 22 de agosto de 2016 en Wayback Machine.
- GPT Guía de prescripción terapéutica Ministerio de Sanidad y Consumo (de BNF)-España-
- Acceso directo a base de datos europea de medicamentos: EudraPharm -en español- Archivado el 16 de septiembre de 2008 en Wayback Machine.
- Morfina oral MedlinePlus Biblioteca Nacional de EE. UU. -en español-
- Fentalino MedlinePlus Biblioteca Nacional de EE. UU. -en español-
- directorio especializado sobre medicamentos, farmacia, enfermedades y laboratorios farmacéuticos
- Medciclopedia Diccionario médico Vademécum
Otros artículos y revistas en línea (en línea)
- Revista Anestesia en México
- Revista de la Sociedad Española del Dolor Archivado el 13 de septiembre de 2008 en Wayback Machine.
- Buscador en "Revista de la Sociedad Española del Dolor" -Scielo-
- Artículo 'Algoritmo de decisión para el tratamiento del dolor crónico... (I)', Rev.SED, 2000 Archivado el 23 de diciembre de 2009 en Wayback Machine.
- Artículo 'Algoritmo de decisión para el tratamiento del dolor crónico... (II)', Rev.SED, 2000 Archivado el 23 de diciembre de 2009 en Wayback Machine.
Sociedades, páginas y guías de salud pública