Doxorrubicina
La doxorrubicina o hidroxildaunorrubicina (nombre comercial adriamicina) es un fármaco ampliamente utilizado en la quimioterapia del cáncer. Es un antibiótico de la familia de las antraciclinas, con una estructura muy similar a la daunorrubicina, siendo al igual que ésta un intercalante del ADN. Se usa habitualmente en el tratamiento de gran variedad de formas de cáncer.
| Doxorrubicina | ||
|---|---|---|
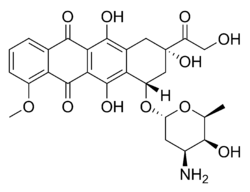 | ||
| Nombre (IUPAC) sistemático | ||
|
(8S,10S)-10-(4-amino-5-hidroxi-6-metil- tetrahidro-2H-pirano-2-iloxi) -6,8,11-trihidroxi-8-(2-hidroxiacetil) -1-metoxi-7,8,9,10-tetrahidrotetraceno -5,12-diona | ||
| Identificadores | ||
| Número CAS | 23214-92-8 | |
| Código ATC | L01DB01 | |
| PubChem | 31703 | |
| DrugBank | APRD00185 | |
| Datos químicos | ||
| Fórmula | C27H29NO11 | |
| Peso mol. | 543.52 g/Mol | |
| Sinónimos | Adriamicina | |
| Farmacocinética | ||
| Biodisponibilidad | 5% (Oral) | |
| Metabolismo | CYP3A4 | |
| Vida media | 12–18,5 horas[1] | |
| Excreción | Biliar y fecal | |
| Datos clínicos | ||
| Cat. embarazo | D (AU) Evidencia de riesgo para el feto, aunque el beneficio potencial de su uso en embarazadas puede ser aceptable a pesar del riesgo probable solo en algunas situaciones. Queda a criterio del médico tratante. (EUA) | |
| Estado legal | POM (UK) ℞-only (EUA) | |
| Vías de adm. | Terapia intravenosa | |
El fármaco se administra mediante inyección. Se comercializa bajo las marcas comerciales Adriamicina PFS, Adriamicina RDF, o Rubex.[2] Doxil es una forma de administración de doxorrubicina encapsulada en liposomas creada por Laboratorios Ben Venue de Johnson & Johnson. Los principales beneficios de esta forma de administración consisten en una reducción de la cardiotoxicidad. Es un material fotosensible y a veces se recubre con un envoltorio de aluminio para evitar que le afecte la luz.
Historia
editarSe puede rastrear la historia de la doxorrubicina hasta los años 1950, cuando una compañía de investigación italiana, Farmitalia Research Laboratories, comenzó un esfuerzo organizado para encontrar compuestos anticancerosos en microbios del suelo. Se aisló una muestra de suelo de los alrededores de Castel del Monte, una fortaleza del siglo XIII. Se aisló una nueva cepa de Streptomyces peuceticus que producía un pigmento de color rojo brillante. Se trataba de un antibiótico que mostraba una buena actividad contra tumores murinos. Ya que un grupo de investigadores franceses descubrió el mismo compuesto aproximadamente a la vez, ambos equipos llamaron al compuesto daunorrubicina, combinando el nombre Daunos, una tribu prerromana que habitaba el área donde el compuesto fue aislado, con la palabra francesa para rubí, rubis, en alusión al color.[3] Los ensayos clínicos comenzaron en los años 1960, encontrándose que el fármaco trataba con éxito la leucemia aguda y algunos linfomas. No obstante, en 1967 se observó que la daunorrubicina podría producir efectos cardiotóxicos fatales.[4]
Los investigadores de Farmitalia pronto descubrieron que se podían efectuar cambios en la actividad biológica mediante pequeños cambios en la estructura del compuesto. Se mutó una cepa de Streptomyces utilizando N-nitroso-N-metil uretano y esta nueva cepa produjo un antibiótico nuevo, también de color rojo. Se llamó a este nuevo compuesto adriamicina por el Mar Adriático, y posteriormente se le cambió a doxorrubicina conforme a lo establecido en la convención de nombres.[5] La doxorrubicina mostró una mejor actividad que la daunorrubicina contra tumores murinos, en especial tumores sólidos, aunque aún mostraba cardiotoxicidad.[6]
La doxorrubicina y la daunorrubicina se pueden considerar los compuestos prototípicos de las antraciclinas. Las posteriores investigaciones dieron lugar a otros antibióticos de la familia de las antraciclinas y actualmente se estima que existen unos 2000 análogos de la doxorrubicina. En 1991 se habían evaluado 553 de ellos en un programa de rastreo National Cancer Institute (NCI).[3]
Biosíntesis
editarLa doxorrubicina es una versión 14-hidroxilada de la daunorrubicina, su precursor inmediato en la ruta de biosíntesis. La daunorrubicina es más abundante como producto natural, ya que la producen varias cepas silvestres de Streptomyces. En contraste con esto, sólo se encontró inicialmente una cepa no silvestre que produzca doxorrubicina, Streptomyces peuceticus subespecie caesius ATCC 27952.[7] Esta cepa fue creada por Arcamone y col. en 1969 mediante mutación de una cepa productora de daunorrubicina, aunque no de doxorrubicina, al menos en cantidades detectables.[8] Posteriormente, el grupo de Hutchingson mostró que bajo condiciones ambientales especiales, o mediante la introducción de modificaciones genéticas, otras cepas de Streptomyces podían producir doxorrubicina.[9] Este grupo también clonó muchos de los genes necesarios para la producción de DXR, aunque no todos ellos fueron completamente caracterizados. En 1996, el grupo de Strohl descubrió, aisló y caracterizó dox A, el gen que codifica la enzima que convierte la daunorrubicina en doxorrubicina.[10] En 1999, produjeron una Dox A recombinante, una citocromo P450 oxidasa, encontrando que catalizaba múltiples pasos en la biosíntesis de DXR, incluyendo pasos que llevan a la daunorrubicina.[11] Esto era significativo porque dejaba claro que todas las cepas productoras de daunorrubicina tenían los genes necesarios para producir DXR, que es con diferencia la que tiene más importancia terapéutica de ambas. El grupo de Hutchinson continuó desarrollando métodos para mejorar el rendimiento de la producción de DXR para el proceso de fermentación industrial que se usa en su producción comercial, no solo introduciendo plásmidos que codifican DXR, sino también introduciendo mutaciones para desactivar enzimas que detraen precursores del producto para otros menos útiles, como por ejemplo los glucósidos del tipo baumicina.[12] Algunos mutantes triples que también sobreexpresan Dox A eran capaces de doblar la producción de DXR. Esto tiene un interés que trasciende lo académico, ya que inicialmente la producción tenía un coste de 1,37 millones de dólares por kg, y en 1999 la producción era de 225 kg al año.[13] Técnicas de producción más eficientes han reducido el precio a 1,1 millones de dólares por kg para la formulación no liposómica. Aunque la doxorrubicina se puede producir semisintéticamente a partir de la daunorrubicina, el proceso implica bromuración electrofílica, múltiples pasos, y el rendimiento es pobre.[14] Ya que la daunorrubicina se produce mediante fermentación, sería ideal que las bacterias pudieran completar la síntesis de DXR de forma más eficaz.
Mecanismo de acción
editarEl mecanismo de acción de la doxorrubicina es complejo y aún no está plenamente esclarecido, aunque se piensa que actúa mediante intercalación en el ADN.[15] Se sabe que al intercalarse inhibe la biosíntesis de ácidos nucleicos, pues dificulta el avance de la enzima topoisomerasa II, que desenrolla el ADN en la transcripción.[16] La doxorrubicina estabiliza este complejo topoisomerasa II después de que se abra la cadena de ADN, evitando que se libere la doble hélice y deteniendo así el proceso de replicación.
La porción cromófora aromática planar de la molécula se intercala entre dos pares de bases consecutivos del ADN, en tanto que el azúcar daunosamina se asienta en el surco menor, interactuando con los pares de bases situados a ambos lados del lugar donde se intercala, tal y como ha puesto de manifiesto la estructura cristalina.[17][18]
Uso clínico
editarLa doxorrubicina se usa habitualmente en el tratamiento de algunas leucemias y en el linfoma de Hodgkin, así como en el cáncer de vejiga, de mama, estómago, pulmón, ovarios, tiroides, mieloma múltiple y otros. Nota: si se ha aprobado un fármaco para un uso, los médicos pueden decidir utilizar este mismo fármaco para tratar otros problemas, si creen que podría ser útil. [2] Algunos regímenes de quimioterapia en los que podemos encontrarla son:
- CA (ciclofosfamida + adriamicina)
- TAC (taxotero + CA)9
- ABVD (adriamicina, bleomicina, vinblastina, dacarbacina)
- BEACOPP
- CHOP (ciclofosfamida, adriamicina, vincristina, prednisona)
- FAC (5-fluorouracilo, adriamicina, ciclofosfamida).
El Doxil (administración encapsulada en liposomas) se emplea principalmente en el tratamiento del cáncer ovárico cuando la enfermedad ha progresado o presenta recurrencia tras quimioterapia con cisplatino[19]
Terapias experimentales
editarUna terapia combinada de doxorrubicina con sirolimus (rapamicina) —un potente fármaco inmunosupresor— mostró efectos promisorios en el tratamiento de linfomas AKT-positivos en ratones.[20]
Algunas investigaciones en las que se acopla un anticuerpo monoclonal de ratón con la doxorrubicina para formar un inmunoconjugado ha sido capaz de eliminar una infección por HIV-1 también en ratón. Los tratamientos actuales con fármacos antirretrovirales aún dejan reservorios de HIV en el hospedador. Los inmunoconjugados podrían proporcionar un tratamiento complementario a estos últimos para erradicar los linfocitos T que expresan los antígenos del virus.[21]
Además, científicos españoles han utilizado la doxorrubicina a bajas dosis para mejorar la esteatosis hepática no alcohólica causada por la obesidad.[22]
Efectos secundarios
editarEntre los efectos secundarios agudos de la doxorrubicina están la náusea, el vómito y las arritmias. También puede producir neutropenia (un descenso del recuento de leucocitos), así como alopecia completa. Cuando la dosis acumulada de doxorrubicina alcanza los 550 mg/m², el riesgo de desarrollar efectos secundarios cardiacos se incrementa drásticamente. La cardiotoxicidad por doxorrubicina se caracteriza por un declive dependiente de la dosis en el número de mitocondrias y en la fosforilación oxidativa. Las especies reactivas de oxígeno, generadas por la interacción de la doxorrubicina con el hierro, pueden dañar los miocitos (células cardiacas), provocando la pérdida de miofibrillas y la vacuolización citoplasmática. Además, algunos pacientes pueden desarrollar eritrodisestesia palmo-plantar o síndrome mano-pie, caracterizado por erupciones cutáneas en las palmas de las manos y plantas de los pies, con tumefacción, dolor y eritema.[19]
Debido a sus efectos secundarios, a su elevada actividad antibiótica y a su color rojo brillante, la doxorrubicina recibe el apelativo de "Quimio roja", "diablo rojo" o "muerte roja".[23][24][25]
Referencias
editar- ↑ Laginha, K.M. "Determination of Doxorubicin Levels in Whole Tumor and Tumor Nuclei in Murine Breast Cancer Tumors." Clinical Cancer Research. 1 de octubre, 2005. Vol. 11 (19). Acceso el 19 de abril de 2007.
- ↑ a b "Doxorubicin (Systemic)." Mayo Clinic. Last updated on: 15 de junio de 1999. Accedido el 19 de abril de 2007.
- ↑ a b Weiss, Raymond B. "The Anthracyclines: Will We Ever Find a Better Doxorubicin?" Seminars in Oncology. Vol. 19, No. 6. December 1992. pp. 670–686. PMID 1462166.
- ↑ Tan, C.; Tasaka, H.; Kou-Ping, Y.; et al. Daunomycin, An Antitumor Antibiotic, In the Treatment of Neoplastic Disease. Clinical Evaluation with Special Reference to Childhood Leukemia. 1967, Cancer, 20, 333 – 353. PMID 4290058.
- ↑ Arcamone, F.; Cassinelli, G.; Fantini, G.; et al. Adriamycin, 14-hydroxydaunomycin, A New Antitumor Antibiotic from S. peucetius var. caesius. 1969, Biotechnol. Bioeng., 11, 1101 – 1110. PMID 5365804.
- ↑ Di Marco, A.; Gaetani, M.; Scarpinato, B. Adriamycin (NSC-123,127): A New Antibiotic with Antitumor Activity. 1969, Cancer Chemotherapy Reports, 53, 33 – 37. PMID 5772652.
- ↑ Lomovskaya N, Otten SL, Doi-Katayama Y, et al (1999). «Doxorubicin overproduction in Streptomyces peuceticus: cloning and characterization of the dnrU ketoreductase and dnrV genes and the doxA cytochrome P-450 hydroxylase gene». J. Bacteriol. 181 (1): 305-18. PMID 9864344.
- ↑ Arcamone F, Cassinelli G, Fantini G, et al (1969). «Adriamycin, 14-hydroxydaunomycin, a new antitumor antibiotic from S. peucetius var. caesius». Biotechnol. Bioeng. 11 (6): 1101-10. PMID 5365804. doi:10.1002/bit.260110607.
- ↑ Grimm A, Madduri K, Ali A, Hutchinson CR (1994). «Characterization of the Streptomyces peucetius ATCC 29050 genes encoding doxorubicin polyketide synthase». Gene 151 (1–2): 1-10. PMID 7828855. doi:10.1016/0378-1119(94)90625-4.
- ↑ Dickens ML, Strohl WR (1996). «Isolation and characterization of a gene from Streptomyces sp. strain C5 that confers the ability to convert daunomycin to doxorubicin on Streptomyces lividans TK24». J. Bacteriol. 178 (11): 3389-95. PMID 8655530.
- ↑ Walczak RJ, Dickens ML, Priestley ND, Strohl WR (1999). «Purification, properties, and characterization of recombinant Streptomyces sp. strain C5 DoxA, a cytochrome P-450 catalyzing multiple steps in doxorubicin biosynthesis». J. Bacteriol. 181 (1): 298-304. PMID 9864343.
- ↑ Lomovskaya N, Otten SL, Doi-Katayama Y, et al (1999). «Doxorubicin overproduction in Streptomyces peucetius: cloning and characterization of the dnrU ketoreductase and dnrV genes and the doxA cytochrome P-450 hydroxylase gene». J. Bacteriol. 181 (1): 305-18. PMID 9864344.
- ↑ Hutchinson CR, Colombo AL (1999). «Genetic engineering of doxorubicin production in Streptomyces peuceticus: a review». J. Ind. Microbiol. Biotechnol. 23 (1): 647-52. PMID 10455495. doi:10.1038/sj.jim.2900673.
- ↑ Lown JW (1993). «Anthracycline and anthraquinone anticancer agents: current status and recent developments». Pharmacol. Ther. 60 (2): 185-214. PMID 8022857. doi:10.1016/0163-7258(93)90006-Y.
- ↑ Fornari, F.A.; Randolph, J.K.; Yalowich, J.C.; Ritke, M.K.; Gewirtz, D.A. Interference by Doxorubicin with DNA Unwinding in MCF-7 Breast Tumor Cells. 1994, Molecular Pharmacology, 45, 649 – 656. PMID 8183243.
- ↑ Momparler, R.L.; Karon, M.; Siegel, S.E.; Avila, F. Effect of Adriamycin on DNA, RNA and Protein Synthesis in Cell-Free Systems and Intact Cells. 1976, Cancer Research, 36, 2891 – 2895. PMID 1277199. Free full text
- ↑ Frederick, C.A.; Williams, L.D.; Ughetto, G.; van der Marel, G.A.; van Boom, J.H.; Rich, A.; Wang, A.H. Structural Comparison of Anticancer Drug-DNA Complexes: Adriamycin and Daunomycin. 1990, Biochemistry, 29, 2538 – 2549. PMID 2334681. Crystal structure is available for download as a PDB file.
- ↑ Pigram, W.J.; Fuller, W.; Hamilton, L.D. Stereochemistry of Intercalation: Interaction of Daunomycin with DNA. 1972, Nature New Biology, 235, 17 – 19. PMID 4502404.
- ↑ a b "DOXIL Product Information." Ortho Biotech Products, L.P. Archivado el 21 de septiembre de 2007 en Wayback Machine. Accedido el 19 de abril de 2007.
- ↑ Wendel H, De Stanchina E, Fridman J, Malina A, Ray S, Kogan S, Cordon-Cardo C, Pelletier J, Lowe S (2004). «Survival signalling by Akt and eIF4E in oncogenesis and cancer therapy». Nature 428 (6980): 332-7. PMID 15029198. doi:10.1038/nature02369.
- ↑ Johansson S, Goldenberg D, Griffiths G, Wahren B, Hinkula J (2006). «Elimination of HIV-1 infection by treatment with a doxorubicin-conjugated anti-envelope antibody». AIDS 20 (15): 1911-1915. PMID 16988511. doi:10.1097/01.aids.0000247111.58961.60.
- ↑ Porteiro B, Fondevila MF, Buque X, Gonzalez-Rellan MJ, Fernandez U, Mora A, Beiroa D, Senra A, Gallego R, Fernø J, López M, Sabio G, Dieguez C, Aspichueta P, Nogueiras R (2017). «Pharmacological stimulation of p53 with low-dose doxorubicin ameliorates diet-induced nonalcoholic steatosis and steatohepatitis». Molecular Metabolism 12 (17): 31011-31016. PMID 29290620. doi:10.1016/j.molmet.2017.12.005.
- ↑ Chhikara, B. S.; Jean, N. S.; Mandal, D.; Kumar, A. y col. (2011). «Fatty acyl amide derivatives of doxorubicin: synthesis and in vitro anticancer activities». European Journal of Medicinal Chemistry 46 (6): 2037-2042. «Doxorubicin has been called as “red devil” or “red death” because of its high antibiotic activity and red color.»
- ↑ Sen, R. (2004). Principles and Management of Cancer. Nueva Delhi: B.I. Publications PVT. p. 102. ISBN 81-7225-203-X. Consultado el 20 de diciembre de 2015.
- ↑ Allison, K. (2011). Red Sunshine: A breast cancer specialist learns from life on the other side of the microscope. Ed. Lulu. p. 17. ISBN 978-1-4583-0749-1. Consultado el 20 de diciembre de 2015.
Enlaces externos
editar- Wikimedia Commons alberga una categoría multimedia sobre Doxorrubicina.
- MedlinePlusDrugInfo medmastera682221