Crocodilia
Los crocodilios (Crocodilia) son un orden de grandes reptiles predadores semiacuáticos. El orden incluye a los cocodrilos (familia Crocodylidae), a los gaviales (familia Gavialidae) y a los aligátores y caimanes (familia Alligatoridae). Aunque a menudo se utiliza para referirse a todos ellos, de forma estricta el término 'cocodrilo' se refiere solo a los miembros de la familia Crocodylidae.
| Crocodilios | ||
|---|---|---|
| Rango temporal: Cretácico superior-Reciente | ||
 Izquierda arriba: Cocodrilo marino (Crocodylus porosus); derecha: caimán del Misisipi (Alligator mississippiensis); izquierda abajo: gavial (Gavialis gangeticus) | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Chordata | |
| Subfilo: | Vertebrata | |
| Superclase: | Tetrapoda | |
| Clase: | Sauropsida | |
| Subclase: | Diapsida | |
| Infraclase: | Archosauromorpha | |
| (sin rango): | Archosauria | |
| Superorden: | Crocodylomorpha | |
| Orden: |
Crocodilia Owen, 1842 | |
| Distribución | ||
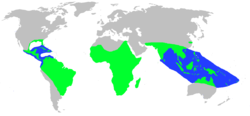 Distribución geográfica | ||
| Subgrupos | ||
| Sinonimia | ||
Crocodylia[1] | ||
Aparecieron durante el Cretácico superior (división Campaniense) hace 83,5 millones de años y son los parientes vivos más próximos de las aves, ya que los dos grupos son los únicos arcosaurios existentes conocidos.
Son reptiles con forma de grandes lagartos, de cuerpo robusto, morro prominente largo y plano, cola comprimida lateralmente y ojos, oídos y fosas nasales en la parte superior de la cabeza. Buenos nadadores, pueden moverse en tierra andando separando el cuerpo de tierra o arrastrando el cuerpo, mientras que las especies de menor tamaño incluso pueden galopar. Su piel es gruesa y está cubierta de escamas que no se superponen. Tienen dientes cónicos, tipo estaca, y una poderosa mordida. El corazón tiene cuatro cámaras y, de forma similar a las aves, un sistema de circulación de aire unidireccional en los pulmones, pero, al igual que otros reptiles, no aviares, son ectotermos.
Se encuentran principalmente en las tierras bajas de la zona intertropical, pero los aligátores también viven en el sureste de los Estados Unidos y en el río Yangtsé en China. Son fundamentalmente carnívoros, se alimentan de animales como peces, crustáceos, moluscos, aves y mamíferos; algunas especies, como el gavial del Ganges (Gavialis gangeticus), tienen una alimentación especializada, mientras que otras, como el cocodrilo marino (Crocodylus porosus), tienen dietas generalizadas. Son animales generalmente solitarios y territoriales, aunque pueden realizar una alimentación cooperativa. Durante la reproducción, los machos dominantes intentan monopolizar las hembras disponibles. Las hembras ponen huevos en agujeros o en montículos y, a diferencia de la mayoría de los demás reptiles, cuidan a sus crías recién nacidas.
Existen ocho especies de crocodilios de las que hay constancia de ataques a humanos, la mayoría por parte del cocodrilo del Nilo (Crocodylus niloticus). Los seres humanos son la mayor amenaza para las poblaciones de este orden de reptiles, fundamentalmente a causa de la caza y la destrucción de su hábitat, aunque la cría en granjas ha reducido en gran medida el comercio ilícito de pieles de animales salvajes. Las representaciones artísticas y literarias de estos reptiles aparecen en las culturas humanas de todo el mundo desde al menos el Antiguo Egipto; la primera mención conocida del mito de que los cocodrilos lloran por sus víctimas fue en el siglo IX, y fue difundido por personajes como Juan de Mandeville en 1400 y posteriormente por autores como William Shakespeare a finales del siglo XVI y principios del XVII.
Etimología
editarDurante décadas se ha utilizado indistintamente Crocodilia y Crocodylia como nombre del orden, empezando por la nueva descripción del grupo realizada por Schmidt a partir del término en desuso Loricata.[2] Schmidt empleó el término más antiguo Crocodilia, basado en el nombre original del grupo que le había asignado Owen.[3] Poco después Wermuth optó por usar Crocodylia como nombre más adecuado para describir el grupo,[4] basándose en el nombre del género tipo Crocodylus (Laurenti, 1768).[5] Dundee, en una revisión de muchos nombres de reptiles y anfibios, argumentó con firmeza en favor de Crocodylia como nombre más adecuado del grupo.[6] Sin embargo, hasta la llegada de la cladística y la clasificación filogenética no se dieron justificaciones más sólidas para optar una ortografía u otra.[7]
Antes de 1988, Crocodilia/Crocodylia era un grupo que comprendía tanto a los animales actuales (el grupo corona) como a sus parientes más lejanos que actualmente están situados en los grupos más grandes Crocodylomorpha y Pseudosuchia.[7] Según esta definición actual, Crocodylia está restringido solo a los antepasados más recientes de los cocodrilos actuales (aligatóridos, crocodílidos y gaviálidos).[7] Esta distinción la hacen fundamentalmente los paleontólogos que estudian la evolución de los cocodrilos, por lo que las ortografías Crocodilia y Crocodylia todavía se utilizan indistintamente en la literatura neontológica.[n 1]
Crocodilia[3] y el nombre común en español 'cocodrilo'[n 2] provienen del latín crocodīlus, y este del griego κροκόδειλος (krokódeilos),[10] que significa lagarto y cocodrilo del Nilo.[11] Crocodylia, tal como lo acuñó Wermuth,[4] por el género Crocodylus, parece que deriva del antiguo griego κρόκη (kroke),[12] 'grava' o 'guijarro', y de δρîλος o δρεîλος (drĩlos), 'lombriz'. El nombre puede referirse al hábito de estos animales de tomar el sol en las riberas de grava del Nilo.[13]
Morfología y fisiología
editarSu tamaño va desde los 1-1,5 m de longitud de las especies de los géneros Paleosuchus y Osteolaemus, hasta los 7 m y 2000 kg de peso del cocodrilo marino (Crocodylus porosus), aunque algunas especies prehistóricas como Deinosuchus, del Cretácico superior, eran todavía más grandes, llegando a alcanzar alrededor de 11 m de longitud y 3450 kg de peso.[14][15] Suelen presentar dimorfismo sexual, con los machos mucho más grandes que las hembras.[16] Aunque con cierta diversidad en la forma del morro y los dientes, todas las especies de este orden tienen esencialmente la misma morfología corporal.[15] Tienen un cuerpo robusto, de forma similar a los lagartos, con morros alargados y aplanados y colas comprimidas lateralmente.[16] Sus extremidades son de tamaño reducido; las patas delanteras tienen cinco dedos sin o con poca o membrana interdigital y las traseras tienen cuatro dedos palmeados y un quinto rudimentario.[17] El esqueleto es típico de los tetrápodos, aunque el cráneo, la pelvis y las costillas son especializados;[16] en concreto, los procesos cartilaginosos de las costillas permiten que el tórax se colapse durante el buceo y la estructura de la pelvis puede acomodar grandes masas de alimentos,[18] o más aire en los pulmones.[19] Ambos sexos tienen cloaca, una única cámara y una salida en la base de la cola en la que se abren los tractos intestinal, urinario y genital.[16] Este alberga el pene en los machos y el clítoris en las hembras;[20] el pene de los crocodilios está permanentemente erecto y depende de los músculos cloacales para la eversión y de ligamentos elásticos y un tendón para el retroceso.[21] Los testículos y los ovarios se encuentran cerca de los riñones.[22]
Los ojos, las orejas y las fosas nasales están situados en la parte superior de la cabeza. Esto les permite acechar a sus presas con la mayor parte del cuerpo bajo el agua.[23] Los ojos cuentan con tapetum lucidum, que mejora la visión en condiciones de poca luz.[17] La vista es bastante buena al aire, pero se debilita significativamente bajo el agua.[24] Mientras que en otros vertebrados la fóvea es generalmente circular, en los crocodilios es una barra horizontal de receptores apretados en medio de la retina. Cuando el animal se sumerge por completo, las membranas nictitantes cubren sus ojos; además, unas glándulas en la membrana nictitante secretan un lubricante salado que mantiene el ojo limpio; cuando salen del agua, esta sustancia se seca y puede confundirse con «lágrimas».[17]
Las orejas están adaptadas para oír tanto en el aire como bajo el agua, y los tímpanos están protegidos por solapas que pueden abrirse o cerrarse mediante músculos.[25] Tienen un amplio margen de audición, con una sensibilidad comparable a la mayoría de las aves y muchos mamíferos.[26] Tienen una sola cámara olfativa y el órgano de Jacobson está ausente en los adultos,[27] lo que indica que toda la percepción olfativa se limita al sistema olfativo. Experimentos conductuales y con olfatómetro indican que detectan sustancias químicas tanto transportadas por el aire como solubles en agua y utilizan su sistema olfativo para cazar. Cuando están sobre el agua, aumentan su capacidad para detectar sustancias olorosas volátiles mediante el bombeo gular, un movimiento rítmico del piso de la faringe.[28][29] Un nervio trigémino bien desarrollado les permite detectar las vibraciones en el agua, como las que producen las presas potenciales.[30] La lengua no puede moverse libremente, sino que se mantiene en su lugar mediante una membrana plegada.[18] Aunque su cerebro es bastante pequeño, son capaces de un mayor aprendizaje que la mayoría de los reptiles.[31] Si bien carecen de las cuerdas vocales de los mamíferos y de la siringe de las aves,[32] los crocodilios pueden producir vocalizaciones al hacer vibrar tres aletas localizadas en la laringe.[33] Parece que han perdido la glándula pineal, pero aún muestran signos de cadencia de melatonina.[34]
Locomoción
editarLos crocodilios son excelentes nadadores; durante la locomoción acuática, su musculada cola realiza un movimiento ondular de lado a lado para impulsar al animal a través del agua, manteniendo las patas cerca del cuerpo para reducir el arrastre.[23][35] Cuando el animal necesita detenerse, maniobrar o avanzar en una dirección diferente, lo hace extendiendo las patas.[23] Generalmente nadan lentamente en la superficie o bajo el agua con suaves movimientos sinuosos de la cola, pero cuando son perseguidos o cuando persiguen a sus presas, pueden moverse con rapidez.[36] No están tan bien adaptados para moverse en tierra; a diferencia de la mayoría de los reptiles, tienen dos formas de locomoción terrestre distintas: el «paso alto» y el «paso bajo».[17] Las articulaciones del tobillo se flexionan de forma diferente a las de otros reptiles, una característica que comparten con algunos de los primeros arcosaurios. Uno de los huesos superiores del tobillo, el astrágalo, se mueve con la tibia y el peroné. El otro, el calcáneo, es funcionalmente parte del pie y tiene un alvéolo en el que se ajusta una proyección del astrágalo. El resultado es que las patas se pueden mantener casi verticalmente debajo del cuerpo cuando están en tierra, y el pie puede girar durante la locomoción con un movimiento giratorio del tobillo.[37]
El paso alto, con el vientre y la mayor parte de la cola separada del suelo, es una característica distintiva de este orden entre los reptiles actuales. Tiene cierto parecido con el andar de los mamíferos cuadrúpedos, con la misma secuencia de movimientos de las extremidades: anterior izquierda, posterior derecha, anterior derecha, posterior izquierda.[36] El paso bajo es similar al alto, pero sin elevar el cuerpo, aunque es bastante similar al caminar reptante de salamandras y lagartos. Pueden cambiar instantáneamente de una forma de desplazamiento a la otra, pero el paso alto es el medio habitual de locomoción en tierra. El animal puede elevar el cuerpo y usar esta forma inmediatamente, o puede dar uno o dos pasos bajos antes de elevar el cuerpo. A diferencia de la mayoría de los vertebrados terrestres, cuando los crocodilios elevan su ritmo de desplazamiento, aumentan la velocidad a la que la mitad inferior de cada pata (en lugar de la pata entera) se mueve hacia adelante; de esta manera, la longitud de la zancada se incrementa mientras que la duración de la zancada disminuye.[38]
Aunque por lo general son lentos en tierra, pueden realizar breves carreras y algunos alcanzan velocidades de 12 a 14 km/h en distancias cortas.[39] Pueden efectuar una rápida entrada en el agua desde un terreno fangoso echándose al suelo y moviendo el cuerpo de un lado a otro y extendiendo las patas.[36][39] En algunas especies pequeñas, como el cocodrilo australiano de agua dulce (Crocodylus johnsoni), el paso en carrera puede llegar a un galope a saltos, lo que implica que las extremidades posteriores lanzan el cuerpo hacia adelante y las anteriores pasan a soportar el peso; a continuación, las extremidades posteriores se balancean hacia adelante a medida que la columna vertebral se flexiona dorsoventralmente, repitiéndose esta secuencia de movimientos.[40] Durante su desplazamiento en tierra pueden mantener el dorso y la cola derechos, ya que las escamas de la piel están unidas a las vértebras por músculos.[18] Ya sea en tierra o en el agua, pueden saltar presionando la cola y las patas traseras contra el sustrato y empujando.[23][41]
Mandíbulas y dientes
editarLa forma del hocico varía según la especie. Los cocodrilos pueden tener hocicos anchos o delgados, mientras que los de los caimanes y aligátores son en su mayoría anchos. Los gaviales tienen hocicos muy estrechos y alargados. Los músculos que cierran las mandíbulas son mucho más gruesos y poderosos que los que las abren.[16] Las mandíbulas pueden ser cerradas por una persona con bastante facilidad, pero son extremadamente difíciles de abrir.[42] Los potentes músculos de cierre se unen en la porción media de la mandíbula inferior, y la articulación de la mandíbula se une a la articulación atlantooccipital, lo que permite que el animal pueda abrir mucho la boca.[18]
Tienen una fuerza de mordida de las más poderosas del reino animal. En un estudio publicado en 2003 se midió la fuerza de mordedura de un caimán del Misisipi que alcanzó los 9450 N.[43] En un estudio de 2012 la fuerza de mordida de un cocodrilo de agua salada fue todavía mayor, alcanzando 16 000 N; este estudio no encontró correlación entre la fuerza de mordida y la forma del hocico. Sin embargo, las mandíbulas extremadamente delgadas del gavial son relativamente débiles y más adecuadas para el cierre rápido de la mandíbula. La fuerza de mordedura de Deinosuchus pudo haber llegado a los 100 000 N,[15] superior incluso a la de dinosaurios terópodos, como Tyrannosaurus.[43]
Sus dientes varían desde romos y comprimidos hasta agudos y con forma de aguja.[15] Las especies de hocico ancho tienen dientes de distintos tamaños, mientras que las de hocico delgado son más uniformes. Los dientes de cocodrilos y gaviales tienden a ser más visibles que los de caimanes y aligátores cuando las mandíbulas están cerradas.[44] La forma más fácil de distinguir cocodrilos de caimanes es mirando la línea de la mandíbula. Los dientes de la mandíbula inferior de un aligátor encajan en cavidades de la mandíbula superior, por lo que cuando la boca está cerrada, solo son visibles los dientes superiores. Los dientes de la mandíbula inferior de un cocodrilo encajan en cavidades en la parte exterior de la mandíbula superior, con lo que cuando la boca está cerrada, son visibles tanto los dientes superiores como los inferiores.[45]
Los crocodílios son polifiodontos[n 3] y pueden reemplazar cada uno de sus aproximadamente 80 dientes hasta 50 veces en su ciclo de vida de 35 a 75 años.[48] Son los únicos vertebrados no mamíferos con alvéolos dentarios.[49] Junto a cada diente completamente desarrollado hay un pequeño diente de reemplazo y una célula madre odontogénica en la lámina dental en espera, que se puede activar cuando sea necesario.[50] A medida que el animal envejece, el reemplazo de dientes se ralentiza en grado significativo y finalmente se detiene.[44]
Piel
editarLa piel es gruesa y queratinizada y está revestida de escamas no superpuestas conocidas como escudos, dispuestos en filas y patrones regulares. Estas escamas se producen continuamente por división celular en la capa inferior de la epidermis, la capa basal, y la superficie de los escudos individuales se desprende periódicamente. La superficie exterior de los escudos está compuesta de beta-queratina relativamente rígida, mientras que la región articular entre los escudos contiene solo alfa-queratina, más flexible.[51]
Muchos de los escudos están reforzados con placas óseas conocidas como osteodermos, que son del mismo tamaño y forma que las escamas superficiales, pero se desarrollan debajo de ellas. Son más numerosas en el dorso y el cuello y pueden formar una armadura protectora. A menudo tienen crestas prominentes y ásperas cubiertas de beta-queratina resistente.[16] La mayor parte de la piel de la cabeza está fusionada al cráneo.[18] La piel del cuello y los flancos está floja, mientras que la del abdomen y la parte inferior de la cola está envuelta en escudos cuadrados planos y grandes dispuestos en hileras proporcionadas.[16][52] Los escudos contienen vasos sanguíneos y pueden absorber o irradiar calor durante la termorregulación.[16] Algunos estudios también sugieren que los iones alcalinos liberados en la sangre, procedentes del calcio y el magnesio de estos huesos dérmicos, actúan como una disolución reguladora durante las inmersiones prolongadas, cuando el aumento de los niveles de dióxido de carbono podría causar acidosis.[53]
Algunos escudos contienen un poro conocido como órgano sensorial tegumentario; cocodrilos y gaviales los tienen en gran parte de sus cuerpos, mientras que caimanes y aligátores solo los tienen en la cabeza. No se comprende del todo su función exacta, pero se cree que pueden ser órganos mecanosensoriales,[54] o que puedan producir una secreción oleosa que evite que el barro se adhiera a la piel. Hay prominentes glándulas tegumentarias pares en los pliegues de la piel de la garganta y otras en las paredes laterales de la cloaca, sobre las que se han propuesto varias funciones, como que pueden desempeñar un papel en la comunicación, ya que evidencias indirectas sugieren que secretan feromonas utilizadas en el cortejo o el anidamiento.[16] La piel de los crocodilios es dura y puede resistir daños de conespecíficos, y su sistema inmunitario es lo suficientemente eficaz como para curar las heridas en unos días.[55]
Sistema circulatorio
editarLos crocodilios puede que tengan el sistema circulatorio más complejo de todos los vertebrados. Tienen un corazón de cuatro cámaras y dos ventrículos, algo inusual entre los reptiles actuales,[56] y una aorta izquierda y otra derecha que están conectadas por un orificio denominado foramen de Panizza.[n 4] Al igual que las aves y los mamíferos, tienen válvulas cardíacas que dirigen el flujo sanguíneo en una sola dirección a través de las cámaras del corazón. También tienen unas singulares válvulas dentadas que, cuando se unen, dirigen la sangre hacia la aorta izquierda y fuera de los pulmones, y luego de vuelta al cuerpo.[60] Este sistema circulatorio puede que permita que permanezcan sumergidos por más tiempo,[61] aunque esta explicación ha sido cuestionada.[62] Otras posibles razones para explicar su peculiar aparato circulatorio pueden ser la asistencia a sus necesidades de termorregulación, la prevención de los edemas pulmonares o una recuperación más rápida de la acidosis metabólica. Retener el dióxido de carbono dentro del cuerpo permite incrementar la tasa de secreción de ácido gástrico, mejorando así la eficiencia de la digestión y haciendo más eficientes otros órganos gastrointestinales, como el páncreas, el bazo, el intestino delgado y el hígado.[63]
Cuando se sumergen, la frecuencia cardíaca disminuye a uno o dos latidos por minuto y se reduce el flujo de sangre a los músculos. Cuando salen a la superficie y toman aire, el ritmo cardíaco se acelera en segundos y los músculos reciben sangre recién oxigenada.[64] A diferencia de muchos mamíferos marinos, los crocodilios tienen poca mioglobina para almacenar oxígeno en sus músculos. Durante el buceo, los músculos reciben oxígeno cuando un incremento en la concentración de iones de bicarbonato hace que la hemoglobina de la sangre libere oxígeno.[65]
Sistema respiratorio
editarTradicionalmente se creyó que los crocodilios respiraban como los mamíferos, esto es, con un flujo de aire entrando y saliendo de forma mareal,[n 5] pero unos estudios publicados en 2010 y 2013 concluyen que en realidad respiran de forma más parecida a la de las aves, con el flujo de aire moviéndose en un circuito unidireccional dentro de los pulmones. Cuando un crocodilio inhala, el aire fluye a través de la tráquea hacia dos bronquios primarios, o vías respiratorias, que se bifurcan en pasadizos secundarios más angostos; el aire continúa moviéndose a través de estos y luego a vías aéreas terciarias aún más estrechas y después a otras vías respiratorias secundarias por las que no pasara la primera vez. Finalmente el aire fluye de regreso a las vías respiratorias primarias y se exhala. Estas válvulas aerodinámicas dentro del árbol bronquial se han propuesto como explicación de cómo los crocodilios pueden tener un flujo de aire unidireccional sin la ayuda de los sacos aéreos de las aves.[67][68]
Los pulmones están unidos al hígado y la pelvis por el músculo diafragmático (análogo al diafragma de los mamíferos). Durante la inhalación, los músculos intercostales externos expanden las costillas, lo que permite que el animal tome más aire, mientras que el músculo isquiopubiano hace que las caderas giren hacia abajo y empujen el vientre hacia afuera y el músculo diafragmático tira del hígado hacia atrás. Al exhalar, los músculos intercostales internos empujan las costillas hacia adentro, mientras que el músculo recto abdominal empuja las caderas y el hígado hacia adelante y el vientre hacia adentro.[19][56][69][70] Debido a que los pulmones se expanden en el espacio que anteriormente ocupaba el hígado y se comprimen cuando vuelve a su posición original, este movimiento a veces se denomina «pistón hepático». Los crocodilios también pueden usar estos músculos para ajustar la posición de sus pulmones, controlando así su flotabilidad en el agua. El animal se hunde cuando tira de los pulmones hacia la cola y flota cuando los mueven hacia la cabeza; esto les permite moverse a través del agua sin crear perturbaciones que puedan alertar a presas potenciales. Además, también pueden girar y retorcerse moviendo los pulmones lateralmente.[69]
Mientras nadan y bucean parece que utilizan la capacidad pulmonar más para la flotabilidad que para el almacenamiento de oxígeno.[56] Justo antes de sumergirse, el animal exhala aire para reducir su volumen pulmonar y conseguir una flotabilidad negativa.[71] Cuando se sumergen, las fosas nasales se cierran herméticamente.[17] Todas las especies de este orden tienen una válvula palatal, una solapa membranosa de piel en la parte posterior de la cavidad bucal que impide que el agua fluya hacia la garganta, el esófago y la tráquea,[16][17] lo que les permite abrir la boca bajo el agua sin ahogarse.[17] Suelen permanecer bajo el agua durante quince minutos o menos, pero algunas especies pueden contener la respiración hasta dos horas en condiciones ideales.[72] Se desconoce la profundidad máxima que pueden alcanzar, pero los cocodrilos pueden sumergirse a por lo menos 20 m.[73]
Sistema digestivo
editarSus dientes están adaptados para atrapar y sujetar presas y tragan los alimentos sin masticar. El tracto digestivo es relativamente corto, ya que la carne es una sustancia bastante fácil de digerir. El estómago se divide en dos partes: una molleja muscular que tritura la comida y una cámara digestiva donde las enzimas actúan sobre ella.[74] El estómago es más ácido que el de cualquier otro vertebrado y contiene rugosidades para gastrolitos, que juegan un papel importante en la trituración y descomposición mecánica de los alimentos. La digestión se produce más rápidamente a temperaturas más elevadas.[23] Los crocodilios tienen una tasa metabólica muy baja, por lo que tienen bajos requerimientos energéticos, lo que les permite sobrevivir durante muchos meses con una única comida abundante, digiriendo la comida lentamente. Pueden soportar un ayuno prolongado, manteniéndose de la grasa almacenada entre comidas. Incluso los recién nacidos pueden sobrevivir unos 58 días sin comida, perdiendo el 23 % de su peso corporal durante este tiempo.[75] Un cocodrilo adulto necesita entre una décima y un quinta parte de la cantidad de alimento necesaria para un león del mismo peso, y puede vivir durante seis meses sin comer.[75]
Termorregulación
editarLos crocodilios son ectotermos, producen relativamente poco calor internamente y dependen de fuentes externas para elevar la temperatura de su cuerpo. El calor del sol es su principal medio de calentamiento; la inmersión en agua también puede elevar su temperatura por conducción o enfriar al animal cuando hace calor. El principal método para regular su temperatura es conductual. Por ejemplo, un aligátor de regiones templadas puede comenzar el día tomando el sol en tierra. Un animal voluminoso se calienta lentamente, pero más tarde se mueve hacia el agua, donde sigue exponiendo su dorso al sol; por la noche permanece sumergido y su temperatura baja lentamente. El período de descanso se extiende en invierno y se reduce en verano. En cambio, para los cocodrilos de los trópicos por lo general su mayor problema es evitar el sobrecalentamiento; pueden tomar durante un rato el sol por la mañana, pero luego se ponen a la sombra, permanezcan allí el resto del día o se sumerjan en agua para mantenerse frescos. Permanecer con la boca abierta puede proporcionar enfriamiento por evaporación de líquidos del revestimiento de la boca.[76] Mediante estos procedimientos los crocodilios consiguen un rango de temperatura corporal que varía entre 25 y 35 °C, manteniéndose generalmente en el rango de 30 a 33 °C.[77]
La distribución geográfica del caimán del Misisipi y el aligátor chino se extienden a regiones que en ocasiones experimentan períodos de heladas en invierno. Al ser ectotermos, su temperatura corporal interna disminuye a medida que desciende la temperatura exterior y se vuelven lentos. Pueden volverse más activos en días cálidos, pero generalmente no se alimentan durante el invierno. Con tiempo frío permanecen sumergidos manteniendo la cola en aguas más profundas y menos frías y con la cabeza hacia arriba asomando solo las fosas nasales en la superficie. Si se forma hielo en el agua, mantienen agujeros para respirar libres de hielo, y ha habido ocasiones en que sus hocicos se congelaron en el hielo. Mediante unas sondas de detección de temperatura implantadas en caimanes del Misisipi salvajes se ha descubierto que su temperatura corporal interna puede descender a alrededor de 5 °C, pero mientras puedan respirar no muestran efectos negativos cuando el tiempo se hace más cálido.[76]
Osmorregulación
editarNinguna especie viviente de crocodilios puede considerarse verdaderamente marina. Aunque el llamado cocodrilo marino (Crocodylus porosus) y el caimán del Misisipi pueden nadar en el mar, sus hábitats habituales son desembocaduras de ríos, estuarios, manglares y lagos hipersalinos. Sin embargo varias especies extintas han tenido hábitats marinos, como el recientemente extinto Ikanogavialis papuensis, que vivía en un hábitat totalmente marino en las costas de las islas Salomón.[78] Todos los crocodilios necesitan mantener la concentración de sal en los fluidos corporales a niveles adecuados. La osmorregulación está relacionada con la cantidad de sales y agua intercambiada con el medio ambiente. La absorción de agua y sales tiene lugar a través del revestimiento de la boca, cuando beben agua, incidentalmente durante la alimentación y cuando está presente en los alimentos.[79] El cuerpo pierde agua durante la respiración y pierden tanto sales como agua en la orina y las heces, a través de la piel y a través de glándulas excretoras de sal situadas en la lengua, aunque solo están presentes en cocodrilos y gaviales.[80][81] La piel es una barrera muy efectiva tanto para el agua como para los iones. Abriendo la boca consiguen pérdida de agua por evaporación del revestimiento bucal, y en tierra también se pierde agua a través de la piel.[80] Los animales grandes mantienen mejor la homeostasis en momentos de estrés osmótico que los más pequeños.[82] Los recién nacidos son mucho menos tolerantes a la exposición al agua salada que los juveniles de más edad, presumiblemente porque tienen una mayor relación superficie-volumen.[80]
Los riñones y el sistema excretor son muy parecidos a los de otros reptiles, pero los crocodilios no tienen vejiga urinaria. En agua dulce, la osmolalidad (la concentración de solutos que contribuyen a la presión osmótica de una solución) en el plasma sanguíneo es mucho más alta que en el agua circundante. Los animales están bien hidratados, la orina en la cloaca es abundante y diluida y el nitrógeno se excreta en forma de bicarbonato de amonio.[82] La pérdida de sodio es baja y se produce principalmente a través de la piel en condiciones de agua dulce. En agua de mar ocurre lo opuesto. La osmolalidad en el plasma es menor que el agua circundante, lo que le produce un efecto deshidratante; la orina cloacal es mucho más concentrada, blanca y opaca y el residuo nitrogenado se excreta principalmente como ácido úrico insoluble.[80][82]
Ecología y ciclo biológico
editarSon reptiles de vida anfibia que pasan parte del tiempo en el agua y parte en tierra. El último género completamente terrestre, Mekosuchus, se extinguió hace unos 3000 años tras la llegada de los humanos a las islas del Pacífico donde vivían, por lo que su extinción posiblemente sea antropogénica.[83] Por lo general viven en la zona intertropical, aunque el caimán del Misisipi y el aligátor chino llegan tan al norte de los trópicos como el sudeste de Estados Unidos y el río Yangtze, respectivamente. Florida, en los Estados Unidos, es el único lugar donde conviven aligátores y cocodrilos.[84] La mayoría viven en tierras bajas y se encuentran pocas especies por encima de los 1000 metros, donde las temperaturas por lo general están en torno a 5 °C más bajas que en la costa. Ninguna especie vive permanentemente en el mar, aunque algunas pueden aventurarse en él y varias pueden tolerar el agua salobre de los estuarios, los manglares y la extrema salinidad de los lagos hipersalinos.[85] El Cocodrilo marino tiene la distribución más extensa de todos los crocodilios, con un rango que se extiende desde el este de la India hasta Nueva Guinea y el norte de Australia. Gran parte de su éxito se debe a su capacidad para nadar por el mar y colonizar nuevos lugares, aunque su hábitat no se restringe al medio ambiente marino y pasa mucho tiempo en estuarios, ríos y grandes lagos.[86]
Viven en distintos hábitats acuáticos. Algunas especies son relativamente más terrestres y prefieren los pantanos, las lagunas y las riberas de los lagos, donde pueden tomar el sol y hay abundancia de plantas que sustentan una fauna variada. Otros pasan más tiempo en el agua y viven en los tramos inferiores de ríos, manglares y estuarios. Estos hábitats también tienen una flora rica y proporcionan mucha comida. Los gaviales asiáticos encuentran los peces de los que se alimentan en las charcas y remansos de ríos rápidos. Los caimanes de Cuvier de Sudamérica habitan corrientes frías y rápidas, a menudo cerca de cascadas, y otros caimanes viven en lagos más cálidos y turbulentos y en ríos de corriente lenta. Los cocodrilos viven generalmente en los ríos, y el aligátor chino se encuentra en ríos lentos y turbios que discurren a través de las llanuras inundables de China. El caimán del Misisipi es una especie adaptable y habita pantanos, ríos o lagos con agua clara o turbia.[85] Los factores climáticos también afectan a su distribución a nivel local. Durante la estación seca, los caimanes pueden restringirse a charcas profundas en los ríos durante varios meses; en la estación lluviosa, gran parte de la sabana en los Llanos venezolanos se inunda y se dispersan a través de la llanura.[87] Los cocodrilos del desierto en Mauritania se han adaptado a su ambiente árido permaneciendo en cuevas o madrigueras en estado de estivación durante los períodos más secos; cuando llueve, estos cocodrilos se reúnen en gueltas.[88]
La tierra seca también es importante para los miembros de este orden, ya que les brinda oportunidades para tomar el sol, hacer los nidos y resguardarse de temperaturas extremas. Abriendo la boca consiguen la evaporación de la humedad del revestimiento bucal, lo que tiene un efecto refrescante, y algunas especies hacen uso de madrigueras poco profundas en tierra para mantenerse frescos. Revolcarse en barro también puede ayudar a evitar que se sobrecalienten.[89] Cuatro especies de crocodilios pueden trepar a los árboles para tomar el sol en áreas que carecen de costa.[90] El tipo de vegetación que bordea los ríos y lagos en los que viven los crodilios es en su mayoría bosque tropical húmedo, con manglares en áreas de estuarios. Estos bosques son de gran importancia para ellos, pues son microhábitats adecuados donde pueden prosperar. Las raíces de los árboles absorben agua cuando llueve y la liberan lentamente al medio ambiente. Cuando se talan los bosques para dar paso a la agricultura, los ríos tienden a sedimentarse, el agua discurre rápidamente, los cursos de agua pueden secarse en la estación seca y puede haber inundaciones en la estación húmeda. La destrucción del hábitat forestal es probablemente una amenaza mayor para los crocodilios que la caza.[91]
Territorialidad
editarLos adultos por lo general son animales territoriales y solitarios. Pueden defender los lugares donde toman el sol, zonas de anidación, áreas de alimentación, guarderías y sitios donde pasar el invierno. Los cocodrilos marinos macho establecen territorios durante todo el año que incluyen varios lugares de anidación de las hembras. Algunas especies son ocasionalmente gregarias, especialmente durante las sequías, cuando varios individuos se reúnen en los escasos sitios con agua que quedan. Algunas especies pueden compartir lugares para tomar el sol en ciertos momentos del día.[23]
Alimentación
editarSon animales fundamentalmente carnívoros. Las dietas de las distintas especies pueden variar en función de la forma del hocico y la agudeza de los dientes. Las especies con dientes afilados y hocicos largos y delgados, como el gavial y el cocodrilo australiano de agua dulce, están especializados en alimentarse de peces, insectos y crustáceos, mientras que especies de hocico muy ancho con dientes romos, como el aligátor chino y el yacaré overo, se especializaron en comer moluscos de caparazón duro. Las especies cuyos hocicos y dientes están entre estas dos formas, como el cocodrilo marino y el caimán del Misisipi, tienen dietas generalistas y se alimentan de manera oportunista de invertebrados, peces, anfibios, otros reptiles, aves y mamíferos.[15][92] Aunque esencialmente carnívoras, se ha observado que varias especies consumen fruta, lo que puede desempeñar un papel en la dispersión de semillas.[93]
En general son depredadores de acecho y emboscada,[15] aunque las estrategias de caza varían dependiendo de la especie y de la presa que cacen.[23] A las presas terrestres las acechan desde el borde del agua y luego las atrapan y ahogan.[23][94] Los gaviales y otras especies piscívoras hacen un movimiento de barrido con las mandíbulas de un lado a otro para atrapar presas e incluso pueden saltar del agua para atrapar pájaros, murciélagos y peces saltadores.[92] A las presas pequeñas pueden matarlas de un latigazo cervical (rotura de cuello) cuando el depredador sacude con fuerza la cabeza.[94] Los caimanes usan la cola y el cuerpo para agrupar y dirigir los peces hacia aguas poco profundas.[23] También pueden excavar en busca de invertebrados que habitan en los fondos,[17] y el caimán frentiplano incluso caza en tierra.[15] Se ha observado que algunas especies utilizan palos y ramas para atraer a aves que están construyendo su nido.[95] Hay constancia de que los cocodrilos del Nilo cazan cooperativamente,[23] y varios individuos pueden alimentarse del mismo cadáver. La mayoría de las especies comerán cualquier cosa adecuada que esté a su alcance y también son carroñeros oportunistas.[17]
Los crocodilios no pueden masticar y tienen que tragar los alimentos enteros, por lo que deben despedazar las presas que son demasiado grandes para tragarse. Cuando son incapaces de dar cuenta de un animal grande con una piel gruesa, pueden esperar hasta que se pudra y se pueda despedazar más fácilmente.[92] Para arrancar un trozo de tejido de un cadáver grande, los crocodilios giran su cuerpo continuamente mientras lo sostienen con sus mandíbulas.[96] Durante la caza cooperativa, algunos individuos pueden aferrarse a la presa, mientras que otras realizan el giro; los animales participantes no pelean entre ellos y cada uno se retira con un pedazo de carne y espera su próximo turno de alimentación.[97] Por lo general consumen su presa con la cabeza fuera del agua. Sostienen la comida con la punta de las mandíbulas, la lanzan hacia la parte posterior de la boca con una sacudida hacia arriba de la cabeza y luego se la tragan.[94] Los cocodrilos del Nilo pueden almacenar cadáveres bajo el agua para su consumo posterior.[17]
Reproducción y crianza
editarLos crodilios son generalmente poligínicos y los machos tratan de aparearse con tantas hembras como puedan,[98] aunque hay constancia de apareamientos monógamos en especies como el cocodrilo del Misisipi.[99] Los machos dominantes patrullan y defienden territorios que contienen varias hembras. Los machos de algunas especies, como el caimán del Misisipi, intentan atraer a las hembras con elaboradas exhibiciones de cortejo. Durante el cortejo, los machos y las hembras pueden frotarse entre sí, dar vueltas alrededor y realizar exhibiciones de natación. Por lo general la cópula se realiza en el agua. Cuando una hembra está lista para aparearse, arquea la espalda mientras sumerge la cabeza y la cola; el macho roza el cuello de la hembra y luego la sujeta con sus extremidades posteriores, colocando su cola debajo de la de ella para que sus cloacas se alineen y pueda insertarle su pene. El apareamiento puede durar hasta 15 minutos, tiempo durante el cual la pareja se sumerge y emerge continuamente.[98] Aunque los machos dominantes suelen monopolizar a las hembras reproductoras, se sabe que existe una paternidad múltiple en los caimanes del Misisipi, especie en la que hasta tres machos diferentes pueden engendrar crías en una única puesta. Un mes después del apareamiento, la hembra comienza a construir un nido.[23]
Dependiendo de la especie, para hacer sus nidos las hembras pueden escarbar agujeros o formar montículos a base de vegetación, arena, o tierra.[23][82] Los nidos generalmente se encuentran cerca de sus madrigueras o cuevas. A veces los nidos construidos por distintas hembras se encuentran bastante cerca unos de otros, sobre todo en especies que anidan en agujeros. La cantidad de huevos de cada puesta oscila entre diez y cincuenta; tienen una cáscara dura compuesta de carbonato de calcio. El período de incubación es de dos a tres meses.[23] La temperatura a la que incuban los huevos determina el sexo de las crías; nidos con temperaturas constantes por encima de 32 °C producen más machos, mientras que las que están por debajo de los 31 °C producen más hembras. Sin embargo los nidos están sujetos a cambios en la temperatura y el sexo de los crocodilios se puede determinar en un intervalo corto, por lo que la mayoría de los nidos naturales producen crías de ambos sexos, aunque también puede haber nidadas de un solo sexo.[82]
Todas las crías pueden nacer en una sola noche.[100] Los crocodilios son un caso inusual entre los reptiles por la cantidad de cuidados que proporcionan a las crías.[23] La madre ayuda a las crías a salir de entre la tierra del nido y las lleva al agua en su boca. Los recién nacidos se reúnen y se mantienen cerca de su madre.[101] En el caso del caimán de anteojos de los Llanos venezolanos, hay constancia de que varias madres dejan a sus crías en una misma guardería al cuidado una de las madres.[102] Las crías de muchas especies tienden a tomar el sol en grupo durante el día y se dispersan al anochecer para alimentarse.[100] El tiempo que tardan los jóvenes en independizarse es variable; en el caso del caimán del Misisipi los grupos de jóvenes se asocian con los adultos durante uno o dos años, mientras que los juveniles del cocodrilo marino y del cocodrilo del Nilo se independizan en unos pocos meses.[23]
Comunicación
editarLa interacción social de un crocodilio comienza cuando todavía está en el huevo, porque las crías comienzan a comunicarse entre sí antes de que nazcan. Se ha comprobado que un ligero golpeteo cerca del nido será repetido por la cría, uno tras otro. Esta temprana comunicación puede ayudarlos a eclosionar simultáneamente. Una vez que ha salido del huevo, la cría emite gritos y gruñidos, ya sea espontáneamente o como resultado de estímulos externos, e incluso los adultos no emparentados responden rápidamente a las llamadas de auxilio de los jóvenes.[100]
Cuando los jóvenes se dispersan las vocalizaciones son frecuentes, y de nuevo cuando se congregan por la mañana. Los adultos cercanos, presumiblemente los padres, también dan señales de advertencia de la presencia de depredadores o alertan a los jóvenes sobre la presencia de posibles alimentos. El rango y la cantidad de vocalizaciones varían de una especia a otra. Los aligátores son los más ruidosos, mientras que algunas especies de cocodrilos son casi completamente silenciosas. Las hembras adultas de cocodrilos del cocodrilo de Nueva Guinea y el cocodrilo siamés rugen cuando se les acerca otro adulto, mientras que los cocodrilos del Nilo gruñen o braman en una situación similar. El caimán del Misisipi es excepcionalmente ruidoso; emite una serie de aproximadamente siete bramidos guturales, cada uno de unos segundos de duración, en intervalos de diez segundos. También hace varios gruñidos y silbidos.[100] Los machos crean vibraciones en el agua para enviar señales infrasónicas que sirven para atraer a las hembras e intimidar a los rivales.[103] La gran protuberancia del extremo del morro del gavial macho puede servir como un resonador de sonido.[104]
Otra forma de comunicación acústica es el golpe de cabeza. Normalmente se inicia con un animal en el agua que eleva su hocico y permanece quieto; después de un tiempo, abre las mandíbulas bruscamente y luego las cierra con un movimiento como si fuera a morder que produce un sonido de golpe, seguido inmediatamente por un fuerte chasquido, después de lo cual puede sumergir la cabeza y producir copiosas burbujas. Algunas especies luego rugen, mientras que otras golpean el agua con sus colas. Los episodios de golpes de cabeza se extendieron por todo el grupo; su propósito varía, pero parece estar asociado con el mantenimiento de las relaciones sociales y también se usa durante el cortejo.[100] Los individuos dominantes también pueden exhibir su tamaño mientras nadan en la superficie del agua, y un subordinado se somete situando la cabeza en un ángulo agudo con las fauces abiertas antes de retirarse bajo el agua.[23]
Desarrollo y mortalidad
editarEl porcentaje de mortalidad de las crías y los huevos es elevado; los nidos se enfrentan a amenazas como inundaciones, sobrecalentamiento y depredadores.[23] Las crecidas son una de las principales causas de fracaso reproductivo entre los crocodilios, ya que al inundarse los nidos los embriones en desarrollo se ven privados de oxígeno y los juveniles son arrastrados por el agua.[91] Numerosos depredadores, tanto mamíferos como reptiles, pueden atacar sus nidos y comerse los huevos.[105][106] A pesar del cuidado materno que reciben, las crías suelen ser víctimas de la depredación.[107] Mientras la hembra está transportando a algunos al área de crianza, los demás son atrapados por depredadores que acechan cerca del nido. Además de los depredadores terrestres, las crías también sufren ataques acuáticos por parte de los peces. Las aves rapaces también los tienen entre sus presas. Por otra parte, también puede haber individuos con malformaciones que es poco probable que sobrevivan.[105] En el norte de Australia, la tasa de supervivencia de las crías de cocodrilo marino es solo del 25 %, aunque con cada año de vida subsiguiente el porcentaje mejora, alcanzando el 60 % en el quinto año.[107]
Las tasas de mortalidad son bastante bajas entre subadultos y adultos, aunque ocasionalmente son víctimas de grandes félidos y serpientes.[107] El jaguar y la nutria gigante pueden alimentarse en ocasiones de caimanes en América del Sur.[108][109] En otras partes del mundo, los elefantes y los hipopótamos pueden matar cocodrilos como autodefensa.[23] Existe discrepancia entre los estudiosos en cuanto a si se produce mucho canibalismo entre los crocodilios. Los adultos normalmente no comen su propia descendencia, pero hay evidencias de que los subadultos se alimentan de juveniles y de adultos que atacan a subadultos. Entre los cocodrilos del Nilo, los machos rivales a veces se matan entre sí durante la temporada de cría.[105]
El crecimiento de las crías y los jóvenes depende de la disponibilidad de comida, y la madurez sexual está más ligada al tamaño que a la edad. Las hembras del crocodilo marino alcanzan la madurez cuando tienen entre 2,2 y 2,5 m, los machos con 3 m. Los cocodrilos australianos de agua dulce tardan diez años en alcanzar la madurez, con 1,4 m de longitud. El caimán de anteojos madura antes, cuando alcanza 1.2 m, cuando tiene entre cuatro y siete años.[98] Los crocodilios continúan creciendo a lo largo de toda su vida. Los machos, en particular, continúan aumentando de peso a medida que envejecen, aunque sobre todo más a un aumento de grosor que de longitud.[110] Pueden vivir entre 35 y 75 años,[48] y su edad puede determinarse por los anillos de crecimiento de sus huesos.[98][110]
Importancia ecológica
editarComo depredadores altamente eficientes, por lo general están el lo más alto de la cadena trófica en sus hábitats acuáticos.[92]
Los montículos de los nidos construidos por algunas especies de crocodilios son utilizados por otros animales para sus propios fines; los del caimán del Misisipi son utilizados por las tortugas y las serpientes, tanto para tomar el sol como para desovar. La tortuga de vientre rojo de Florida utiliza los montículos para depositar sus huevos, que se desarrollarán junto con los del propietario.[111] Los crocodilios modifican algunos hábitats de humedales de llanuras como los Everglades mediante la construcción de pequeños estanques conocidos como «agujeros de cocodrilo», que crean hábitats más húmedos o más secos para otros organismos, como plantas, peces, invertebrados, anfibios, reptiles y mamíferos. En las depresiones de piedra caliza de los pantanos de árboles Taxodium, los agujeros de cocodrilo tienden a ser grandes y profundos. En las praderas de marga y calveros rocosos son generalmente pequeños y poco profundos, mientras que en depresiones de turba de ciénagas y humedales pantanosos son más variables. Los agujeros hechos por el hombre no parecen tener tanto efecto.[112]
En la cuenca del río Amazonas, cuando los caimanes escasearon a causa de la caza excesiva a mediados del siglo XX, el número de peces locales, como la importante arapaima, también disminuyó. Estas aguas son pobres en nutrientes y la orina y las heces de los caimanes pueden haber aumentado la producción primaria al aportar nutrientes a las plantas, por lo que la presencia de estos reptiles podría haber beneficiado a la población de peces,[113] pues el número de cocodrilos en un tramo de agua parece estar correlacionado con la población de peces.[114]
Evolución y clasificación
editarEvolución
editarLa principal característica distintiva de los tetrápodos diápsidos es la presencia de dos aberturas (fosa temporal) a cada lado del cráneo detrás de los ojos. Los diápsidos vivos incluyen todos los crocodilios, lagartos, serpientes, tuátaras y aves.[115] La característica que distinguen a los arcosaurios de otros diápsidos son un par de aberturas adicionales en el cráneo (fosa anteorbital) frente a las cuencas oculares. Archosauria es el grupo corona que contiene el ancestro común más reciente de crocodilios y aves y todos sus descendientes. Comprende Pseudosuchia (los «falsos cocodrilos») y Ornithosuchia, que a su vez comprende los dinosaurios y sus parientes, los pterosaurios y las aves.[116] Pseudosuchia se define como los crocodilios vivos y todos los arcosaurios más estrechamente relacionados con los crocodilios que con las aves. Se supone que la división de Pseudosuchia de las aves ocurrió cerca del evento de extinción masiva del Pérmico-Triásico.[117] En los crocodilios modernos las fosas anteorbitales están aisladas externamente y existen simplemente como senos paranasales;[118] estuvieron presentes en la mayoría de sus ancestros fósiles como pequeñas aberturas.[119]
Los crocodilomorfos son los únicos pseudosuquios que han sobrevivido al evento de extinción masiva del Triásico-Jurásico de hace 201,3 millones de años. Durante el período Jurásico Inferior, los dinosaurios dominaron la Tierra y los crocodilomorfos experimentaron importantes diversificaciones adaptativas para llenar nichos ecológicos desocupados por grupos recientemente extinguidos. Las evidencias fósiles descubiertas muestran que los crocodilomorfos mesozoicos tenían una diversidad de formas mucho mayor que los crocodilios modernos. Algunos se convirtieron en pequeños insectívoros de movimientos rápidos, otros en piscívoros especializados, otros en carnívoros marinos y terrestres y unos pocos en herbívoros.[120] La primera etapa de la evolución de los crocodilios fue la de los protosuquios, que evolucionaron a finales del Triásico y principios del Jurásico. Fueron seguidos por los mesosuquios, que se diversificaron ampliamente durante el Jurásico y el Terciario. Los eusuquios aparecieron a finales del Cretácico hace 80 millones de años e incluyen a todos los crocodilios que viven hoy en día.[119]
Los protosuquios eran pequeños, en su mayoría animales terrestres con hocicos cortos y extremidades largas. Tenían una armadura ósea en forma de dos hileras de placas que se extendían desde la cabeza hasta la cola, armadura que conservan la mayoría de los crocodilios modernos. Sus vértebras eran convexas en las dos superficies principales de articulación y sus paladares óseos estaban poco desarrollados. Los mesosuquios experimentaron una fusión de los huesos palatinos para formar un paladar óseo secundario y una gran extensión de los conductos nasales cerca de los huesos pterigoideos. Esto permitió que el animal respirara a través de sus fosas nasales mientras su boca estaba abierta bajo el agua. Los eusuquios continuaron este proceso con las fosas nasales interiores ahora abriéndose a través de una abertura en los huesos pterigoideos. Las vértebras de los eusuquios tenían una superficie de articulación convexa y una cóncava, lo que permite una articulación esferoidal entre las vértebras, ofreciendo mayor flexibilidad y fuerza.[119] El eusuquio más antiguo que se conoce es Hylaeochampsa vectiana del Cretácico inferior de la Isla de Wight en el Reino Unido,[121] seguido por crocodilios como Planocraniidae, los llamados «cocodrilos con pezuña», en el Paleógeno.[122] El género Borealosuchus de América del Norte, con seis especies, vivió entre el Cretáceo y el Paleógeno aunque no se ha decidido su posición filogenética.[123]
Las tres ramas principales de Crocodilia se habían separado a finales del Mesozoico. Los miembros más antiguos conocidos del grupo son los aligatoroides y los gavialoides que vivieron en América del Norte y Europa durante el Campaniense (alrededor de hace 83,6-72,1 millones de años). Aunque los primeros crocodiloides conocidos aparecieron en el Maastrichtiense (alrededor de hace 72,1-66,0 millones de años), ese linaje debe haber estado presente durante el Campaniense y los aligatóridos y gavialoides más antiguos incluyen formas muy derivadas, lo que indica que el momento de la divergencia real entre los tres linajes deben haber sido un evento precampaniense.[124]
Relaciones filogenéticas
editarLas relaciones filogenéticas de los crocodilios han sido objeto de debate y de resultados contradictorios. Muchos estudios y sus cladogramas resultantes, o «árboles genealógicos» de este orden de reptiles, han dado como resultado que las familias de «hocico corto» de Crocodylidae y Alligatoridae son parientes cercanos, con Gavialidae, de hocico largo, como una rama divergente del árbol. El grupo resultante de especies de hocico corto, denominado Brevirostres, fue respaldado sobre todo por estudios que analizaron solo las características de sus esqueletos.[125]
En 2012 Erickson et al. elaboraron una filogenia a partir de secuenciación del ADN que dio como resultado un cladograma de máxima verosimilitud de las relaciones entre crocodilios vivos (excluyendo el yacaré negro, del que no se disponía de evidencia de ADN). En este estudio se descartó la existencia de un grupo diferenciado de Brevirostres, con los gaviálidos de hocico largo más estrechamente relacionados con los cocodrilos que con los caimanes.[15]
| Crocodilia |
| ||||||||||||||||||||||||||||||||||||||||||||||||
Filogenia con otros reptiles
editarLos estudios genéticos revelan las siguientes relaciones filogenéticas para los cocodrilos con respecto a otros reptiles y tetrápodos vivos (incluyendo las secuencias proteicas obtenidas de Tyrannosaurus rex y Brachylophosaurus canadensis). Puede notarse que los cocodrilos son los parientes más cercanos genéticamente a las aves que se consideran dinosaurios vivientes debido a las evidencias fósiles, esto convierte a los reptiles en un taxón parafilético. El clado conformado por las aves, otros dinosaurios, cocodrilos y formas fósiles relacionadas se denomina Archosauria.[126][127][128][129][130][131]
| Tetrapoda |
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Taxonomía
editar- Familia Gavialidae
- Género Gavialis
- Gavial (Gavialis gangeticus)
- Género Tomistoma
- Falso gavial (Tomistoma schlegelii)
- Género Gavialis
Hay dos especies existentes de Gavialidae: el gavial y el falso gavial o gavial malayo. Los gaviales pueden reconocerse por su largo y estrecho hocico, con un prominente abultamiento en la punta. Son escasos y solo se encuentran en el sur de Asia.[23]
- Familia Alligatoridae
- Género Alligator
- Caimán del Misisipi (Alligator mississippiensis)
- Aligátor chino (Alligator sinensis)
- Género Paleosuchus
- Caimán de Cuvier (Paleosuchus palpebrosus)
- Caimán frentiplano (Paleosuchus trigonatus)
- Género Caiman
- Yacaré negro (Caiman yacare)
- Caimán de anteojos (Caiman crocodilus)
- Yacaré overo (Caiman latirostris)
- Género Melanosuchus
- Caimán negro (Melanosuchus niger)
- Género Alligator
Los aligatóridos existentes son dos especies del género Alligator y seis especies de caimanes agrupados en tres géneros. Pueden reconocerse por su hocico ancho, en el que el cuarto diente de la mandíbula inferior no se puede ver cuando la boca está cerrada.[23]
- Familia Crocodylidae
- Género Crocodylus
- Cocodrilo americano (Crocodylus acutus)
- Cocodrilo del Orinoco (Crocodylus intermedius)
- Cocodrilo australiano de agua dulce (Crocodylus johnsoni)
- Cocodrilo filipino (Crocodylus mindorensis)
- Cocodrilo de Morelet (Crocodylus moreletii)
- Cocodrilo del Nilo (Crocodylus niloticus)
- Cocodrilo africano occidental (Crocodylus suchus)
- Cocodrilo de Nueva Guinea (Crocodylus novaeguineae)
- Cocodrilo de las marismas (Crocodylus palustris)
- Cocodrilo marino (Crocodylus porosus)
- Cocodrilo cubano (Crocodylus rhombifer)
- Cocodrilo siamés (Crocodylus siamensis)
El cocodrilo enano de África Occidental tiene un hocico corto.
- Género Mecistops
- Cocodrilo hociquifino africano (Mecistops [Crocodylus] cataphractus)
- Género Osteolaemus
- Cocodrilo enano (Osteolaemus tetraspis)
- Género Crocodylus
Los crocodílidos existentes son doce especies en el género Crocodylus y dos especies en otros géneros. Tienen distintas formas de hocico, pero se pueden reconocer porque el cuarto diente de la mandíbula inferior es visible cuando la boca está cerrada.[23]
- Grupos actuales y extintos
| Crocodilia |
|---|
|
Conservación
editarLa principal amenaza para estos reptiles en todo el mundo es la actividad humana, como la caza y la destrucción de su hábitat. A principios de la década de 1970 se habían comercializado más de dos millones de pieles de crocodilios salvajes de distintas especies, lo que afectó a la mayoría de sus poblaciones, en algunos casos llevándolos casi a la extinción. Desde 1973 la CITES intentó evitar el comercio de partes del cuerpo de animales en peligro de extinción, como las pieles de cocodrilos. Esto resultó ser problemático en la década de 1980, ya que los cocodrilos eran muy abundantes y peligrosos para los humanos en algunas partes de África, y allí era legal cazarlos. En la Conference of the Parties celebrada en Botsuana en 1983, se argumentó en nombre de las poblaciones locales perjudicadas que era razonable vender las pieles cazadas legalmente. A finales de la década de 1970 comenzaron a criarse en distintos países, inicialmente con huevos extraídos de la naturaleza. Para la década de 1980 se producían pieles de cocodrilo en cantidades suficientes como para acabar con el comercio ilícito de crocodilios salvajes. Para el año 2000 treinta países vendían pieles de doce especies de crocodilios, criadas legalmente en la naturaleza o en granjas, y el comercio ilícito de los productos de estos animales casi había desaparecido.[132]
El gavial ha sufrido un declive crónico a largo plazo, combinado con un rápido declive a corto plazo, lo que llevó a la Unión Internacional para la Conservación de la Naturaleza (UICN) a catalogarlo como especie en peligro crítico de extinción.[133] En 1946 la población del gavial era de entre 5000 y 10 000 ejemplares; en 2006, sin embargo, había disminuido un 96-98 %, quedando reducida a un pequeño número de subpoblaciones muy espaciadas de menos de 235 individuos. Este declive a largo plazo se debió, entre otros factores, a la captura de huevos y la caza, o su utilización en la medicina indígena. La rápida disminución de alrededor del 58 % entre 1997 y 2006 fue causada por el creciente uso de redes de enmalle y la pérdida de su hábitat ribereño.[133] La población del gavial continúa estando en peligro por las amenazas ambientales, como los metales pesados y los parásitos protozoarios,[134] aunque desde 2013 su número está aumentando, debido a la protección de los nidos contra los depredadores de huevos.[135]
El aligátor chino estuvo históricamente muy extendido por todo el sistema oriental del río Yangtsé, pero actualmente está restringido a algunas áreas en la provincia de Anhui, al sudeste, debido a la fragmentación y degradación de su hábitat; se cree que la población silvestre solo existe en pequeños estanques dispersos. En 1972 la especie fue declarada en peligro de extinción clase I por el gobierno chino y recibió la máxima protección legal. Desde 1979 se establecieron programas de cría en cautividad en China y América del Norte, creando una población sana en cautividad.[136] En 2008 los caimanes criados en el zoológico del Bronx fueron reintroducidos con éxito en la isla de Chongming.[137] El cocodrilo filipino es quizás el cocodrilo más amenazado y la UICN lo considera en peligro crítico;[138] la caza y los hábitos de pesca destructivos han reducido su población a alrededor de 100 individuos en 2009. Ese mismo año, 50 cocodrilos criados en cautiverio fueron liberados en la naturaleza para ayudar a impulsar su recuperación; el apoyo por parte de la población local es crucial para la supervivencia de la especie.[139]
El caimán del Misisipi también ha sufrido un grave declive a causa de la caza y la pérdida de hábitat en toda su área de distribución, amenazándolo con la extinción. En 1967 se incluyó en la lista de especies en peligro de extinción, pero el Servicio de Pesca y Vida Silvestre de los Estados Unidos y las agencias estatales de vida silvestre en el sur de los Estados Unidos intervinieron y trabajaron para su recuperación. La protección permitió que la especie se recuperara y en 1987 fue retirada de la lista de especies en peligro de extinción.[140] Se han llevado a cabo numerosas investigaciones sobre su cría de cocodrilos en el Rockefeller Wildlife Refuge, una gran extensión de marismas en el estado de Luisiana; los datos obtenidos han incrementado la comprensión de los nidos, las tasas de puesta, la incubación de huevos, la eclosión, la cría y la dieta, y esta información se ha utilizado en otros establecimientos de todo el mundo. Los ingresos obtenidos de la cría de los caimanes mantenidos en el Rockefeller Wildlife Refuge contribuyen a la conservación de los pantanos.[141] Un estudio que examinó las granjas de aligátores en los Estados Unidos mostró que han generado importantes beneficios para la conservación de la especie y la caza furtiva de aligátores silvestres ha disminuido significativamente.[142]
Relación con los humanos
editarCría en cautividad
editarAligátores y cocodrilos se empezaron a criar en cautividad a principios del siglo XX; las instalaciones utilizadas eran similares a las de los zoos y su principal fuente de ingresos era el turismo. A principios de la década de 1960, se estudió la viabilidad de criar estos reptiles a escala comercial en respuesta al declive de muchas especies de crocodilios en todo el mundo. La crianza en granjas puede ser mediante la cría y reproducción de animales en cautiverio de manera autosuficiente, o bien mediante el uso de huevos, juveniles o adultos capturados anualmente en la naturaleza. Las organizaciones comerciales deben cumplir los criterios de la Convención sobre el Comercio Internacional de Especies Amenazadas de Fauna y Flora Silvestres (CITES) demostrando que, en la zona en cuestión, no suponen un impacto adverso en la población silvestre.[143][144]
La cría de cocodrilos y aligátores comenzó debido a la demanda de sus pieles, pero en la actualidad se utilizan casi todas las partes del animal. La piel del costado y del vientre es la que produce el mejor cuero, la carne se come, las vesículas biliares son apreciadas en el este de Asia y las cabezas en ocasiones se venden como adorno.[145][146] En la medicina china tradicional se cree que la carne de cocodrilo cura el resfriado común y previene el cáncer y que varios órganos internos tienen propiedades medicinales.[147]
Ataques a humanos
editarLos crocodilios son depredadores oportunistas sumamente peligrosos en el agua y en las orillas. Hay constancia de ataques a humanos por parte de ocho especies, bien para defender sus territorios, nidos o crías, bien por error mientras ataca a animales domésticos como los perros, o bien para alimentarse, ya que las especies más grandes pueden capturar presas del tamaño de los humanos. Las especies sobre las que existen más referencias a ataques son el cocodrilo marino, el cocodrilo del Nilo y el caimán del Misisipi. Otras especies que en ocasiones han atacado a los humanos son el caimán negro, el cocodrilo de Morelet, el cocodrilo de las marismas, el cocodrilo americano, el gavial y el cocodrilo australiano de agua dulce.[148]
El cocodrilo del Nilo tiene la reputación de ser el mayor asesino de grandes animales, incluidos los humanos, en el continente africano. Está ampliamente distribuido, se encuentra en muchos hábitats y tiene una coloración críptica. Desde una posición de acecho, asomando tan solo los ojos y las fosas nasales sobre el agua, puede arremeter contra los animales que beben en la orilla, los pescadores, los bañistas o las personas que recogen agua o lavan la ropa. Una vez capturada la presa y arrastrada al agua, hay pocas posibilidades de que la víctima escape. El análisis de sus ataques muestra que la mayoría tiene lugar durante la época de cría o cuando los cocodrilos están protegiendo los nidos o los recién nacidos.[149] Aunque muchos ataques no se denuncian, se estima que hay más de 300 por año, el 63 % de los cuales son fatales.[148] Los cocodrilos marinos silvestres en Australia llevaron a cabo 62 ataques confirmados y no provocados que causaron lesiones o muertes entre 1971 y 2004. Estos animales también han causado muertes en Malasia, Nueva Guinea y en otros lugares. Son muy territoriales y rechazan la presencia en sus territorios de otros cocodrilos, humanos o canoas. Los ataques pueden provenir de animales de diversos tamaños, pero los responsables de muertes generalmente son los machos más grandes. A medida que aumenta su tamaño también lo hace su necesidad de presas mamíferas más grandes, y los cerdos, el ganado, los caballos o los humanos están entre sus presas potenciales. La mayoría de las personas atacadas estaban nadando o vadeando, pero hay constancia de dos casos en los que estaban durmiendo en tiendas de campaña.[150]
Hay registro de 242 ataques a humanos no provocados por parte de caimanes del Misisipi entre 1948 y mediados de 2004, que causaron 16 muertes. Diez de las víctimas estaban en el agua y dos en tierra, y se desconocen las circunstancias de los otros cuatro. La mayoría de los ataques se produjeron en los meses más cálidos del año, aunque en Florida, con su clima más cálido, los ataques pueden ocurrir en cualquier época del año.[148] Se considera que los aligátores son menos agresivos que el cocodrilo del Nilo o el marino,[151] pero el aumento de la densidad de la población humana en los Everglades ha acercado a las personas a los territorios de los aligátores y ha aumentado el riesgo de ataques.[148][151] Por el contrario, en Mauritania, donde el tamaño de los cocodrilos se ve gravemente atrofiado por la aridez del clima, los lugareños nadan con ellos sin ser atacados.[88]
Como mascotas
editarAlgunas especies de este orden se comercializan como mascotas exóticas. A algunas personas les resultan atractivos cuando son jóvenes y los dueños de tiendas de mascotas pueden venderlos fácilmente, pero los crocodilios no son buenas mascotas; crecen mucho y son peligrosos y costosos de mantener. Cuando crecen a menudo son abandonados por sus dueños y existen, por ejemplo, poblaciones salvajes de caimanes de anteojos en los Estados Unidos y Cuba. La mayoría de los países tienen regulaciones estrictas para poder tener estos reptiles como mascotas.[152]
En la medicina
editarLa sangre de aligátores y cocodrilos contiene péptidos con propiedades antibacterianas y pueden contribuir al desarrollo de futuros fármacos antibióticos.[153]
En la cultura
editarEn la mitología y el folclore
editarLos crocodilios han tenido un papel destacado en los mitos y leyendas de diversas culturas en todo el mundo, e incluso pueden haber inspirado historias de dragones.[154] En la religión del Antiguo Egipto, Ammyt, la demoníaca devoradora de almas indignas, y Sobek, el dios del poder, la protección y la fertilidad, se representan con cabezas de cocodrilo. Esto refleja la visión en el Antiguo Egipto del cocodrilo como un depredador aterrador y una parte importante del ecosistema del Nilo. El cocodrilo era uno de los animales que los egipcios momificaron.[155] También fueron asociados con varias deidades del agua por los pueblos del África Occidental.[156] Durante el Reino de Benín estaban considerados los «policías de las aguas» y simbolizaban el poder del oba (rey) para castigar a los malhechores.[157] El Leviatán descrito en el Libro de Job puede haberse basado en un cocodrilo.[158][159] En Mesoamérica, los mexicas tenían un dios cocodrilo de la fertilidad llamado Cipactli que protegía los cultivos. También en la mitología azteca, la deidad de la tierra Tlaltecuhtli a veces se representa como un monstruo parecido a un cocodrilo.[160] Los mayas también asociaron a los crocodilios con la fertilidad y la muerte.[161]
El gavial aparece en los cuentos populares de la India. En una historia, un gavial y un mono se hacen amigos cuando el mono le da una fruta al gavial.[162] Historias similares existen en las leyendas de los pueblos nativos de los Estados Unidos y en el cuento popular afroestadounidense de un aligátor y El Hermano Conejo y El Hermano Zorro.[163]
En un cuento popular malayo, el ciervo ratón Sang Kancil quiere cruzar un río para llegar a los árboles frutales en el otro lado, pero Sang Buaya, un cocodrilo, está esperando en el río para comérselo.[164] Una leyenda de Timor Oriental cuenta cómo un niño rescata a un cocodrilo gigante que se queda varado; a cambio, el cocodrilo lo protege por el resto de su vida y cuando muere su espalda escamosa se convierte en las colinas de Timor.[165] Una historia del Tiempo del Sueño australiano habla de un antepasado cocodrilo que tenía el fuego solo para él; un día, un «pájaro del arco iris» le robó sus palos ardientes y se los dio al Hombre, y por eso, según la leyenda, el cocodrilo vive en el agua.[166]
En la literatura
editarLos historiadores antiguos han descrito a los cocodrilos de los registros históricos más antiguos, aunque a menudo sus descripciones incluían tanto leyenda como hechos. El historiador griego Heródoto (c. 440 a. C.) describió el cocodrilo con detalle, aunque gran parte de su descripción era fantasiosa; afirmaba por ejemplo que dejaba la boca abierta para permitir que un pájaro «trochilus» (posiblemente un chorlito egipcio) entrara para quitarle las sanguijuelas que encontrase.[167] El cocodrilo era una de las bestias descritas en el Bestiario de Rochester, de finales del siglo XIII, basado en fuentes clásicas, incluida la Naturalis historia de Plinio el Viejo (c. 79 d. C.)[168] y las Etimologías de Isidoro de Sevilla.[169][170] Isidoro afirma que el cocodrilo se llama así por su color azafrán (en latín croceus, 'azafrán') y que a menudo mide veinte codos (10 m) de largo; además afirmaba que unos peces con crestas serradas podrían matarlo cortando su blando vientre, y que el macho y la hemañbra se turnaban para proteger los huevos.[171]
La primera mención conocida del mito de que los cocodrilos lloran por sus víctimas fue en la Biblioteca de Focio, un patriarca de Constantinopla del siglo IX,[172] y en relatos posteriores como el de Bartolomeo Ánglico en el siglo XIII.[173] El mito estaba ya muy extendido en 1400, cuando el viajero inglés Juan de Mandeville hacía la siguiente descripción de los «cockodrills»:[174]
In that country and by all Ind be great plenty of cockodrills, that is a manner of a long serpent, as I have said before. And in the night they dwell in the water, and on the day upon the land, in rocks and in caves. And they eat no meat in all the winter, but they lie as in a dream, as do the serpents. These serpents slay men, and they eat them weeping; and when they eat they move the over jaw, and not the nether jaw, and they have no tongue.[174]En ese país [el de Preste Juan] y por toda Ind [la India] hay una gran cantidad de cockodrills, una especie de serpiente larga, como dije antes. Y en la noche habitan en el agua, y en el día sobre la tierra, en rocas y en cuevas. Y no comen carne en todo el invierno, sino que descansan como en un sueño, como lo hacen las serpientes. Estas serpientes matan hombres, y los comen llorando; y cuando comen mueven la mandíbula superior, y no la mandíbula inferior, y no tienen lengua.
William Shakespeare habla de las lágrimas de cocodrilo en Otelo (acto IV, escena i), Enrique VI, segunda parte (acto III, escena i) y Antonio y Cleopatra (acto II, escena vii). En español, la expresión 'lágrimas de cocodrilo' se ha incorporado al Diccionario de la lengua española con el sentido de muestra de dolor expresada por alguien que en realidad no lo está sintiendo.[175]
Los crocodilios, especialmente el cocodrilo, han sido personajes recurrentes en historias infantiles a lo largo de la era moderna. Las aventuras de Alicia en el país de las maravillas (1865), de Lewis Carroll, incluye el poema Ved al ágil cocodrilo, parodia del poema moralista de Isaac Watts Contra la ociosidad y la maldad.[176] En la novela de J. M. Barrie, Peter Pan y Wendy (1911), el personaje del capitán Garfio ha perdido su brazo por culpa de un cocodrilo.[177] En El hijo del elefante, uno de los relatos de Los cuentos de así fue (1902), de Rudyard Kipling, el niño elefante consigue su trompa haciendo que un cocodrilo tire con fuerza de su pequeña nariz, haciéndosela más larga, permitiendo así a los elefantes coger fruta de los árboles en lugar de esperar que caiga y hacer otras muchas cosas útiles.[178] El cocodrilo enorme (1978) de Roald Dahl, ilustrado por Quentin Blake, cuenta cómo un cocodrilo deambula por la jungla en busca de niños para comer, probando distintas tretas.[179]
En el deporte y el cine
editarEstos reptiles se utilizan en ocasiones como mascotas de los equipos deportivos, como los de la Universidad de la Florida, que son conocidos como los Florida Gators, en referencia al caimán del Misisipi, y sus mascotas son Albert y Alberta Gator.[180] En cine y televisión, los cocodrilos se representan como peligrosos obstáculos en lagos y ríos, como en la comedia australiana de 1986 Cocodrilo Dundee,[181] o como monstruosos devoradores de hombres en películas de terror como Eaten Alive (1977), Alligator (1980) o Primeval (2007).[182] Algunos medios han intentado retratar a estos reptiles de una manera más positiva o educativa, como la serie documental de vida silvestre de Steve Irwin The Crocodile Hunter.[183] Los crocodilios también están representados por algunos personajes de dibujo animado, como El Lagarto Juancho, de Hanna-Barbera, o Ben Ali Gator, del segmento «La danza de las horas» de la película de Disney de 1940 Fantasía.
Véase también
editarNotas y referencias
editar- Notas
- ↑ La neontología es la parte de la biología que trata de los organismos vivos o extintos recientemente, en contraposición a la paleontología, que estudia el pasado de la vida sobre la Tierra a través de los fósiles.[8]
- ↑ Aunque actualmente en desuso, en español también es válida la grafía 'crocodilo'.[9]
- ↑ Un polifiodonto es cualquier animal cuyos dientes son reemplazados continuamente. Por el contrario, los difiodontos se caracterizan por tener denticiones permanentes y caducas.[46][47]
- ↑ El foramen de Panizza es un orificio que conecta la aorta izquierda y derecha del corazón de todos los crocodilios,[57][58] gracias al cual parte de la sangre oxigenada del ventrículo izquierdo, que fluye hacia la aorta derecha, entra en la aorta izquierda a través de esta abertura, y el animal desvía sangre hacia las partes del cuerpo que más lo necesitan.[59]
- ↑ Los mamíferos tienen un patrón de respiración «de marea»: el aire fluye por las ramificaciones de los pulmones terminando en pequeñas cavidades llamadas alveolos, donde el oxígeno pasa a la sangre y el dióxido de carbono sale de la sangre y entra en los pulmones, momento en el que aire fluye de vuelta por el mismo camino.[66]
- Referencias
- ↑ «Crocodilia (TSN 551734)». Sistema Integrado de Información Taxonómica (en inglés).
- ↑ Schmidt, K. P. (1953). A Checklist of North American Amphibians and Reptiles (6.ª edición). Chicago, University of Chicago Press: American Society of Ichthyologists and Herpetologists.
- ↑ a b Owen, R. (1842). «Report on British Fossil Reptiles. Part II». Report British Association for the Advancement of Science. Plymouth Meeting 1841. Londres: John Murray. pp. 60-240.
- ↑ a b Wermuth, H. (1953). «Systematik der Rezenten Krokodile». Mitteilungen aus dem Museum für Naturkunde in Berlin 29 (2): 375-511. doi:10.1002/mmnz.19530290203.
- ↑ Laurenti, J. N. (1768). Specimen Medicum, Exhibens Synopsin Reptilium Emendatum cum Experimentis Circa Venena et Antidota Reptilium Austriacorum. Viena: Joan. Thom. Nob. de Trattern.
- ↑ Dundee, H. A. (1989). «Higher Category Name Usage for Amphibians and Reptiles». Systematic Biology 38 (4): 398-406. doi:10.2307/2992405.
- ↑ a b c Brochu, C. A. (2003). «Phylogenetic Approaches Toward Crocodylian History». Annual Review of Earth and Planetary Sciences 31: 357-397. doi:10.1146/annurev.earth.31.100901.141308.
- ↑ Lawrence, E., ed. (2003). Diccionario Akal de términos biológicos. Traducido por Codes, R. y Espino, F. J. Akal Ediciones. p. 426. ISBN 84-460-1582-X.
- ↑ Real Academia Española. «crocodilo». Diccionario de la lengua española (23.ª edición).
- ↑ Real Academia Española. «cocodrilo». Diccionario de la lengua española (23.ª edición).
- ↑ Liddell, Henry George; Scott, Robert (1901). «An Intermediate Greek-English Lexicon». Tufts University. Consultado el 23 de enero de 2018.
- ↑ Gove, Philip B., ed. (1986). «Crocodile». Webster's Third New International Dictionary (Encyclopædia Britannica).
- ↑ Kelly, 2006. p. xiii.
- ↑ Schwimmer, David R. (2002). «The Size of Deinosuchus». King of the Crocodylians: The Paleobiology of Deinosuchus. Indiana University Press. pp. 42-63. ISBN 0-253-34087-X.
- ↑ a b c d e f g h Erickson, G. M., et al. (2012). «Insights into the ecology and evolutionary success of crocodilians revealed through bite-force and tooth-pressure experimentation». En Claessens, Leon, ed. PLoS ONE 7 (3): e31781. Bibcode:2012PLoSO...731781E. PMC 3303775. PMID 22431965. doi:10.1371/journal.pone.0031781.
- ↑ a b c d e f g h i j Grigg y Gans, pp. 326-327.
- ↑ a b c d e f g h i j Kelly, pp. 70-75.
- ↑ a b c d e Huchzermeyer, pp. 7-10.
- ↑ a b Farmer, C. G.; Carrier, D. R. (2000). «Pelvic aspiration in the American alligator (Alligator mississippiensis)». Journal of Experimental Biology 203 (11): 1679-1687. PMID 10804158.
- ↑ Grigg y Gans, p. 336.
- ↑ Kelly, D. A. (2013). «Penile anatomy and hypotheses of erectile function in the American Alligator (Alligator mississippiensis): muscular eversion and elastic retraction». Anatomical Record 296 (3): 488-494. doi:10.1002/ar.22644.
- ↑ Huchzermeyer, p. 19.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t Lang, J. W. (2002). «Crocodilians». En Halliday, T.; Adler, K., eds. The Firefly Encyclopedia of Reptiles and Amphibians. Firefly Books. pp. 212-221. ISBN 1-55297-613-0.
- ↑ Fleishman, L. J.; Howland, H. C.; Howland, M. J.; Rand, A. S., Davenport, M. L. (1988). «Crocodiles don't focus underwater». Journal of Comparative Physiology A 163 (4): 441-443. PMID 3184006. doi:10.1007/BF00604898.
- ↑ Grigg y Gans, p. 335.
- ↑ Wever, E. G. (1971). «Hearing in the crocodilia». Proceedings of the National Academy of Sciences 68 (7): 1498-1500. Bibcode:1971PNAS...68.1498W. JSTOR 60727. PMC 389226. PMID 5283940. doi:10.1073/pnas.68.7.1498.
- ↑ Hansen, A. (2007). «Olfactory and solitary chemosensory cells: two different chemosensory systems in the nasal cavity of the American alligator, Alligator mississippiensis». BMC Neuroscience 8: 64. doi:10.1186/1471-2202-8-64.
- ↑ Gans, C.; Clark, B. (1976). «Studies on ventilation of Caiman crocodilus (Crocodilia: Reptilia)». Respiration Physiology 26 (3): 285-301. doi:10.1016/0034-5687(76)90001-3.
- ↑ Putterill, J. F.; Soley, J. T. (2006). «Morphology of the gular valve of the Nile crocodile, Crocodylus niloticus (Laurenti, 1768)». Journal of Morphology 267 (8): 924-939. doi:10.1002/jmor.10448.
- ↑ George, I. D.; Holliday, C. M. (2013). «Trigeminal nerve morphology in Alligator mississippiensis and its significance for crocodyliform facial sensation and evolution». The Anatomical Record 296 (4): 670-680. PMID 23408584. doi:10.1002/ar.22666.
- ↑ Dieter, C. T. (2000). «The Ultimate Guide to Crocodilians in Captivity». Crocodile Encounter publishing. p. 7. ISBN 978-1-891429-10-1.
- ↑ Huchzermeyer, p. 13.
- ↑ Senter, P. (2008). «Voices of the past: a review of Paleozoic and Mesozoic animal sounds». Historical Biology 20 (4): 255-287. doi:10.1080/08912960903033327.
- ↑ Firth, B. T.; Christian, K. A.; Belan, I.; Kennaway, D. J. (2010). «Melatonin rhythms in the Australian freshwater crocodile (Crocodylus johnstoni): a reptile lacking a pineal complex?». Journal of Comparative Physiology B 180 (1): 67-72. doi:10.1007/s00360-009-0387-8.
- ↑ Fish, F. E. (1984). «Kinematics of undulatory swimming in the American alligator». Copeia 1984 (4): 839-843. doi:10.2307/1445326. Archivado desde el original el 21 de octubre de 2013.
- ↑ a b c Mazzotti, pp. 43-46.
- ↑ Sues, p. 21.
- ↑ Reilly, S. M.; Elias, J. A. (1998). «Locomotion in Alligator mississippiensis: kinematic effects of speed and posture and their relevance to the sprawling-to-erect paradigm». The Journal of Experimental Biology 201 (18): 2559-2574. PMID 9716509.
- ↑ a b Kelly, pp. 81-82.
- ↑ Renous, S.; Gasc, J.-P.; Bels, V. L.; Wicker, R. (2002). «Asymmetrical gaits of juvenile Crocodylus johnstoni, galloping Australian crocodiles». Journal of Zoology 256 (3): 311-325. doi:10.1017/S0952836902000353.
- ↑ Grigg y Gans, p. 329.
- ↑ Kelly, p. 69.
- ↑ a b Erickson, Gregory M.; Lappin, A. Kristopher; Vliet, Kent A. (2003). «The ontogeny of bite-force performance in American alligator (Alligator mississippiensis)». Journal of Zoology 260 (3): 317-327. doi:10.1017/S0952836903003819.
- ↑ a b Grigg y Gans, pp. 227-228.
- ↑ Grigg, Gordon; Kirshner, David (2015). Biology and Evolution of Crocodylians. CSIRO Publishing. ISBN 9781486300662.
- ↑ Lawrence, E., ed. (2003). Diccionario Akal de términos biológicos. Traducido por Codes, R. y Espino, F. J. Akal Ediciones. pp. 182, 491. ISBN 84-460-1582-X.
- ↑ Buchtova, M.; Stembirek, J.; Glocova, K.; Matalova, E.; Tucker, A. S. (2012). «=Early Regression of the Dental Lamina Underlies the Development of Diphyodont Dentitions». Journal of Dental Research 91 (5): 491-498. doi:10.1177/0022034512442896.
- ↑ a b Nuwer, Rachel (13 de mayo de 2013). «Solving an alligator mystery may help humans regrow lost teeth». Smithsonian.com. Consultado el 5 de febrero de 2018.
- ↑ LeBlanc, A. R. H.; Reisz, R. R. (2013). «Periodontal ligament, cementum, and alveolar bone in the oldest herbivorous tetrapods, and their evolutionary significance». PLoS ONE 8 (9): e74697. Bibcode:2013PLoSO...874697L. PMC 3762739. PMID 24023957. doi:10.1371/journal.pone.0074697.
- ↑ Wu, Ping, et al. (2013). «Specialized stem cell niche enables repetitive renewal of alligator teeth». Proceedings of the National Academy of Sciences of the United States of America 110 (22): E2009-E2018. Bibcode:2013PNAS..110E2009W. PMC 3670376. PMID 23671090. doi:10.1073/pnas.1213202110. Archivado desde el original el 4 de noviembre de 2013.
- ↑ Ebling, F. John G. «Integument: Reptiles». Encyclopædia Britannica. Consultado el 11 de febrero de 2018.
- ↑ Scott, C. (2004). Endangered and Threatened Animals of Florida and Their Habitats. University of Texas Press. p. 213. ISBN 978-0-292-70529-6.
- ↑ Salleh, Anna (25 de abril de 2012). «Antacid armour key to tetrapod survival». ABC Science. Consultado el 12 de febrero de 2018.
- ↑ Jackson, K.; Butler, D. G.; Youson, J. H. (1996). «Morphology and ultrastructure of possible integumentary sense organs in the estuarine crocodile (Crocodylus porosus)». Journal of Morphology 229 (3): 315-324. doi:10.1002/(SICI)1097-4687(199609)229:3<315::AID-JMOR6>3.0.CO;2-X. Archivado desde el original el 23 de julio de 2018. Consultado el 22 de julio de 2018.
- ↑ Kelly, p. 85.
- ↑ a b c Grigg y Gans, pp. 331-332.
- ↑ Hill, Richard W.; Wyse, Gordon A.; Anderson, Margaret (2006). Fisiología animal. Ed. Médica Panamericana. p. 751. ISBN 8479039906.
- ↑ Kardong, K. V. (1990). Vertebrados. Anatomía comparada, función y evolución. McGraw-Hill Interamericana. pp. 448-449. ISBN 8448602536.
- ↑ «¿Por qué los cocodrilos no sufren infartos?». Muy Interesante. Consultado el 14 de febrero de 2018.
- ↑ Franklin, C. E.; Axelsson, M. (2000). «Physiology: An actively controlled heart valve». Nature 406 (6798): 847-848. PMID 10972278. doi:10.1038/35022652.
- ↑ Axelsson, M.; Franklin, C. E.; Löfman, C. O.; Nilsson, S.; Grigg, G. C. (1996). «Dynamic anatomical study of cardiac shunting in crocodiles using high-resolution angioscopy». The Journal of Experimental Biology 199 (Pt 2): 359-365. PMID 9317958.
- ↑ Milius, S. (2000). «Toothy valves control crocodile hearts». Science News 158 (9): 133. doi:10.2307/3981407.
- ↑ Farmer, C. G.; Uriona, T. J.; Olsen, D. B.; Steenblik, M.; Sanders, K. (2008). «The right-to-left shunt of crocodilians serves digestion». Physiological and Biochemical Zoology 81 (2): 125-137. PMID 18194087. doi:10.1086/524150.
- ↑ Kelly, p. 78.
- ↑ Komiyama, N. H.; Miyazaki, G.; Tame, J.; Nagai, K. (1995). «Transplanting a unique allosteric effect from crocodile into human haemoglobin». Nature 373 (6511): 244-246. Bibcode:1995Natur.373..244K. PMID 7816138. doi:10.1038/373244a0.
- ↑ «El secreto de la respiración del lagarto». ABC. 11 de diciembre de 2013. Consultado el 16 de febrero de 2018.
- ↑ Farmer, C. G.; Sanders, K. (2010). «Unidirectional airflow in the lungs of alligators». Science 327 (5963): 338-340. Bibcode:2010Sci...327..338F. PMID 20075253. doi:10.1126/science.1180219. Archivado desde el original el 24 de junio de 2016. Consultado el 23 de enero de 2018.
- ↑ Schachner, E. R.; Hutchinson, J. R.; Farmer, C. (2013). «Pulmonary anatomy in the Nile crocodile and the evolution of unidirectional airflow in Archosauria». PeerJ 1: e60. PMC 3628916. PMID 23638399. doi:10.7717/peerj.60.
- ↑ a b Uriona, T. J.; Farmer, C. G. (2008). «Recruitment of the diaphragmaticus, ischiopubis and other respiratory muscles to control pitch and roll in the American alligator (Alligator mississippiensis)». Journal of Experimental Biology 211 (7): 1141-1147. PMID 18344489. doi:10.1242/jeb.015339.
- ↑ Munns, S. L.; Owerkowicz, T.; Andrewartha, S. J.; Frappell, P. B. (2012). «The accessory role of the diaphragmaticus muscle in lung ventilation in the estuarine crocodile Crocodylus porosus». Journal of Experimental Biology 215 (5): 845-852. PMID 22323207. doi:10.1242/jeb.061952.
- ↑ Wright, J. C.; Kirshner, D. S. (1987). «Allometry of lung volume during voluntary submergence in the saltwater crocodile Crocodylus porosus». Journal of Experimental Biology 130 (1): 433-436.
- ↑ «AquaFacts: Crocodilians». Vancouver Aquarium. Ocean Wise Conservation Association. Archivado desde el original el 16 de febrero de 2018. Consultado el 16 de febrero de 2018.
- ↑ Webb, Grahame; Manolis, Charlie (2009). Green Guide to Crocodiles of Australia. New Holland. p. 45. ISBN 1-74110-848-9. Archivado desde el original el 4 de octubre de 2009.
- ↑ Mazzotti, p. 54.
- ↑ a b Garnett, S. T. (1986). «Metabolism and survival of fasting estuarine crocodiles». Journal of Zoology 208 (4): 493-502. doi:10.1111/j.1469-7998.1986.tb01518.x.
- ↑ a b Mazzotti, pp. 48-51.
- ↑ Grigg y Gans, p. 330.
- ↑ Rauhe, M.; Frey, E.; Pemberton, D. S.; Rossmann, T. (1999). «Fossil crocodilians from the Late Miocene Baynunah Formation of the Emirate of Abu Dhabi, United Arab Emirates: osteology and palaeoecology». En Whybrow, P. J.; Hill, A., eds. Fossil vertebrates of Arabia New Haven. Yale University Press. pp. 163-185.
- ↑ Mazzotti, Frank J.; Dunson, William A. (1989). «Osmoregulation in Crocodilians». American Zoologist 29 (3): 903-920. JSTOR 3883493. doi:10.1093/icb/29.3.903.
- ↑ a b c d Mazzotti, pp. 52-55.
- ↑ Kelly, p. 68.
- ↑ a b c d e Grigg y Gans, pp. 333-334.
- ↑ Mead, Jim I.; Steadman, David W.; Bedford, Stuart H.; Bell, Christopher J. Bell; Spriggs, Matthew (2002). «New Extinct Mekosuchine Crocodile from Vanuatu, South Pacific». Copeia 3: 632-641. JSTOR 1448145. doi:10.1643/0045-8511(2002)002[0632:nemcfv]2.0.co;2.
- ↑ «Alligator - Where Do Alligators Live?». Habitat Tracker. Florida State University. Archivado desde el original el 25 de julio de 2017. Consultado el 24 de febrero de 2018.
- ↑ a b Alcala y Dy-Liacco, pp. 136-139.
- ↑ Ross, p. 68.
- ↑ Alcala y Dy-Liacco, p. 141.
- ↑ a b Mayell, H. (18 de junio de 2002). «Desert-Adapted Crocs Found in Africa». National Geographic. Consultado el 24 de febrero de 2018.
- ↑ Alcala y Dy-Liacco, pp. 144-146.
- ↑ Dinets, Vladimir; Britton, Adam; Shirley, Matthew (2013). «Climbing behaviour in extant crocodilians». Herpetology Notes 7: 3-7.
- ↑ a b Alcala y Dy-Liacco, pp. 148-152.
- ↑ a b c d Pooley, pp. 76-80.
- ↑ Platt, S. G.; Elsey, R. M.; Liu, H.; Rainwater, T. R.; Nifong, J. C.; Rosenblatt, A. E.; Heithaus, M. R.; Mazzotti, F. J. (2013). «Frugivory and seed dispersal by crocodilians: an overlooked form of saurochory?». Journal of Zoology 291 (2): 87-99. doi:10.1111/jzo.12052.
- ↑ a b c Grigg y Gans, pp. 229-330.
- ↑ Dinets, V.; Brueggen, J. C.; Brueggen, J. D. (2013). «Crocodilians use tools for hunting». Ethology, Ecology and Evolution 27: 74-78. doi:10.1080/03949370.2013.858276.
- ↑ Fish, F. E.; Bostic, S. A.; Nicastro, A. J.; Beneski, J. T. (2007). «Death roll of the alligator: mechanics of twist feeding in water». Journal of Experimental Biology 210 (16): 2811-2818. PMID 17690228. doi:10.1242/jeb.004267.
- ↑ Pooley, pp. 88-91.
- ↑ a b c d Kelly, pp. 86-88.
- ↑ Lance, S. L.; Tuberville, T. D.; Dueck, L.; Holz-schietinger, C.; Trosclair III, P. L.; Elsey, R. M.; Glenn, T. C. (2009). «Multi-year multiple paternity and mate fidelity in the American alligator, Alligator mississippiensis». Molecular Ecology 18 (21): 4508-4520. PMID 19804377. doi:10.1111/j.1365-294X.2009.04373.x.
- ↑ a b c d e Lang, pp. 104-109.
- ↑ Kelly, pp. 89-90.
- ↑ Thorbjarnarson, J. B. (1994). «Reproductive ecology of the spectacled caiman (Caiman crocodilus) in the Venezuelan Llanos». Copeia 1994 (4): 907-919. JSTOR 1446713. doi:10.2307/1446713.
- ↑ Vliet, K. A. (1989). «Social displays of the American alligator (Alligator mississippiensis)». American Journal of Zoology 29 (3): 1019-1031. doi:10.1093/icb/29.3.1019.
- ↑ Martin, B. G. H.; Bellairs, A. D'A. (1977). «The narial excresence and pterygoid bulla of the gharial, Gavialis gangeticus (Crocodilia)». Journal of Zoology 182 (4): 541-558. doi:10.1111/j.1469-7998.1977.tb04169.x.
- ↑ a b c Pooley y Ross, pp. 94-97.
- ↑ Hunt, R. Howard; Ogden, Jacqueline J. (1991). «Selected aspects of the nesting ecology of American alligators in the Okefenokee Swamp». Journal of Herpetology 25 (4): 448-453. JSTOR 1564768. doi:10.2307/1564768.
- ↑ a b c Kelly, p. 91.
- ↑ Silveira, R. D.; Ramalho, E. E.; Thorbjarnarson, J. B.; Magnusson,, W. E. (2010). «Depredation by jaguars on caimans and importance of reptiles in the diet of jaguar». Journal of Herpetology 44 (3): 418-424. doi:10.1670/08-340.1.
- ↑ Wylie, p. 22.
- ↑ a b Huchzermeyer, p. 31.
- ↑ Alcala y Dy-Liacco, p. 145.
- ↑ Campell, Mark R.; Mazzotti, Frank J. (2004). «Characterization of natural and artificial alligator holes». Southeastern Naturalist 3 (4): 583-94. doi:10.1656/1528-7092(2004)003[0583:CONAAA]2.0.CO;2.
- ↑ Fittkau, E.-J. (1970). «Role of caimans in the nutrient regime of mouth-lakes of Amazon affluents (an hypothesis)». Biotropica 2 (2): 138-142. JSTOR 2989771. doi:10.2307/2989771.
- ↑ Alcala y Dy-Liacco, pp. 146-148.
- ↑ Polly, P. David; Guralnick, Rob P.; Collins, Alan G.; Hutchinson, John R.; Speer, Brian R. (1997). «Those diverse diapsids». University of California Museum of Paleontology. Consultado el 4 de febrero de 2018.
- ↑ Hutchinson, John R.; Speer, Brian R.; Wedel, Matt (2007). «Archosauria». University of California Museum of Paleontology. Consultado el 4 de febrero de 2018.
- ↑ Stricherz, Vince (18 de mayo de 2011). «China fossil shows bird, crocodile family trees split earlier than thought». University of Wasington. Consultado el 4 de febrero de 2018.
- ↑ Witmer, L. M. (1997). «The evolution of the antorbital cavity of archosaurs: a study in soft-tissue reconstruction in the fossil record with an analysis of the function of pneumaticity». Journal of Vertebrate Paleontology. 17 (1 sup.): 1-76. doi:10.1080/02724634.1997.10011027. Archivado desde el original el 11 de agosto de 2017..
- ↑ a b c Buffetaut, pp. 26-37.
- ↑ Stubbs, Thomas L.; Pierce, Stephanie E.; Rayfield, Emily J.; Anderson, Philip S. L. (2013). «Morphological and biomechanical disparity of crocodile-line archosaurs following the end-Triassic extinction». Proceedings of the Royal Society B 280 (20131940): 20131940. doi:10.1098/rspb.2013.1940.
- ↑ Martin, Jeremy E.; Benton, Michael J. (2008). «Crown Clades in Vertebrate Nomenclature: Correcting the Definition of Crocodylia». Systematic Biology 57 (1): 173-181. PMID 18300130. doi:10.1080/10635150801910469.
- ↑ Brochu, C. A. (2007). «Systematics and phylogenetic relationships of hoofed crocodiles (Pristichampsinae)». Journal of Vertebrate Paleontology 27 (3, Supl.): 53A. doi:10.1080/02724634.2007.10010458.
- ↑ Brochu, C. A.; Parris, D. C.; Grandstaff, B. S.; Denton, R. K. Jr.; Gallagher, W. B. (2012). «A new species of Borealosuchus (Crocodyliformes, Eusuchia) from the Late Cretaceous-early Paleogene of New Jersey». Journal of Vertebrate Paleontology 32 (1): 105-116. doi:10.1080/02724634.2012.633585.
- ↑ Brochu, C. A. (2003). «Phylogenetic approaches toward crocodylian history». Annual Review of Earth and Planetary Sciences 31: 357-397. Bibcode:2003AREPS..31..357B. doi:10.1146/annurev.earth.31.100901.141308.
- ↑ Holliday, Casey M.; Gardner, Nicholas M. (2012). «A new eusuchian crocodyliform with novel cranial integument and its significance for the origin and evolution of Crocodylia». En Farke, Andrew A., ed. PLoS ONE 7 (1): e30471. Bibcode:2012PLoSO...730471H. PMC 3269432. PMID 22303441. doi:10.1371/journal.pone.0030471.
- ↑ Iwabe, N.; Hara, Y.; Kumazawa, Y.; Shibamoto, K.; Saito, Y.; Miyata, T.; Katoh, K. (2005). «Sister group relationship of turtles to the bird-crocodilian clade revealed by nuclear DNA-coded proteins». Molecular Biology and Evolution 22 (4): 810-813. PMID 15625185. doi:10.1093/molbev/msi075.
- ↑ Chiari, Y.; Cahais, V.; Galtier, N.; Delsuc, Frédéric (2012). «Phylogenomic analyses support the position of turtles as the sister group of birds and crocodiles (Archosauria)». BMC Biol 10 (65). doi:10.1186/1741-7007-10-65.
- ↑ Crawford, N. G.; Faircloth, B. C.; McCormack, J. E.; Brumfield, R. T.; Winker, K.; Glenn, T. C. (2012). «More than 1000 ultraconserved elements provide evidence that turtles are the sister group of archosaurs». Biology Letters 8 (5): 783-786. PMC 3440978. PMID 22593086. doi:10.1098/rsbl.2012.0331.
- ↑ Schweitzer, Mary H.; Zheng, Wenxia; Organ, Chris L.; Asara, John M. (2009). «Biomolecular Characterization and Protein Sequences of the Campanian Hadrosaur B. canadensis». Science 324 (5927): 626-631. doi:10.1126/science.1165069.
- ↑ Schroeter, Elena R.; Cleland, Timothy; Dehart, Caroline J.; Schweitzer, Mary H. (2017). «Expansion for the Brachylophosaurus canadensis Collagen I Sequence and Additional Evidence of the Preservation of Cretaceous Protein». Journal of Proteome Research 16 (2). doi:10.1021/acs.jproteome.6b00873.
- ↑ Asara, John M.; Schweitzer, Mary H.; Freimark, Lisa; Phillips, Matthew (2007). «Protein Sequences from Mastodon and Tyrannosaurus Rex Revealed by Mass Spectrometry». Science 316 (5822): 280-285. doi:10.1126/science.1137614.
- ↑ Adams, William M. (2004). Against Extinction: The Story of Conservation. Earthscan. pp. 197-201. ISBN 1-84407-056-5.
- ↑ a b Choudhury, B. C., Singh, L. A. K., Rao, R. J., Basu, D., Sharma, R. K., Hussain, S. A., Andrews, H. V., Whitaker, N., Whitaker, R., Lenin, J., Maskey, T., Cadi, A., Rashid, S. M. A., Choudhury, A. A., Dahal, B., Win Ko Ko, U., Thorbjarnarson, J., Ross, J. P. (2007). «Gavialis gangeticus». Lista Roja de especies amenazadas de la UICN. Versión 2017.3. Consultado el 11 de abril de 2018.
- ↑ Whitaker, R.; Basu, D.; Huchzermeyer, F. (2008). «Update on gharial mass mortality in National Chambal Sanctuary». Crocodile Specialist Group Newsletter 27 (1): 4-8.
- ↑ Shukla, Neha (10 de junio de 2013). «Ghariyal population rising in Chambal». Times of India. Consultado el 11 de abril de 2018.
- ↑ Hong Xing, Jiang. «Chinese Alligator Alligator sinensis». En Manolis, S.C.; Stevenson, C., eds. Crocodiles. Status Survey and Conservation Action Plan (3.ª edición). Darwin: IUCN - Crocodile Specialist Group.
- ↑ Sautner, Stephen; Delaney, John (18 de julio de 2009). «Critically Endangered Alligators, Born and Raised at WCS's Bronx Zoo, Now Multiplying in China's Wild». Wildlife Conservation Society. Consultado el 11 de abril de 2018.
- ↑ van Weerd, M., C. Pomaro, C., de Leon, J., Antolin, R. y Mercado, V. (2016). «Crocodylus mindorensis». Lista Roja de especies amenazadas de la UICN. Versión 2017.3. Consultado el 11 de abril de 2018.
- ↑ van Weerd, Merlijn (22 de diciembre de 2009). «Local pride offers a boost to endangered crocodile». IUCN. Archivado desde el original el 3 de enero de 2017. Consultado el 11 de abril de 2018.
- ↑ «American Alligator Alligator mississippiensis». United States Fish and Wildlife Service. 1 de febrero de 2008. Consultado el 12 de abril de 2018.
- ↑ «Rockefeller Wildlife Refuge». Louisiana Department of Wildlife and Fisheries. Consultado el 12 de abril de 2018.
- ↑ Moyle, Brendan (2013). «Conservation that's more than skin-deep: alligator farming». Biodiversity and Conservation 22 (8): 1663-1677. doi:10.1007/s10531-013-0501-9.
- ↑ «Crocodiles and Alligator Farms». American Alligator. Consultado el 4 de abril de 2018.
- ↑ Hutton, J. M.; Webb, G. J. W. (1992). «Introducción a la crianza de crocodilianos». En Luxmoore, R. A., ed. Directory of Crocodil3ian Farming Operations. An Introduction to the Farming of Crocodilians, traducción de Andrés E. Seijas (2.ª edición). Gland, Suiza y Cambridge: IUCN. pp. 1-39.
- ↑ Lyman, Rick (30 de noviembre de 1998). «Anahuac Journal; Alligator Farmer Feeds Demand for All the Parts». The New York Times. Consultado el 4 de abril de 2018.
- ↑ «El pujante negocio de criar cocodrilos en México». La Opinión. BBC Mundo. 26 de julio de 2016. Consultado el 4 de abril de 2018.
- ↑ Stromberg, Joseph; Zielinski, Sarah (18 de octubre de 2011). «Ten Threatened and Endangered Species Used in Traditional Medicine: Chinese Alligator». Smithsonian. Consultado el 4 de abril de 2018.
- ↑ a b c d «Crocodilian Attacks». Crocodile Specialist Group. IUCN. Consultado el 9 de abril de 2018.
- ↑ Pooley, Hines y Shield, pp. 174-177.
- ↑ Caldicott, David G. E.; Croser, David; Manolis, Charlie; Webb, Grahame; Britton, Adam (2005). «Crocodile attack in Australia: an analysis of its incidence and review of the pathology and management of crocodilian attacks in general». Wilderness and Environmental Medicine 16 (3): 143-159. PMID 16209470. doi:10.1580/1080-6032(2005)16[143:CAIAAA]2.0.CO;2.
- ↑ a b Kelly, pp. 61-62.
- ↑ Kelly, pp. 108-111.
- ↑ Avasthi, Amitabh (7 de abril de 2008). «Alligator Blood May Lead to Powerful New Antibiotics». National Geographic. Consultado el 10 de abril de 2018.
- ↑ Kelly, p. 41.
- ↑ Kelly, pp. 49-50.
- ↑ Wylie, p. 51.
- ↑ «Benin: an African kingdom». British Museum. Consultado el 12 de abril de 2018.
- ↑ Wylie, p. 28.
- ↑ «Leviatán. Perspicacia, volumen 2». Watch Tower Bible and Tract Society of Pennsylvania. Consultado el 12 de abril de 2018.
- ↑ «Tlaltecuhtli Plaque vs. The Stone of Tizoc». Tenochtitlan. Fordham University's Art History Department. Archivado desde el original el 19 de octubre de 2016. Consultado el 12 de abril de 2018. «Many scholars refer to Tlaltecuhtli in two major depictions, one in her anthropomorphic representation as seen in the Tlaltecuhtli Plaque and the other "a spiny monster with an extended snout (cipactli), based essentially on the crocodile".» citando Nicholson, H. B.; Quiñones Keber, Eloise (1983). Art of Aztec Mexico: Treasures of Tenochtitlan. Washington: National Gallery of Art.
- ↑ Kelly, pp. 58-59.
- ↑ Kelly, pp. 45-46.
- ↑ Kelly, p. 62.
- ↑ Chok, Yoon Foo; Traditional (2008). «Outwitting a Crocodile: A Traditional Malaysian Folktale». Topics Online Magazine. Archivado desde el original el 30 de junio de 2017. Consultado el 12 de abril de 2018.
- ↑ Torchia, Christopher (2007). Indonesian Idioms and Expressions: Colloquial Indonesian at Work. Tuttle Publishing. p. 17.
- ↑ Wylie, pp. 120-121.
- ↑ Heródoto (siglo V a. C.). «Libro II, capítulo 68». Histories.
- ↑ Plinio el Viejo (c. 79 d. C.). «8». Natural History. pp. 37-38.
- ↑ Isidoro de Sevilla (c. siglo VII). «12.6». Etymologies. pp. 19-20.
- ↑ McCulloch, Florence (1960). Mediaeval Latin and French Bestiaries. Chapel Hill: University of North Carolina Press. pp. 22, 28-29.
- ↑ Barney, Stephen A.; Lewis, W. J.; Beach, J. A.; Berghof, Oliver (2006). The Etymologies of Isidore of Seville. Cambridge University Press. p. 260 (XII.vi.19 en la edición original en latín). ISBN 978-0-521-83749-1.
- ↑ Focio (1977). «Tomo VIII : Códices 257-280». Bibliothèque (en francés y griego antiguo). Traducido por R. Henry. París: Les Belles Lettres. p. 93. ISBN 978-2-251-32227-8.
- ↑ Anglicus, Bartholomaeus (c. siglo XIII). «Libro 18». De proprietatibus rerum.
- ↑ a b Mandeville, John (1400). «31. Of the Devil's Head in the Valley Perilous. And of the Customs of Folk in diverse Isles that be about in the Lordship of Prester John». The Travels of Sir John Mandeville.
- ↑ Real Academia Española. «lágrima». Diccionario de la lengua española (23.ª edición).
- ↑ Carroll, Lewis (2002). Fernández Alonso de Armiño, Mauro, ed. Alicia en el país de las maravillas. EDAF. pp. 49-50. ISBN 8441411395.
- ↑ Barrie, J. M. (1911). Peter and Wendy. Hodder and Stoughton. pp. 87-91.
- ↑ Kipling, Rudyard (1962) [1902]. Just So Stories. Macmillan. pp. 45-56.
- ↑ Dahl, Roald (1978). The Enormous Crocodile. Jonathan Cape.
- ↑ «GatorSports homepage». GatorSports. GateHouse Media. Consultado el 13 de abril de 2018.
- ↑ Darnton, Nina (26 de septiembre de 1986). «Film: 'Crocodile Dundee'». The New York Times. Consultado el 13 de abril de 2018.
- ↑ Wylie p. 183.
- ↑ Kelly. p. 228.
Bibliografía
editar- Grigg, Gordon; Gans, Carl (1993). «Morphology and physiology of the Crocodylia». En Glasby, Christopher J.; Ross, Graham J. B.; Beesley, Pamela L., eds. Fauna of Australia. 2A, Amphibia and Reptilia. Australian Government Publishing Service. pp. 326-343. ISBN 978-0-644-32429-8.
- Huchzermeyer, F. W. (2003). Crocodiles: Biology, Husbandry and Diseases. CABI. ISBN 978-0-85199-656-1.
- Kelly, Lynne (2007). Crocodile: Evolution's greatest survivor. Orion. ISBN 978-1-74114-498-7.
- Ross, Charles A., ed. (1992). Crocodiles and Alligators. Blitz. ISBN 978-1-85391-092-0.
- - Sues, Hans-Dieter. «The Place of Crocodilians in the Living World». pp. 14-25.
- - Buffetaut, Eric. «Evolution». pp. 26-41.
- - Mazzotti, Frank J. «Structure and Function». pp. 42-57.
- - Ross, Charles A.; Magnusson, William Ernest. «Living Crocodilians». pp. 58-73.
- - Pooley, A. C. «Food and Feeding Habits». pp. 76-91.
- - Pooley, A. C.; Ross, Charles A. «Mortality and Predators». pp. 92-101.
- - Lang, Jeffrey W. «Social Behaviour». pp. 102-117.
- - Magnusson, William Ernest; Vliet, Kent A.; Pooley, A. C.; Whitaker, Romulus. «Reproduction». pp. 118-135.
- - Alcala, Angel C.; Dy-Liacco, Maria Teresa S. «Habitats». pp. 136-153.
- - Pooley, A. C.; Hines, Tommy C.; Shield, John. «Attacks on Humans». pp. 172-187.
- Wylie, Dan (2013). Crocodile. Reaktion Books. ISBN 978-1-78023-087-0.
Enlaces externos
editar- Portal:Saurópsidos. Contenido relacionado con Saurópsidos.
- International Crocodile Rescue Archivado el 28 de enero de 2011 en Wayback Machine.
- Florida's Museum of Natural History: Crocodilians Archivado el 8 de julio de 2011 en Wayback Machine.