Piridina
| Piridina | |
|---|---|
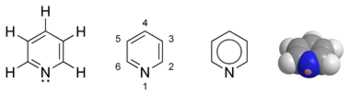
| |
| Nombre IUPAC | Piridina |
| Otros nombres | Azabenceno, Azina, py |
| Fórmula empírica | C5H5N |
| Masa molecular | 79,10 g/mol |
| Estado físico/Color | Líquido/Incoloro |
| Número CAS | 110-86-1 |
| Propiedades | |
| Densidad | 0,9819 g/cm³ a 20 °C |
| Punto de fusión | –41,16 °C (232,0º K) |
| Punto de ebullición | 115,2 °C (388º K) |
| Solubilidad en agua | Miscible en agua |
| Información de Seguridad | |
 
| |
| Frases R: R11-20, R21, R22
Frases S: S26-28 | |
| Exenciones y Referencias[1][2][3] | |
La piridina (fórmula molecular C5H5N, masa molecular: 79,10) es un líquido incoloro de olor desagradable, similar al pescado en mal estado. Pertenece a la familia de los compuestos heterocíclicos aromáticos, y está estructuralmente relacionada con el benceno, siendo la única diferencia entre ellos el reemplazo de un grupo CH del anillo bencénico por un átomo de nitrógeno.
El olor puede llegar a ser nauseabundo y provocar estornudos.
Historia
editarLa piridina impura fue, sin dudas, preparada por los primeros alquimistas al calentar huesos animales y otra materia orgánica,[4] pero la referencia documentada más temprana se adjudica al científico escocés Thomas Anderson.[5][6] En 1849, Anderson examinó el contenido del aceite obtenido a través del calentamiento a altas temperaturas de huesos animales.[6] Entre otras sustancias, separó del aceite un líquido incoloro de olor desagradable, a partir del cual aisló piridina pura dos años después. La describió como altamente soluble en agua, fácilmente soluble en ácidos concentrados y sales después de calentarla y levemente soluble en aceites. Debido a su inflamabilidad, Anderson llamó a la nueva sustancia piridina, del griego πῦρ (pyr) que significa fuego. El sufijo -idina se le suma de acuerdo con la nomenclatura química, como en toluidina, para indicar que un carbono del ciclo contiene un átomo de nitrógeno.[7]
La estructura química de la piridina fue determinada décadas después de su descubrimiento. Wilhelm Körner (1869)[8] y James Dewar (1871)[9] sugirieron independientemente que, análogamente a la quinoleína y al naftaleno, la estructura de la piridina derivaba del benceno mediante la sustitución de un C-H con un átomo de nitrógeno.[10][11] La sugerencia de Körner y Dewar luego fue confirmada experimentalmente cuando la piridina fue reducida a piperidina con alcohol de sodio. En 1876, William Ramsay combinó acetileno y cianuro de hidrógeno en piridina en un horno de acero al rojo. Esta, fue la primera síntesis de un compuesto hetero-aromático.[12][13]
Los métodos contemporáneos en la producción de piridina tienen un bajo rendimiento y una demanda creciente para el compuesto requiere de la búsqueda de nuevas rutas para sintetizarla. Un punto de inflexión ocurrió en 1924 cuando el químico ruso Alekséi Chichibabin desarrolló la Síntesis de piridina de Chichibabin, la cual utiliza reactivos relativamente baratos.[14] Este método aún se usa en la producción industrial de la piridina.[15]
Nomenclatura
editarEl nombre sistemático de la piridina, dentro de la nomenclatura de Hantzsch-Widman recomendada por la IUPAC, es azina. Sin embargo, los nombres sistemáticos para compuestos simples son raramente utilizados, por lo que la nomenclatura de los heterociclos sigue a los nombres comunes. La IUPAC no recomienda el uso de azina en vez de piridina.[16] La numeración de los átomos del anillo de piridina comienza en el nitrógeno. También se utiliza la distribución de las posiciones de los carbonos según el alfabeto griego (α-γ) y cuando se habla de los patrones de sustitución se utiliza (orto, meta y para). Aquí α (orto), β (meta) y γ (para) se refieren a las posiciones 2, 3 y 4 del anillo respectivamente. El nombre sistemático de los derivados de piridina es piridinil, donde la posición del sustituyente es precedida por un número. Sin embargo en este caso también la IUPAC no aconseja el uso optando por el nombre común piridil en vez del sistemático.[17] El derivado catiónico formado por la adición de un electrófilo al nitrógeno es llamado piridinio.
-
4-bromopiridina
-
2,2′-bipiridina
-
Ácido piridina-2,6-dicarboxílico (Ácido dipicolínico)
-
Catión piridinio
Existencia en la naturaleza
editarLa piridina se presenta en un sinfín de compuestos relacionados con la vida (pero no en su forma pura), entre ellos el NAD, la nicotina, la vitamina B3 o niacina (cuya falta causa pelagra), y la vitamina B6 o piridoxina. Los derivados saturados de la piridina tales como la piperidina y las piperideínas también se encuentran presentes en compuestos tales como la coniína, la manojirimicina, la peletierina, la mimosina, la anabasina y la anaferina. Algunas piridinas relacionadas con el ácido nicotínico son los alcaloides de la palma Areca (Arecolina, guvacina), la ricinina de las semillas del ricino, la hermidina de Mercurialis annua y la trigonelina de la alholva. Varias plantas de la familia Celastraceae producen ésteres del ácido evonínico (ácido nicotínico enlazado con una molécula de ácido 2-metilbutírico) y sesquiterpenos tipo agarofurano. Ejemplos de estos alcaloides son la maytolina, maytina, acantotamina, evonina, neoevonina, euonimina, hipocratinas, emarginatinas. Las betalaínas y betaninas también contienen anillos de piridina.
Sin embargo, la piridina pura no está muy extendida en la naturaleza es una sustancia nociva si se la inhala, ingiere o si se absorbe por la piel. Reduce la fertilidad masculina y femenina y es considerada un carcinógeno. Los síntomas de exposición más comunes son: dolor de cabeza, tos, dificultad respiratoria, laringitis, náuseas y vómitos.
En la naturaleza, en su forma más perjudicial se la encuentra en las hojas y raíces de la belladona (Atropa belladonna)[18] y en el malvavisco (Althaea officinalis).[19] Pero como vimos, los derivados de la piridina se encuentran en ciertas biomoléculas como los nucleótidos de piridina y alcaloides. En la vida diaria se encuentran trazas de piridina como componentes volátiles de compuestos orgánicos que se generan en los procesos de tostación y enlatado. Como es el caso del pollo frito,[20] sukiyaki,[21] panceta frita,[22] el queso Beaufort,[23] el aroma del café,[24] el té negro[25] y la miel de girasol.[26] El humo del tabaco[27][28] y el de la marihuana[13] contienen piridina.
Propiedades
editarPropiedades físicas
editarLa piridina es un líquido incoloro cuyo punto de fusión es de –41,6 °C, su punto de ebullición de 115,2 °C. Su densidad es de 0,9819 g/cm³, es cercana a la del agua y su índice de refracción es de 1,5093 a una longitud de onda de 589 nm y a una temperatura de 20 °C.[29] El agregado de una cantidad de 40 mol% de agua a la piridina reduce gradualmente su punto de fusión de –41,6 °C a –65,0 °C.[30] El momento dipolar eléctrico molecular es de 2,22 debye.[31]
La piridina además es diamagnética y su susceptibilidad diamagnética es de –48,7×10−6 cm³·mol−1.[32] La entalpía estándar de formación es de 100,2 kJ·mol−1 en fase líquida[33] y de 140,4 kJ·mol−1 en la fase gaseosa. A 25 °C la piridina tiene una viscosidad[34] de 0,88 mPa/s y una conductividad térmica de 0,166 W·m−1·K−1.[35] La entalpía de vaporización es de 35,09 kJ·mol−1 en el punto de ebullición a presión normal.[36] La entalpía de fusión es de 8,28 kJ·mol−1 en el punto de fusión.[37]
Los piridina cristaliza en un sistema cristalino ortorrómbico con un grupo espacial Pna21 con parámetros de red de a = 1752, b = 897, c = 1135 pm, y 16 unidades de fórmula por celda unidad (medido a 153 K). Por comparación el cristal de benceno es también ortorrómbico, con un grupo espacial Pbca, a = 729,2 p. m., b = 947.1 pm, c = 674,2 p. m. (a 78 K), pero el número de moléculas por celda unidad es de solamente 4.[38] Esta diferencia se debe en parte a la menor simetría mostrada por las moléculas individuales de piridina (C2v vs. D6h para benceno). Un trihidrato (pyridine·3H2O) es conocido, también cristaliza en un sistema ortorrómbico en el grupo espacial Pbca, los parámetros de red son a = 1244, b = 1783, c = 679 pm y ocho unidades de fórmula por celda unidad (medido a 223 K).[30]
El punto crítico de la piridina se encuentra a una presión de 6,70 MPa, 620 K y un volumen de 229 cm³·mol−1.[39] En el rango de temperatura de 340-426 °C su presión de vapor p puede ser descripta por la Ecuación de Antoine
Donde T es temperatura, A = 4,16272, B = 1371,358 K y C = –58,496 K.[40]
La espectro de absorción óptica de la piridina en hexano contiene tres bandas en las longitudes de onda de 95 nm (transición π → π*, absortividad molar ε = 7500 L·(mol·cm)−1), 251 nm (transición π → π*, ε = 2000 L·(mol·cm)−1) y 270 nm (transición n → π*, ε = 450 L·(mol·cm)−1).[41] El espectro de resonancia magnética nuclear de protón (NMR 1H)contiene tres señales con una relación integral de intensidad de 2:1:2 que corresponde a los tres protones químicamente diferentes en la molécula. Estas señales se originan de los α-protones (desplazamiento químico 8,5 ppm), el γ-protón (7,5 ppm) y los β-protones (7,1 ppm). El análogo de carbono de la piridina, el benceno, tiene solo una señal de protón a 7,27 ppm. Los desplazamientos químicos de mayor amplitud de los protones -α y -γ en comparación al benceno se deben a la menor densidad electrónica entre las posiciones alfa y gamma, hecho que puede ser visto a partir de las estructuras de resonancia. La situación es similar para el espectro NMR de 13C tanto de benceno como de piridina: La piridina muestra un triplete a δ (α-C) = 150 ppm, δ (β-C) = 124 ppm and δ (γ-C) = 136 ppm, mientras que en el benceno se observa una línea simple a 129 ppm. Todos los desplazamientos citados son para solventes libres de otras sustancias.[42] Normalmente la piridina se detecta por los métodos de cromatografía de gas y espectrometría de masas.[13]
Propiedades químicas
editarLa piridina es soluble en agua y prácticamente en todos los solventes orgánicos.[29] Es débilmente básica y con ácido clorhídrico forma una sal cristalina (hidrocloruro) que funde a 145-147 °C[43] La mayoría de las propiedades químicas de la piridina son típicas de los compuestos heteroaromáticos. En reacciones orgánicas se comporta tanto como una amina terciaria experimentando la protonación, alquilación, acilación y N-oxidación en el átomo de nitrógeno. Y también como un compuesto aromático experimentando sustituciones nucleófilas.
Debido a su nitrógeno electronegativo en el anillo, la molécula es relativamente electro-deficiente. Y por lo tanto, experimenta más lentamente la sustitución electrófila aromática, que es típica de los derivados del benceno. Sin embargo, en contraposición al benceno y a sus derivados, la piridina es más lábil frente a sustituciones nucleofílicas y frente a la metilación del anillo frente a bases fuertes organometálicas.[44][45] La reactividad de la piridina puede ser diferenciada para tres grupos químicos. Frente a electrófilos, la sustitución electrófila tiene lugar cuando la piridina presenta propiedades aromáticas. Frente a nucleófilos, la piridina reacciona a través del segundo y cuarto átomo de carbono y por lo tanto, se comporta como iminas y carbonilos. La reacción con muchos ácidos de Lewis resulta en la adición al nitrógeno de la piridina, lo cual es similar al comportamiento de las aminas terciarias. La capacidad de la piridina y de sus derivados a oxidarse, formando nitróxidos (N-óxidos), es también una característica de las aminas terciarias.[46]
El nitrógeno de la piridina posee un par solitario de electrones, los cuales son básicos. Debido a su par solitario que no es parte del sistema aromático, la piridina es una base, que posee propiedades similares a la de las aminas terciarias. El pKa del ácido conjugado es de 5,16. La piridina es protonada mediante una reacción con un ácido formando un ion poliatómico positivamente cargado llamado piridinio. Las longitudes de enlace y los ángulos de enlace en la piridina y el piridinio son prácticamente idénticos.[47] El catión piridinio es isoelectrónico con el benceno. El p-toluenosulfonato de piridinio (PPTS) es una sal de piridinio típica; la cual es producida por el tratamiento de la piridina con ácido-p-toluenosulfónico.
La piridina, puede actuar como una base de Lewis, donando su par electrónico a un ácido de Lewis como en el complejo piridina-trióxido de azufre.
La piridina en sí misma es un ligando relativamente débil en la formación de complejos con iones metales de transición. Por ejemplo, forma complejos 1:1 con níquel(II) y cobre (II) con valores de logK1 de ca. 1,9 y 2,6 respectivamente.[48] El espectro de infrarrojo de los complejos de piridina es conocido en detalle.[49] El ácido picolínico que es un derivado sustituido de la piridina, forma complejos fuertes debido al efecto quelante. La 2,2'-bipiridina y la 1,10-fenantrolina, que pueden ser vistos también como derivados sustituidos de la piridina, forman también complejos fuertes como en el caso de la ferroína. La cual puede ser usada como indicador redox en el análisis cuantitativo del hierro.[50]
El modo de coordinación η6, como ocurre en los complejos η6 del benceno, solamente es observado en derivados estéricamente impedidos que bloquean el centro de nitrógeno.[51]
Propiedades moleculares
editarLa piridina posee un sistema conjugado de seis electrones π que se encuentran deslocalizados sobre el anillo. La molécula es plana y sigue la regla de Hückel para los sistemas aromáticos. A diferencia del benceno, la densidad electrónica no se encuentra distribuida uniformemente en el anillo, hecho que explica el efecto inductivo negativo en el átomo de nitrógeno. Por esta razón, la piridina tiene momento dipolar y una energía de resonancia menor a la del benceno (117 kJ·mol−1 para la piridina frente a 150 kJ·mol−1 para el benceno).[52] Pero aun así, posee una energía superior a la del furano, tiofeno y pirrol. La localización electrónica en la piridina se ve reflejada también por la menor longitud del enlace C-N (137 p. m. para el enlace C-N en la piridina frente a 139 p. m. para el enlace C-C en el benceno),[53] mientras que los enlaces C-C de la piridina son de la misma longitud que en el benceno. Estas longitudes de enlace poseen valores intermedios entre los de un enlace simple y un enlace doble, característica típica de un compuesto aromático.
Todos los átomos en el anillo de la piridina son híbridos sp2. El átomo de nitrógeno "dona" sus tres electrones hibridados al sistema anular y su par de electrones "extra" se ubica paralelo al plano de la molécula, hacia afuera y sin participar de la deslocalización electrónica por lo que tampoco contribuye a la aromaticidad de la molécula. Pero este par solitario, influye en las propiedades químicas de la piridina, por ejemplo mediante la fácil formación de enlaces a través de un ataque electrofílico. Sin embargo, debido a la exclusión del par solitario del sistema aromático anular, este par solitario del nitrógeno no puede ejercer un efecto mesomérico positivo sobre el anillo.
Se conocen muchos análogos de la piridina donde el N es reemplazado por otros heteroátomos. El reemplazo de un CH en la piridina por un segundo nitrógeno da lugar a los diazoheterociclos. C4H4N2), con los nombres piridazina, pirimidina y pirazina.
Obtención
editarIndustrialmente, la piridina se obtiene del petróleo y en menor medida, del alquitrán de hulla (en el cual su concentración es de aproximadamente 0,1%), o bien por medio de síntesis a partir del acetaldehído y el amoníaco. También puede ser preparada por destilación del aceite obtenido de la destilación destructiva de huesos.
Síntesis de Chichibabin
editarLa Síntesis de piridina de Chichibabin fue publicada por vez primera en 1924 y sigue industrialmente en uso.[14] En forma general, la reacción puede ser descrita como una reacción de condensación de aldehídos, cetonas, compuestos carbonílicos α,β-insaturados o cualquier combinación de las anteriores en amoníaco o aminas.[54] Específicamente, la piridina no sustituida es producida desde formaldehído y acetaldehído los cuales son reactivos baratos y fácilmente disponibles. Primero, se forma la acroleína en una Condensación de Knoevenagel a partir del acetaldehído y el formaldehído. Es entonces cuando se condensa con acetaldehído y amoníaco formando dihidropiridina, luego se oxida con un catalizador en estado sólido a piridina. Este proceso ocurre en fase gaseosa a 400-450 °C. El producto, consiste de una mezcla de piridina, piridinas metiladas simples (picolina) y (lutidina); su composición depende del catalizador usado y por lo tanto, la reacción puede ser adaptada a las necesidades del que ejecuta la reacción. El catalizador es usualmente una sal de un metal de transición como fluoruro de cadmio (II) o fluoruro de manganeso (II), pero también pueden utilizarse compuestos de cobalto y talio. La piridina obtenida es separada de otros productos mediante un proceso de múltiples etapas.[15]
La aplicación práctica de la síntesis tradicional de Chichibabin está limitada por su bajo rendimiento, normalmente del 20%. Este bajo rendimiento, junto a la alta concentración de derivados no deseados torna a la reacción de Chichibabin muy poco popular cuando no es modificada.[54]
Desalquilación de alquilpiridinas
editarLa piridina puede ser preparada mediante la desalquilación de piridinas alquiladas, las cuales son obtenidas como productos derivados en la síntesis de otras piridinas. La desalquilación oxidativa es llevada a cabo utilizando un catalizador de Óxido de Vanadio (V) con aire[55] o con una desalquilación en vapor con catalizadores basados en níquel,[56][57] o una hidro-desalquilación con un catalizador basado en plata o platino.[58] Se pueden obtener rendimientos de piridina de hasta un 93% con el catalizador basado en níquel[15]
Ciclación de Bönnemann
editarLa trimerización entre una parte de una molécula de nitrilo y dos partes de acetileno en piridina es llamada ciclación de Bönnemann. Esta modificación de la Síntesis de Reppe puede ser activada ya sea por calor o luz. Mientras que la activación térmica requiere altas presiones y temperaturas, la cicloadición foto-inducida ocurre a condiciones ambientales normales con CoCp2(cod) (Cp = ciclopentadienilo, cod = 1,5-ciclooctadieno) como catalizador y puede ser realizada incluso en agua.[59] Se puede producir una serie de derivados de piridina de esta forma. Cuando se usa acetonitrilo como nitrilo, se obtiene 2-metilpiridina, que puede ser desalquilada a piridina.
Métodos de síntesis de derivados de piridina y compuestos relacionados
editarSíntesis de Hantzsch: La primera y principal síntesis de derivados de piridina fue descrita en 1881 por Arthur Rudolf Hantzsch.[60] Se usa normalmente una mezcla 2:1:1 de un β-cetoácido (normalmente acetoacetato, un aldehído (formaldehído) y amoníaco o una sal del amoníaco con el nitrógeno dador. Primero, se obtiene una piridina dihidrogenada, que es consiguientemente oxidada a su correspondiente derivado de piridina. Emil Knoevenagel mostró que las piridinas sustituidas asimétricamente podrían ser producidas mediante este proceso.[61]
En una reacción similar se sintetiza 2-picolina a partir de acetaldehído y amoniaco:[62]
La síntesis de piridina de Kröhnke involucra una condensación de una 1,5-dicetona con acetato de amonio en ácido acético seguida por una oxidación.
La transposición de Ciamician-Dennstedt conlleva la expansión del anillo de pirrol con diclorocarbeno para dar 3-cloropiridina.[63]
En la Síntesis de Gattermann-Skita,[64] Un sal del éster malonico reacciona con diclorometilamina.[65]
La síntesis de Bohlmann-Rahtz permite preparar piridinas sustituidas en dos pasos. El primer paso es la condensación de una enamina (formada por la reacción de una cetona y amoniaco) con un grupo electro atractor (EWG) con una etinilcetona para formar un aminodieno como intermediario. Este compuesto formado sufre una isomería E/Z por acción del calor y una reacción de ciclodeshidratación para formar finalmente las piridinas 2,3,6-trisustituídas. EWG = -COOR, -CN
La síntesis de piridina de Boger se basa en la cicloadición para la formación de piridinas que lleva el nombre de su descubridor Dale L. Boger, quien la reportó por primera vez en 1981.[66] La reacción es una forma de reacción de Diels-Alder reversa en la que una enamina reacciona con una 1,2,4-triazina para formar el núcleo de piridina.[67][68] La reacción es especialmente útil para preparar piridinas que serían difíciles de sintetizar a partir de otros métodos y se ha usado en la síntesis total de varios productos naturales complicados.[69]
Para síntesis de anillos de piridina fusionados con anillos de benceno véase síntesis de quinolinas, Síntesis de isoquinolinas y síntesis de acridinas.
La 2-piridona puede ser obtenida por una reacción de amonólisis de 2-pironas:
En la síntesis de piridonas de Guareschi-Thorpe la cianoacetamida reacciona con una 1,3-dicetona para formar la 2-piridona.[70][71][72][73]
Otros derivados de la piridina pueden ser sintetizados haciendo reaccionar 1,5-dicetonas con acetato de amonio en ácido acético, seguido de oxidación. Para derivados de reducción parcial o total, véase síntesis de piperidina, síntesis de nanofina, síntesis de 2-piperidona, síntesis de glutarimidas y la Síntesis de piperidona de Petrenko-Kritschenko.
Algunas piridinas se pueden obtener por oxidación de las quinolinas. El ácido quinolínico fue sintetizado por Zdenko Hans Skraup, quien observó que las quinolinas metil-sustituidas pueden ser oxidadas con permanganato de potasio al ácido quinolínico, el cual puede ser precursor de otras piridinas.[74] Por ejemplo, la primera descarboxilación puede formar el ácido nicotínico:
Otra aplicación de estos compuestos es la reacción de Hammick, la cual consiste en la descarboxilación térmica de ácidos α-picolínicos para dar como productos 2-piridil-carbinoles, en presencia de compuestos carbonílicos. Esta reacción fue descrita por el químico inglés Dalziel Hammick (1887-1966).[75][76][77]
Reacciones
editarMuchas reacciones que son características del benceno ocurren también en la piridina pero bajo condiciones más complicadas y/o con bajos rendimientos. Debido a la disminución de la densidad electrónica en el anillo aromático, las reacciones de sustitución electrófila aromática son menores en favor de las reacciones de adición de nucleófilos en el átomo de nitrógeno rico en electrones. La adición al átomo de nitrógeno lleva a la consiguiente desaparición de las propiedades aromáticas y al impedimento de la sustitución electrófila. Por otro lado, la sustitución radicalaria y la sustitución nucleófila aromática son experimentadas más fácilmente que en el benceno.[31][44]
Sustituciones electrófilas
editarLa mayoría de las sustituciones electrófilas en la piridina no ocurren o bien ocurren solo parcialmente; sin embargo, el carácter heteroaromático puede ser activado mediante la funcionalización del anillo con sustituyentes electrodadores. Las comunes alquilaciones y acilaciones, como las alquilaciones y acilaciones de Friedel Crafts, usualmente no ocurren debido a que solo conducen a la adición al átomo de nitrógeno. Las sustituciones, usualmente tienen lugar en la posición 3, que es el átomo de carbono más rico en electrones del anillo y por lo tanto es la posición más susceptible a la adición electrófila.
Las sustituciones en las posiciones 2- y 4- de la piridina llevan a un complejo σ energéticamente desfavorable. Pueden ocurrir, sin embargo, utilizando ciertas técnicas experimentales como desarrollar la reacción sobre el N-óxido de piridina seguido de la desoxigenación del átomo de nitrógeno. Entonces, la adición de oxígeno disminuye la densidad electrónica en el átomo de nitrógeno y promueve la sustitución en las posiciones 2- y 4-. Luego, el átomo de oxígeno puede ser removido por diferentes vías, comúnmente se utilizan compuestos de fósforo trivalente o azufre divalente, los cuales son fácilmente oxidados. La trifenilfosfina es un reactivo comúnmente utilizado, el cual se oxida a óxido de trifenilfosfina reduciendo al nitrógeno. Cuando los N-óxidos de piridina con sustituyentes saturados en la posición 2 son tratados con anhídrido trifluoroacético el oxígeno puede migrar del nitrógeno al sustituyente (Reacción de Boekelheide).[78]
Los párrafos siguientes corresponden a reacciones de sustitución electrófila características de la piridina.[44]
La nitración directa de la piridina requiere condiciones extremas y da solamente un bajo rendimiento. La 3-nitropiridina puede ser obtenida al reaccionar la piridina con óxido de nitrógeno (V) en presencia de sodio.[79][80][81] Los derivados de la piridina donde el átomo de nitrógeno se encuentra impedido estérica o electrónicamente pueden ser obtenidos por nitración con tetrafluoroborato de nitronio (NO2BF4). En esta vía, la 3-nitropiridina se obtiene mediante la síntesis de 2,6-dibromopiridina seguida de la remoción de los átomos de bromo.<refNone>Duffy, Joseph L.; Laali, Kenneth K. (1991). «Aprotic Nitration (NO2+BF4−) of 2-Halo- and 2,6-Dihalopyridines and Transfer-Nitration Chemistry of Their N-Nitropyridinium Cations». The Journal of Organic Chemistry 56: 3006. doi:10.1021/jo00009a015.</ref>[82] La sulfonación directa de la piridina es aún más difícil que la nitración directa. Sin embargo, el ácido piridina-3-sulfónico puede ser obtenido con rendimientos aceptables mediante el calentamiento de la piridina en exceso de ácido sulfúrico a 320 °C.[83] La reacción con el grupo SO3 facilita también la adición de azufre al átomo de nitrógeno, especialmente en presencia de un catalizador de Sulfato de mercurio (II).[44][84]
En contraste a lo que ocurre con la nitración y la sulfonación, la bromación directa y la cloración directa de la piridina ocurren fácilmente. La reacción de la piridina con bromo molecular en ácido sulfúrico a 130 °C produce rápidamente 3-bromopiridina. El rendimiento para 3-cloropiridina es más bajo en la cloración con cloro molecular en presencia de cloruro de aluminio a 100 °C. Tanto la 2-bromopiridina como la 2-cloropiridina pueden ser producidas por reacción directa con el halógeno con un catalizador de cloruro de paladio (II).[85]
Sustituciones nucleófilas
editarA diferencia del benceno, la Piridina experimenta eficientemente muchas sustituciones nucleófilas, y es tenida en cuenta como un buen nucleófilo (número dador 33.1). La razón de esto es la densidad electrónica relativa baja de los átomos de carbono en el anillo. Las reacciones incluyen sustituciones con eliminación de un ion hidruro y eliminación-adición con formación de un intermedio arino. Usualmente ocurren en las posiciones 2- y 4- del anillo.[44][45]
Muchas sustituciones son experimentadas fácilmente, pero no con la piridina sola sino con piridinas sustituidas con bromo, cloro, flúor o ácido sulfónico que toman el rol de grupo saliente. Entonces, el flúor es el mejor grupo saliente en la sustitución con compuestos de organolitio. Los compuestos que realizarán el ataque nucléofilo pueden ser alcóxidos, tiolatos, aminas y amoníaco (a presión elevada).[86]
El ion hidruro es generalmente un pobre grupo saliente y actúa como tal solamente en algunas reacciones heterocíclicas como la reacción de Chichibabin que da derivados de piridina aminados en la posición 2-. Aquí, el amiduro de sodio es utilizado como nucleófilo dando como producto 2-aminopiridina. El ion hidruro liberado en esta reacción se combina con un protón de un grupo amino disponible formando moléculas de hidrógeno.[45][87]
Análogamente al benceno, las sustituciones nucleófilas en piridina pueden resultar en la formación de un intermedio heteroarino. A propósito de esto, los derivados de piridina indeseados pueden ser eliminados con buenos grupos salientes usando bases fuertes como el tert-butóxido de potasio o de sodio. La adición subsecuente de un nucleófilo al triple enlace del intermedio posee poca selectividad y el resultado es una mezcla de los dos aductos posibles.[44]
Reacciones radicalarias
editarLa piridina experimenta una serie de reacciones radicalarias, las cuales son usadas en su dimerización en bipiridinas. La dimerización radicalaria de la piridina con sodio elemental o níquel Raney da selectivamente 4,4'-bipiridina[88] o 2,2'-bipiridina,[89] la cual es un reactivo precursor importante en la industria química. Una de las reacciones que involucra radicales libres es la Reacción de Minisci. La misma puede producir 2-tert-butilpiridina cuando reacciona piridina con ácido piválico, nitrato de plata y amonio en ácido sulfúrico con un rendimiento del 97%.[44]
Reacciones sobre el átomo de nitrógeno
editarLos ácidos de Lewis se adicionan fácilmente al átomo de nitrógeno de la piridina formando sales de piridinio. La reacción con haluros de alquilo conduce a la alquilación en el átomo de nitrógeno. Esto, crea una carga positiva en el anillo que incrementa la reactividad de la piridina tanto frente a la oxidación como a la reducción.
La reacción de Zincke se utiliza para la introducción selectiva de radicales en compuestos de piridinio.
La reacción con aminas secundarias, sin embargo, lleva a la apertura del anillo y a la formación de aldehídos de Zincke.
Hidrogenación y reducción
editarLa piperidina (piridina saturada de hidrógeno) se obtiene a través de una reacción con hidrógeno gaseoso en presencia de un catalizador níquel Raney.[90] Esta reacción libera una energía de 193.8 kJ·mol−1,[91] la cual es levemente inferior a la energía de hidrogenación del benceno (205.3 kJ·mol−1).[91]
Se pueden obtener derivados parcialmente hidrogenados con condiciones más suaves. Por ejemplo, la reducción con hidruro de litio y aluminio da una mezcla de 1,4-dihidropiridina, 1,2-dihidropiridina y 2,5-dihidropiridina.[92] La síntesis selectiva de 1,4-dihidropiridina se consigue en presencia de complejos organometálicos de magnesio y cinc,[93] y la (Δ3,4)-tetrahidropiridina se obtiene mediante una reducción electroquímica de la piridina.[94]
Aplicaciones
editarLa piridina y los compuestos relacionados con ella encuentran gran utilidad como disolventes, en análisis químicos, y como reactivos para la síntesis de fármacos, insecticidas, herbicidas, saborizantes, colorantes, adhesivos, pinturas, explosivos, desinfectantes y químicos para el caucho. También es utilizada junto con las picolinas como desnaturalizante en mezclas anticongelantes y en el alcohol etílico, en fungicidas, y en la tinción de textiles.
Biosíntesis
editarLos anillos de piridina y piperidina se encuentran presentes en diversos metabolitos de gran relevancia para los seres vivos. Se comentarán los más representativos:
- Fosfato de piridoxal: Existen dos rutas de biosíntesis, a partir de ribosa (en plantas) y a partir del DOXP (bacteriana):[95]
- Ácido nicotínico: El aspartato puede aceptar un grupo carbamilo por medio de su nitrógeno amino para formar el ácido N-carbamoilaspártico. Además, el ácido aspártico puede condensarse con el fosfato de dihidroxiacetona para formar la vitamina ácido nicotínico.[96][97] Este compuesto es precursor de la nicotina, la arecolina y la ricinina:
- Ácidos picolínicos: La lisina puede ser biosintetizada por la ruta del diaminopimelato (DAP) en hongos o por la ruta de α-aminoadipato (AAA). Durante su biosíntesis se pueden formar metabolitos tales como el ácido picolínico y ácido dipicolínico, los cuales son isómeros del ácido nicotínico y el ácido quinolínico, respectivamente.
- Ácido fusárico: Se forma por la condensación de trans-hexenal y O-acetilhomoserina por la acción de una PKS:[98]
- Desmosina: Aminoácido que se ha demostrado que proviene de cuatro unidades de lisina, de la elastina:
- Pseudoalcaloides piridínicos iridoides: La actinidina es un derivado de la piridina que se encuentra en el aceite esencial de la valeriana (Valeriana officinalis).[99]
- Betalaínas:La base de estos pigmentos alcaloides es el ácido betalámico, el cual se forma por la escisión oxidativa de la DOPA. Cuando el ácido betalámico forma iminas con el nitrógeno de los aminoácidos, se forman las betalaínas. Se clasifican en dos tipos: las betacianinas, que son sales de iminio de la cicloDOPA, y las betaxantinas, que son iminas con aminoácidos o aminas biógenas[100]).
- Piridinas derivadas del triptófano: El ácido nicotínico se puede sintetizar durante la ruta de degradación del triptófano:
Existen diversos organismos que forman derivados de ácido antránílico y los escinden oxidativamente para formar piridinas, como es el caso de la orellanina:
Compuestos relacionados
editar- DMAP o 4-dimetilaminopiridina
- Bipiridina, una compuesto polipiridínico simple que consiste de dos moléculas de piridina unidas por una unión simple.
- Terpiridina, un compuesto formado por tres anillos piridínicos conectados por dos uniones simples.
- Quinolina e Isoquinolina, compuestos formados por un anillo piridínico y un anillo bencénico fusionados.
- Anilina, un derivado bencénico con un grupo amino (-NH2) unido, pero NO una piridina.
- Diazinas, compuestos con uno o más átomos de carbono reemplazados por un átomo de nitrógeno, como la pirazina y la pirimidina.
- Triazinas, compuestos con dos o más átomos de carbono reemplazados por nitrógeno.
- 2,6-lutidina, nombre trivial para la 2,6-dimetilpiridina.
- Colidina, nombre trivial para la 2,4,6-trimetilpiridina.
- p-toluenosulfonato de piridinio (PPTS), una sal formada por intercambio de protones entre la piridina y el ácido p-toluenosulfónico.
Referencias
editar- ↑ «Fichas internacionales de seguridad química (FISQ)». Archivado desde el original el 18 de diciembre de 2008. Consultado el 14 de marzo de 2011.
- ↑ Fichas de datos de seguridad (FDS)
- ↑ Hazardous Substances Data Bank (HSDB)
- ↑ A. Weissberger (Ed.), A. Klingberg (ed.), R.A. Barnes, F. Brody, P.R. Ruby: Pyridine and its Derivatives, Volume 1, 1960, Interscience Pub., New York
- ↑ Anderson, T. Transactions of Royal Society of Edinburg, 16 (1849) 123
- ↑ a b Von Anderson, Th. (1849). «Producte der trocknen Destillation thierischer Materien». Annalen der Chemie und Pharmacie 70: 32. doi:10.1002/jlac.18490700105.
- ↑ Anderson, Th. (1851). «Ueber die Producte der trocknen Destillation thierischer Materien». Annalen der Chemie und Pharmacie 80: 44. doi:10.1002/jlac.18510800104.
- ↑ Körner, W. Giorn. academ. Palermo, vol. 5 (1869)
- ↑ Dewar, J. Chem. News, 23 (1871) 38
- ↑ Albert Ladenburg Lectures on the history of the development of chemistry since the time of Lavoisier., pp. 283–287
- ↑ Raj K. Bansal Heterocyclic Chemistry, (1999) ISBN 81-224-1212-2, p. 216
- ↑ «A. Henninger, aus Paris. 12. April 1877». Berichte der deutschen chemischen Gesellschaft 10: 727. 1877. doi:10.1002/cber.187701001202.
- ↑ a b c Pyridine, IARC Monogrpahs Vol. 77, OSHA, Washington D.C., 1985
- ↑ a b Tscihtschibabin, A.E. (1924). «Über Kondensation der Aldehyde mit Ammoniak zu Pyridinebasen». Journal für praktische Chemie 107: 122. doi:10.1002/prac.19241070110.
- ↑ a b c S. Shimizu, N. Watanabe, T. Kataoka, T. Shoji, N. Abe, S. Morishita, H. Ichimura Pyridine and Pyridine Derivatives, in Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi 10.1002/14356007.a22_399
- ↑ Powell, W. H. (1983). «Revision of the extended Hantzsch-Widman system of nomenclature for hetero mono-cycles». Pure and Applied Chemistry 55: 409-416. doi:10.1351/pac198855020409.
- ↑ D. Hellwinkel: Die systematische Nomenklatur der Organischen Chemie, 4th ed., p. 45, Springer, Berlin, 1998, ISBN 3-540-63221-2
- ↑ G. A. Burdock (ed.) Fenaroli's Handbook of Flavor Ingredients, Vol. II, 3rd Edition, CRC Press, Boca Raton, 1995, ISBN 0-8493-2710-5
- ↑ A. Täufel, W. Ternes, L. Tunger, M. Zobel: Lebensmittel-Lexikon, 4th ed., p. 450, Behr, 2005, ISBN 3-89947-165-2
- ↑ Tang, Jian; Jin, Qi Zhang; Shen, Guo Hui; Ho, Chi Tang; Chang, Stephen S. (1983). «Isolation and identification of volatile compounds from fried chicken». Journal of Agricultural and Food Chemistry 31: 1287. doi:10.1021/jf00120a035.
- ↑ Shibamoto, Takayuki; Kamiya, Yoko; Mihara, Satoru (1981). «Isolation and identification of volatile compounds in cooked meat: sukiyaki». Journal of Agricultural and Food Chemistry 29: 57. doi:10.1021/jf00103a015.
- ↑ Ho, Chi Tang; Lee, Ken N.; Jin, Qi Zhang (1983). «Isolation and identification of volatile flavor compounds in fried bacon». Journal of Agricultural and Food Chemistry 31: 336. doi:10.1021/jf00116a038.
- ↑ Dumont, Jean Pierre; Adda, Jacques (1978). «Occurrence of sesquiterpene in mountain cheese volatiles». Journal of Agricultural and Food Chemistry 26: 364. doi:10.1021/jf60216a037.
- ↑ Aeschbacher, HU; Wolleb, U; Löliger, J; Spadone, JC; Liardon, R (1989). «Contribution of coffee aroma constituents to the mutagenicity of coffee». Food and Chemical Toxicology 27 (4): 227-32. PMID 2659457.
- ↑ Vitzthum, Otto G.; Werkhoff, Peter.; Hubert, Peter. (1975). «New volatile constituents of black tea flavored». Journal of Agricultural and Food Chemistry 23: 999. doi:10.1021/jf60201a032.
- ↑ A. Täufel, W. Ternes, L. Tunger, M. Zobel: Lebensmittel-Lexikon, 4th ed., p. 226, Behr, 2005, ISBN 3-89947-165-2
- ↑ Curvall, Margareta; Enzell, Curt R.; Pettersson, Bertil (1984). «An evaluation of the utility of four in vitro short term tests for predicting the cytotoxicity of individual compounds derived from tobacco smoke». Cell Biology and Toxicology 1 (1): 173. PMID 6400922. doi:10.1007/BF00125573.
- ↑ Schmeltz, Irwin.; Hoffmann, Dietrich. (1977). «Nitrogen-containing compounds in tobacco and tobacco smoke». Chemical Reviews 77: 295. doi:10.1021/cr60307a001.
- ↑ a b Lide, p. 3-448
- ↑ a b Mootz, D. (1981). «Crystal structures of pyridine and pyridine trihydrate». The Journal of Chemical Physics 75: 1517. doi:10.1063/1.442204.
- ↑ a b «RÖMPP Online – Version 3.5». Thieme Chemistry (Stuttgart: Georg Thieme). 2009.
- ↑ Lide, p. 3-673
- ↑ Lide, p. 5-28
- ↑ Lide, p. 6-211
- ↑ Lide, p. 6-221
- ↑ V. Majer, V. Svoboda: Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation, Blackwell Scientific Publications, Oxford, 1985, ISBN 0-632-01529-2
- ↑ Domalski, Eugene S.; Hearing, Elizabeth D. (1996). «Heat Capacities and Entropies of Organic Compounds in the Condensed Phase». Journal of Physical and Chemical Reference Data 25: 1. doi:10.1063/1.555985.
- ↑ Cox, E. (1958). «Crystal Structure of Benzene». Reviews of Modern Physics 30: 159. doi:10.1103/RevModPhys.30.159.
- ↑ Lide, p. 6–67
- ↑ McCullough, J. P.; Douslin, D. R.; Messerly, J. F.; Hossenlopp, I. A.; Kincheloe, T. C.; Waddington, Guy (1957). «Pyridine: Experimental and Calculated Chemical Thermodynamic Properties between 0 and 1500°K.; a Revised Vibrational Assignment». Journal of the American Chemical Society 79: 4289. doi:10.1021/ja01573a014.
- ↑ Joule, p. 14
- ↑ Joule, p. 16
- ↑ Pyridine hydrochloride MSDS Archivado el 18 de octubre de 2014 en Wayback Machine., Alfa Aesar, 26 June 2010
- ↑ a b c d e f g Joule, pp. 125–141
- ↑ a b c D. T. Davies Aromatic heterocyclic chemistry, Oxford University Press, 1992, ISBN 0-19-855660-8
- ↑ R. Milcent, F. Chau: Chimie organique hétérocyclique: Structures fondamentales, pp. 241–282, EDP Sciences, 2002, ISBN 2-86883-583-X
- ↑ T. M. Krygowski, H. Szatyowicz, and J. E. Zachara (2005). «How H-bonding Modifies Molecular Structure and π-Electron Delocalization in the Ring of Pyridine/Pyridinium Derivatives Involved in H-Bond Complexation†». J. Org. Chem. 70 (22): 8859. PMID 16238319. doi:10.1021/jo051354h.
- ↑ IUPAC SC-Database Archivado el 19 de junio de 2017 en Wayback Machine. A comprehensive database of published data on equilibrium constants of metal complexes and ligands
- ↑ Nakamoto, K. (1997). Infrared and Raman spectra of Inorganic and Coordination compounds. Part A (5.ª edición). Wiley. ISBN 0471 16394 5.
- ↑ Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K. (2000). Vogel's Quantitative Chemical Analysis (6.ª edición). New York: Prentice Hall. p. 418. ISBN 0-582-22628-7.
- ↑ C. Elschenbroich Organometallchemie, 6th ed., pp. 524–525, Vieweg+Teubner, 2008, ISBN 3-8351-0167-6
- ↑ Joule, p. 7
- ↑ C. Elschenbroich Organometallchemie, 6th ed., p. 218, Vieweg+Teubner, 2008, ISBN 3-8351-0167-6
- ↑ a b Frank, R.L.; Seven, R. P. (1949). «Pyridines. IV. A Study of the Chichibabin Synthesis». Journal of the American Chemical Society 71 (8): 2629-2635. doi:10.1021/ja01176a008.
- ↑ ICI DE-AS Patent No 1,917,037, (1968)
- ↑ Nippon Kayaku, Japanese patent No. 7039545 (1967)
- ↑ Koei Chemicals, Patent BE 758 201 (1969)
- ↑ F. Mensch Erdöl Kohle Erdgas Petrochemie, 1969, 2, pp. 67–71
- ↑ A. Behr: Angewandte homogene Katalyse, 2008, p. 722, Wiley-VCH, Weinheim, ISBN 3-527-31666-3
- ↑ Hantzsch, A. (1881). «Condensationsprodukte aus Aldehydammoniak und ketonartigen Verbindungen». Berichte der deutschen chemischen Gesellschaft 14: 1637. doi:10.1002/cber.18810140214.
- ↑ Knoevenagel, E.; Fries, A. (1898). «Synthesen in der Pyridinreihe. Ueber eine Erweiterung der Hantzsch'schen Dihydropyridinsynthese». Berichte der deutschen chemischen Gesellschaft 31: 761. doi:10.1002/cber.189803101157.
- ↑ Anderson, T. (1846). «On the constitution and properties of Picoline, a new organic base from Coal Tar» (Free full text at Google Books). Edinburgh New Phil. J. XLI: 146-156; 291-300.
- ↑ Ciamician-Dennstedt Rearrangement, G. L. Ciamician, M. Dennstedt, Ber. 14, 1153 (1881); A. H. Corwin, Heterocyclic Compounds 1, 309 (1950); H. S. Mosher, ibid. 475; P. S. Skell, R. S. Sandler, J. Am. Chem. Soc. 80, 2024 (1958); E. Vogel, Angew. Chem. 72, 8 (1960).
- ↑ L. Gattermann, A. Skita (1916). «Eine Synthese von Pyridin-Derivaten». Ber. 49 (1): 494-501. doi:10.1002/cber.19160490155.
- ↑ Gattermann-Skita Archivado el 16 de junio de 2006 en Wayback Machine., Institute of Chemistry, Skopje, Macedonia
- ↑ Boger, Dale L.; Panek, James S. (May 1981). «Diels-Alder reaction of heterocyclic azadienes. I. Thermal cycloaddition of 1,2,4-triazine with enamines: simple preparation of substituted pyridines». The Journal of Organic Chemistry 46 (10): 2179-2182. doi:10.1021/jo00323a044.
- ↑ Boger, Dale L. (October 1986). «Diels-Alder reactions of heterocyclic aza dienes. Scope and applications». Chemical Reviews 86 (5): 781-793. doi:10.1021/cr00075a004.
- ↑ Li, Jie Jack (2002). Name Reactions A Collection of Detailed Reaction Mechanisms. Berlin: Springer-Verlag. p. 40. ISBN 3-540-43024-5.
- ↑ Boger, Dale L.; Boyce, Christopher W.; Labroli, Marc A.; Sehon, Clark A.; Jin, Qing (January 1999). «Total Syntheses of Ningalin A, Lamellarin O, Lukianol A, and Permethyl Storniamide A Utilizing Heterocyclic Azadiene Diels−Alder Reactions». Journal of the American Chemical Society 121 (1): 54-62. doi:10.1021/ja982078+.
- ↑ Gilchrist, T.L. (1997). Heterocyclic Chemistry ISBN 0-470-20481-8
- ↑ Rybakov V. R.; Bush A. A.; Babaev E. B.; Aslanov L. A. (2004). «3-Cyano-4,6-dimethyl-2-pyridone (Guareschi Pyridone)». Acta Crystallogr E 6 (2): o160-o161. doi:10.1107/S1600536803029295.
- ↑ I. Guareschi (1896). Mem. Reale Accad. Sci. Torino II. 46, 7, 11, 25.
- ↑ Baron, H.; Remfry, F. G. P.; Thorpe, J. F. (1904). «CLXXV.-The formation and reactions of imino-compounds. Part I. Condensation of ethyl cyanoacetate with its sodium derivative». J. Chem. Soc., Trans. 85: 1726-1761. doi:10.1039/ct9048501726.
- ↑ Skraup, Zd. H. (1881). «Synthetische Versuche in der Chinolinreihe». Monatshefte fü Chemie 2 (1): 139. doi:10.1007/BF01516502.
- ↑ Dyson, P.; Hammick, D. L. (1937). «362. Experiments on the mechanism of decarboxylation. Part I. Decomposition of quinaldinic and isoquinaldinic acids in the presence of compounds containing carbonyl groups». J. Chem. Soc.: 1724. doi:10.1039/jr9370001724.
- ↑ Hammick, D. L.; Dyson, P. (1939). «172. The mechanism of decarboxylation. Part II. The production of cyanide-like ions from α-picolinic, quinaldinic, and isoquinaldinic acids». J. Chem. Soc.: 809. doi:10.1039/jr9390000809.
- ↑ Brown, E. V.; Shambhu, M. B. (1971). «Hammick reaction of methoxypyridine-2-carboxylic acids with benzaldehyde. Preparation of methoxy-2-pyridyl phenyl ketones». J. Org. Chem. 36: 2002. doi:10.1021/jo00813a034.
- ↑ Boekelheide, V.; Linn, W. J. J. Am. Chem. Soc. 1954, 76, 1286.
- ↑ Joule, p. 129
- ↑ Bakke, Jan M.; Hegbom, Ingrid; Verne, Hans Peter; Weidlein, Johann; Schnckel, Hansgeorg; Paulsen, Gudrun B.; Nielsen, Ruby I.; Olsen, Carl E. et al. (1994). «Dinitrogen Pentoxide-Sulfur Dioxide, a New nitrate ion system». Acta Chemica Scandinavica 48: 181. doi:10.3891/acta.chem.scand.48-0181.
- ↑ Ono, Noboru; Murashima, Takashi; Nishi, Keiji; Nakamoto, Ken-Ichi; Kato, Atsushi; Tamai, Ryuji; Uno, Hidemitsu (2002). «Preparation of Novel Heteroisoindoles from nitropyridines and Nitropyridones». Heterocycles 58: 301. doi:10.3987/COM-02-S(M)22.
- ↑ Joule, p. 126
- ↑ Gabriel, S. (1882). «Note on nicotinic acid from pyridine». Berichte der deutschen chemischen Gesellschaft 15: 834. doi:10.1002/cber.188201501180.
- ↑ Möller, Ernst Friedrich; Birkofer, Leonhard (1942). «Konstitutionsspezifität der Nicotinsäure als Wuchsstoff bei Proteus vulgaris und Streptobacterium plantarum». Berichte der deutschen chemischen Gesellschaft (A and B Series) 75: 1108. doi:10.1002/cber.19420750912.
- ↑ Joule, p. 130
- ↑ Joule, p. 133
- ↑ Shreve, R. Norris; Riechers, E. H.; Rubenkoenig, Harry; Goodman, A. H. (1940). «Amination in the Heterocyclic Series by Sodium amide». Industrial & Engineering Chemistry 32: 173. doi:10.1021/ie50362a008.
- ↑ Badger, G; Sasse, W (1963). The action of metal catalysts on pyridines 2. p. 179. doi:10.1016/S0065-2725(08)60749-7.
- ↑ Sasse, W. H. F. (1966). «2,2'-bipyridine». Organic Syntheses 46: 5-8. Archivado desde el original el 21 de enero de 2012.
- ↑ Burrows, George H.; King, Louis A. (1935). «The Free Energy Change that Accompanies Hydrogenation of pyridines to piperidines». Journal of the American Chemical Society 57: 1789. doi:10.1021/ja01313a011.
- ↑ a b J.D. Cox, G. Pilcher: Thermochemistry of Organic and Organometallic Compounds, Academic Press, New York, 1970, p. 1–636, ISBN 0-12-194350-X
- ↑ Tanner, Dennis D.; Yang, Chi Ming (1993). «On the structure and mechanism of formation of the Lansbury reagent, lithium tetrakis (N-dihydropyridyl) aluminate». The Journal of Organic Chemistry 58: 1840. doi:10.1021/jo00059a041.
- ↑ De Koning, A (1980). «Specific and selective reduction of aromatic nitrogen heterocycles with the bis-pyridine complexes of bis (1,4-dihydro-1-pyridyl) zinc and bis (1,4-dihydro-1-pyridyl) magnesium». Journal of Organometallic Chemistry 199: 153. doi:10.1016/S0022-328X(00)83849-8.
- ↑ M. Ferles Collection of Czechoslovak Chemical Communications, 1959, 24, pp. 1029–1033
- ↑ Pyridoxal phosphate: Biosynthesis and catabolism. Mukherjeea et al. Biochimica et Biophysica Acta (BBA) - Proteins and Proteomics. Volume 1814, Issue 11, November 2011, Pages 1585-1596
- ↑ Lamberts, Burton L.; Dewey, Lovell J.; Byerrum, Richard U. (1959). «Ornithine as a precursor for the pyrrolidine ring of nicotine». Biochimica et Biophysica Acta 33 (1): 22-6. PMID 13651178. doi:10.1016/0006-3002(59)90492-5.
- ↑ Dawson, R. F.; Christman, D. R.; d'Adamo, A.; Solt, M. L.; Wolf, A. P. (1960). «The Biosynthesis of Nicotine from Isotopically Labeled Nicotinic Acids1». Journal of the American Chemical Society 82 (10): 2628-2633. doi:10.1021/ja01495a059.
- ↑ Two separate key enzymes and two pathway-specific transcription factors are involved in fusaric acid biosynthesis in Fusarium fujikuroi.Studt L.Environ Microbiol. 2016 Mar;18(3):936-56. doi: 10.1111/1462-2920.13150. Epub 2016 Jan 21.
- ↑ Biocyclopedia [1]
- ↑ Clement JS, TJ Mabry, H Wyler y AS Dreiding. 1994. "Chemical review and evolutionary significance of the betalains". En: Caryophyllales, H-D Behnke y TJ Mabry (eds.) 247-261. Springler, Berlin.
Enlaces externos
editar- Wikimedia Commons alberga una categoría multimedia sobre Piridina.
- ATSDR en Español - ToxFAQs™: Polibromobifenilos (PBB) Departamento de Salud y Servicios Humanos de EE. UU. (dominio público)
- ATSDR en Español - Resumen de Salud Pública: Polibromobifenilos (PBB) Departamento de Salud y Servicios Humanos de EE. UU. (dominio público)